RESOLUCIÓN 35379 DE 2025
(junio 10)
<Fuente: Archivo interno entidad emisora>
SUPERINTENDENCIA DE INDUSTRIA Y COMERCIO
Radicado No. 25-90192 VERSIÓN PÚBLICA
Por la cual se autoriza un acuerdo en aplicación del parágrafo único del artículo 1 de la ley 155 de 1959.
LA SUPERINTENDENTE DE INDUSTRIA Y COMERCIO
En ejercicio de sus facultades legales, especialmente las previstas en el parágrafo único del artículo 1 de la Ley 155 de 1959, el numeral 8 del artículo 1 y el numeral 10 del artículo 3 del Decreto 092 de 2022[1], y
CONSIDERANDO
PRIMERO: Que el artículo 333 de la Constitución Política de la República de Colombia establece, primero, que la actividad económica y la iniciativa privada son libres, segundo, la libre competencia como un derecho de todos y, tercero, establece a la empresa como base del desarrollo y con una función social.
"Artículo 333. La actividad económica y la iniciativa privada son libres, dentro de los límites del bien común. Para su ejercicio, nadie podrá exigir permisos previos ni requisitos, sin autorización de la ley.
La libre competencia económica es un derecho de todos que supone responsabilidades.
La empresa, como base del desarrollo, tiene una función social que implica obligaciones. El Estado fortalecerá las organizaciones solidarias y estimulará el desarrollo empresarial.
El Estado, por mandato de la ley, impedirá que se obstruya o se restrinja la libertad económica y evitará o controlará cualquier abuso que personas o empresas hagan de su posición dominante en el mercado nacional.
La ley delimitará el alcance de la libertad económica cuando así lo exijan el interés social, el ambiente y el patrimonio cultural de la Nación.”
SEGUNDO: Que, en el parágrafo único del artículo 1 de la Ley 155 de 1959 se establece la posibilidad que tiene el Gobierno Nacional, a través de la Superintendencia de Industria y Comercio de acuerdo con el numeral 8 del artículo 1 del Decreto 092 de 2022, de autorizar los acuerdos o convenios que, a pesar de limitar la libre competencia económica, defiendan la estabilidad de un sector básico de la economía.
"Artículo 1. (...) Parágrafo: El Gobierno, sin embargo, podrá autorizar la celebración de acuerdos o convenios que no obstante limitar la libre competencia, tengan por fin defender la estabilidad de un sector básico de la producción de bienes o servicios de interés para la economía general.”
Que, en un mismo sentido, el artículo 10 del Decreto 1663 de 1994, estableció que le corresponde a la Superintendencia, la aplicación de las normas sobre promoción de la competencia y prácticas comerciales restrictivas en el mercado de los servicios de salud, en los términos contemplados en ese Decreto, en la Ley 155 de 1959 y el Decreto 2153 de 1992. De la misma manera, el artículo 2 del mismo Decreto, indicó que en el régimen de libre competencia económica en el mercado de servicios de salud se deberá garantizar la variedad de precios y calidades de bienes y servicios, así como mejorar la eficiencia en la prestación de los servicios de salud.
TERCERO: Que mediante comunicación enviada a esta Superintendencia el 26 de febrero de 2025, con número de radicado 25-90192-00, nueve (9) Entidades Promotoras de Salud (EPS): ENTIDAD PROMOTORA DE SALUD SANITAS S.A.S. (en adelante, E.P.S. SANITAS S.A.S.), ASMET SALUD EPS S.A.S., EMSSANAR ENTIDAD PROMOTORA DE SALUD S.A.S. (en adelante, EMSSANAR EPS S.A.S.), ENTIDAD PROMOTORA DE SALUD FAMISANAR S.A.S. (en adelante, EPS FAMISANAR S.A.S.), NUEVA EMPRESA PROMOTORA DE SALUD S.A. (en adelante, NUEVA EPS S.A.), ALIANZA MEDELLIN ANTIOQUIA EPS S.A.S (en adelante, SAVIA SALUD EPS), ENTIDAD PROMOTORA DE SALUD SERVICIO OCCIDENTAL DE SALUD S.A. (en adelante, EPS-SOS S.A.), CAJA DE PREVISIÓN SOCIAL DEL CASANARE (en adelante, CAPRESOCA EPS) y COOSALUD ENTIDAD PROMOTORA DE SALUD S.A. (en adelante, COOSALUD EPS S.A.) (en conjunto se denominarán en adelante, las Intervinientes) presentaron una solicitud de autorización en aplicación del parágrafo único del artículo 1 de la Ley 155 de 1959. El acuerdo tiene el objetivo de defender la estabilidad del sistema general de seguridad social en salud en Colombia (en adelante, SGSSS). Es de resaltar que sobre las Intervinientes en esta solicitud de autorización existen medidas de intervención administrativa impuestas por la SUPERINTENDENCIA NACIONAL DE SALUD (en adelante, SNS)[2].
En esencia, el objeto del acuerdo es negociar de manera conjunta la adquisición de tecnologías en salud para que, una vez realizada la negociación, cada una de las intervinientes en el acuerdo puedan adquirir y distribuir estas tecnologías. Esto fue expuesto por las Intervinientes así:
"El objeto principal del acuerdo es garantizar la estabilidad de un sector básico de la producción de bienes y servicios destinados a satisfacer las necesidades e de salud de la población colombiana, a través del sistema General de Seguridad Social en Salud - SGSSS, puesto que actualmente este sistema enfrenta serios problemas de desabastecimiento de tecnologías en salud (medicamentos, dispositivos médicos, alimentos de propósitos medico especial APME). Este acuerdo sería suscrito de manera voluntaria por los agentes interventores de las nueve EPS intervenidas por la Superintendencia Nacional de Salud, y se comprometerían a negociar de manera conjunta, adquirir individualmente y entregar las tecnologías en salud a los afiliados del SGSSSS, en el marco de la política de gobierno nacional.
Se busca fomentar el crecimiento económico, generar empleo y garantizar el acceso oportuno a los tratamientos médicos, especialmente para la población más vulnerable, que no tiene los recursos para adquirirlos de manera particular, contribuyendo así al mandato legal establecido en el Plan Nacional de Desarrollo "Prosperidad para todos”[3].
Además, las Intervinientes establecieron este acuerdo estaría dividido en tres etapas. En cada etapa se planea negociar diferentes tipos de medicamentos, dispositivos médicos y alimentos con propósitos médicos. La descripción de cada etapa es la siguiente:
"Primera Etapa: Medicamentos de alto costo, en sus diferentes presentaciones y concentraciones, los cuales están destinados a tratar enfermedades raras o crónicas graves en pacientes cuyas condiciones de salud requieren tratamientos especiales y prolongados.
Segunda Etapa: Dispositivos médicos como pañales desechables en sus diferentes marcas, características y tallas, más Alimentos de Propósito Médico Especial - APME, en sus diferentes marcas, presentaciones y/o concentraciones.
Tercera Etapa: Medicamentos genéricos o de bajo costo por el alto volumen en su consumo, en sus diferentes presentaciones y concentraciones.”[4]
Con el acuerdo proyectado por las Intervinientes se crearía un escenario de colaboración para efectuar negociaciones directas con los proveedores del sector farmacéutico, orientadas a la adquisición de tecnologías en salud, dispositivos médicos y alimentos de propósito médico especial a mejores precios. Con esto también se busca eliminar la intermediación en la cadena de distribución y, según lo expuesto en la solicitud, permitiría superar deficiencias estructurales del mercado, en particular aquellas asociadas al acceso restringido, los sobrecostos y la insuficiencia de insumos esenciales para la atención médica.
Es importante señalar que, una vez recibida la solicitud de autorización para el acuerdo objeto de análisis, la Superintendencia ha realizado varias actuaciones. Por un lado, requirió a las Intervinientes con el fin de que suministraran información adicional relacionada con el alcance del acuerdo e información del mercado. Además, le solicitó al Ministerio de Salud y Protección Social (en adelante, Ministerio de Salud) y a la SNS la expedición de un concepto técnico sobre la viabilidad del acuerdo objeto de análisis[5]. Las actuaciones más relevantes realizadas en este trámite administrativo son:
Tabla No. 1. Actuaciones relevantes en la presente actuación administrativa
| No. | Radicado | Fecha | Tiipo de actuación |
| 1 | 25-90192-0 | 27/02/2025 | Solicitud de autorización de acuerdo para defender la estabilidad del sector salud presentada por las nueve (9) EPS intervenidas. |
| 2 | 25-90192-5 | 25/03/2025 | Requerimiento de información enviado a las nueve (9) EPS intervenidas. |
| 3 | 25-90192-6 | 10/04/2025 | Solicitud de concepto técnico sobre la viabilidad del acuerdo propuesto por las nueve (9) EPS intervenidas a la SNS. |
| 4 | 25-90192-7 | 10/04/2025 | Solicitud de concepto técnico sobre la viabilidad del acuerdo propuesto por las nueve (9) EPS intervenidas al Ministerio de Salud y Protección Social. |
| 5 | 25-90192-11 | 21/04/2025 | Respuesta al requerimiento de información por parte de las nueve (9) EPS. |
| 6 | 25-90192-12 | 23/04/2025 | Concepto técnico emitido por la SNS sobre la viabilidad del acuerdo propuesto por las nueve (9) EPS intervenidas. |
| 7 | 25-90192-14 | 14/05/2025 | Requerimiento de complemento de información a las (9) EPS intervenidas. |
| 8 | 25-90192-14 | 14/05/2025 | Requerimiento de información a la SNS. |
| 9 | 25-234102 (Acumulado a esta actuación) | 15/05/2025 | Concepto técnico emitido por el Ministerio de Salud y Protección Social sobre la viabilidad del acuerdo propuesto por las nueve (9) EPS intervenidas. |
| 10 | 25-90192-16 | 26/05/2025 | Respuesta a requerimiento de información formulado a la SNS |
Fuente: Radicaciones Sistema de Trámites - Superintendencia de Industria y Comercio.
CUARTO: Que, como se estableció al inicio de esta Resolución, esta solicitud de autorización de un acuerdo está basada en la excepción establecida en el parágrafo único del artículo 1 de la Ley 155 de 1959. Como ya se ha mencionado antes, el parágrafo citado establece la posibilidad de que la Superintendencia de Industria y Comercio autorice la celebración de acuerdos que, a pesar de limitar la libre competencia económica, "tengan la finalidad de defender la estabilidad de un sector básico de la producción de bienes o servicios de interés para la economía en general”[6]. El concepto de "sector básico de la producción de bienes y servicios”, como elemento fundamental para aprobar un acuerdo, que en la práctica sería anticompetitivo, fue definido de la siguiente forma en el artículo 2.2.2.29.5.1. del Decreto 253 de 2022, así:
"Acuerdos para la estabilidad de un sector de la economía sectores básicos
Artículo 2.2.2.29.5.1. Para los efectos del parágrafo del Artículo 1 de la Ley 155 de 1959, considérense sectores básicos de la producción de bienes o servicios de interés para la economía general y el bienestar social, todas aquellas actividades económicas que tengan o llegaren a tener en el futuro importancia fundamental para estructurar racionalmente la economía del país y abastecerlo de bienes o servicios indispensables al bienestar general, tales como:
1. El proceso de producción y distribución de bienes destinados a satisfacer las necesidades de la alimentación, el vestido, la sanidad y la vivienda de la población colombiana;
2. La producción y distribución de combustibles y la prestación de los servicios bancarios, educativos, de transporte, energía eléctrica, acueducto, telecomunicaciones y seguros."
La autorización de este tipo de acuerdo lo debe realizar la Superintendencia de Industria y Comercio y esta función específica está a cargo del Despacho de la Superintendente de Industria y Comercio, como lo indican el numeral 8 del artículo 1 y el numeral 10 del artículo 3 del Decreto 092 de 2022[7]. Para que el acuerdo objeto de análisis pueda ser aprobado debe cumplir con unos requisitos relacionados con la información que debe suministrar el solicitante de la autorización. En el capítulo primero del título VII de la Circular Única de la Superintendencia de Industria y Comercio[8] se establecen cinco (5) elementos para tener en cuenta al analizar un acuerdo o convenio que limite la libre competencia.
El primer elemento es la explicación del sector básico de la producción de bienes o servicios. Con esto, el solicitante debe indicar el código CIIU al que pertenece la actividad que realiza en el mercado. Igualmente, indicar el porcentaje del PIB asociado con el sector durante los dos últimos años, así como el número de empleos generados por el sector. Finalmente, explicar la interdependencia con otros sectores.
Lo segundo que debe tener la solicitud es la descripción del acuerdo en el que se identifique las empresas que participan, el objeto, la duración y las normas específicas que se pretenden inaplicar de manera temporal. Finalmente, los solicitantes de la autorización presentarán una justificación del acuerdo, con la descripción de los efectos en la defensa de la estabilidad del sector.
El tercer elemento está relacionado con la precisión sobre las normas de competencia para determinar las eficiencias que se buscan obtener en la cadena productiva del sector respectivo y el libre acceso a los mercados de bienes y servicios ofrecidos por las empresas del sector. Igualmente, se deberá analizar la existencia de variedad de precios y calidad de bienes y servicios.
En cuarto lugar, se establecerá un mecanismo de seguimiento a través del cual la Superintendencia pueda vigilar el comportamiento de los agentes en el mercado, específicamente en el marco del acuerdo objeto de análisis. Para lograr ejecutar esta función, se debe señalar la información que suministrarán los participantes en el acuerdo.
Finalmente, la Superintendencia analiza que el acuerdo objeto de evaluación no esté vinculado a una conducta objeto de investigación o que haya sido sancionada. Además, tiene el deber de reiterar que la inobservancia en los términos de la autorización puede constituir una violación de las normas de protección de la libre competencia económica.
Con el fin de abordar cada uno de los temas que exige el marco legal sobre protección de la libre competencia económica en los acuerdos descritos en el parágrafo único del artículo 1 de la Ley 155 de 1959, esta resolución estará dividida en cinco (5) capítulos:
- En el primer capítulo se expondrán las generalidades del mercado de aseguramiento en salud y de la compra de medicamentos, específicamente en el mercado institucional, así como las precisiones frente al PIB asociado con el sector, la actividad económica y el análisis desde un punto de vista laboral que se vería involucrado con el acuerdo objeto de análisis (considerando quinto).
- En el segundo, la Superintendencia hará un recuento del problema que dio lugar a la solicitud de autorización de acuerdo objeto de análisis, así como de los elementos que están involucrados en el acuerdo propuesto (considerando sexto).
- En el tercer capítulo, la Autoridad de Competencia analizará tanto los antecedentes nacionales como internacionales de este tipo de acuerdos (considerando séptimo).
- En el cuarto capítulo se describirán las eficiencias que se pretenden lograr con el acuerdo objeto de análisis (considerando octavo).
- En el quinto capítulo se establecerán el esquema de seguimiento que implementará la Superintendencia para vigilar el cumplimiento del acuerdo (considerando noveno).
- Por último, se realizarán algunas recomendaciones desde el punto de vista de la libre competencia con el fin de asegurar el cumplimiento del régimen de protección de la libre competencia económica (considerando décimo) en la ejecución del acuerdo.
QUINTO: Que, con el fin de analizar el acuerdo del cual se solicitó autorización, es necesario describir cómo es la estructura y funcionamiento del mercado de salud en Colombia. Además, se presentarán los argumentos que sustentan porqué el mercado de salud, y específicamente, el de Tecnologías en Salud, es un sector básico, en los términos del marco regulatorio de competencia. Por último, la Superintendencia expondrá los elementos exigidos para el análisis de este tipo de acuerdos, los cuales son, la identificación del acuerdo en la clasificación internacional CIIU, el porcentaje del PIB asociado al sector, el número de empleos generados por el sector y, finalmente, la interdependencia con otros sectores de la economía.
5.1. Estructura y funcionamiento de la salud en Colombia
De conformidad con lo establecido en la Ley 100 de 1993, la estructura del sector salud en Colombia se organiza mediante el Sistema de Seguridad Social Integral, dentro del cual se encuentra el Sistema General de Seguridad Social en Salud (en adelante, SGSSS).
Según el Decreto 780 de 2016, el sector salud adopta la siguiente estructura. Por un lado, el Ministerio de Salud se erige como la cabeza del sector. Esta entidad tiene como funciones: formular, adoptar, dirigir, coordinar, ejecutar y evaluar la política pública en materia de salud, salud pública y promoción social en salud. Además, participa en la formulación de políticas en materia de pensiones, beneficios económicos periódicos y riesgos laborales. Bajo su dirección se encuentran dos fondos especiales: el Fondo de Solidaridad y Garantía, que administra recursos financieros del sistema de salud, y el Fondo de Salvamento y Garantías para el Sector Salud (en adelante, FONSAET), cuyo objetivo es asegurar el pago de obligaciones de las Empresas Sociales del Estado en riesgo financiero o bajo intervención. De igual forma, el MINSALUD se apoya en órganos sectoriales de asesoría y coordinación que abordan temáticas específicas, como lo es la Comisión Nacional de Precios de Medicamentos y Dispositivos Médicos (en adelante, CNPMDM).
Por otro lado, el sector salud comprende entidades adscritas[9] y vinculadas[10]. Entre las entidades adscritas más relevantes se encuentran: el Instituto Nacional de Salud, que lidera la investigación y vigilancia en salud pública; el Instituto Nacional de Vigilancia de Medicamentos y Alimentos (en adelante, INVIMA), encargado de la regulación y control sanitario de medicamentos y alimentos; la Superintendencia Nacional de Salud, como entidad de inspección, vigilancia y control; y la Administradora de los Recursos del Sistema General de Seguridad Social en Salud (en adelante, ADRES)[11].
La estructura del sector salud en Colombia refleja un modelo institucional caracterizado por la articulación entre un ente rector central, como el Ministerio de Salud, y un conjunto de entidades descentralizadas que cumplen funciones especializadas de regulación, control, financiamiento, investigación y prestación de servicios. Esta organización busca garantizar la formulación coherente de políticas públicas en salud, así como asegurar la eficiencia en la administración de los recursos, la vigilancia del sistema y la protección efectiva del derecho fundamental a la salud de la población.
En línea con lo expuesto, la Ley 100 de 1993 estructuró el sistema de salud en Colombia alrededor de dos mercados de competencia gerenciada[12]: el mercado de aseguramiento en salud y el mercado de provisión de servicios de salud. A continuación, se presentan las características principales de ambos mercados.
5.1.1. Mercado de aseguramiento en salud
En el mercado de aseguramiento en salud, las aseguradoras -denominadas Empresas Promotoras de Salud (en adelante, EPS)- reciben una prima denominada Unidad de Pago por Capitación (en adelante, UPC), a cambio de garantizar la prestación del Plan de Beneficios en Salud (en adelante, PBS) a los afiliados. La UPC[13] constituye una variable que condiciona tanto la atención en salud dentro del SGSSS como la operación de cada uno de sus agentes, en la medida en que corresponde al valor de la prima de aseguramiento en salud que el sistema reconoce, con ciertas distinciones, por cada persona afiliada o beneficiaria. Su determinación está en función del perfil epidemiológico de la población relevante, de los riesgos cubiertos y de los costos de prestación del servicio en condiciones medias de calidad, tecnología y hotelería[14]. Este valor debe cubrir el costo promedio del PBS y los costos de administración. Por su parte, el PBS corresponde a todos los servicios y tecnologías financiados con la UPC para satisfacer las necesidades de salud de la población residente en el territorio colombiano.
En relación con lo anterior, es importante destacar que tanto los contenidos del PBS como el valor y la composición de la UPC son regulados por el Ministerio de Salud. Ello implica que el precio de los servicios de aseguramiento en salud no es el resultado de la libre fijación por parte de los agentes del mercado ni de la interacción espontánea entre la oferta y la demanda, sino que obedece a una imposición normativa.
Los afiliados ejercen simultáneamente la calidad de tomadores y beneficiarios del servicio de aseguramiento. Además, pueden incluir en su cobertura a los integrantes de su núcleo familiar, quienes, sin ser cotizantes, adquieren la condición de asegurados y beneficiarios. De este modo, los usuarios acceden a los servicios de salud mediante la libre elección de la EPS en la que desean afiliarse, optando por uno de los siguientes regímenes de aseguramiento:
i. Régimen Contributivo: comprende el conjunto de normas que regulan la vinculación de los individuos y sus familias al SGSSS mediante el pago de una cotización individual o familiar, financiada directamente por el afiliado o en concurrencia con su empleador.
ii. Régimen Subsidiado: constituye la vía efectiva de acceso al derecho fundamental a la salud para la población pobre y vulnerable, en cumplimiento de la obligación estatal de garantizar su afiliación al sistema.
Ahora bien, las variables de competencia en el mercado de aseguramiento en salud se encuentran en función de las fuentes de ingresos de las EPS, ya que éstas determinan sus incentivos competitivos. A saber, los ingresos de una EPS provienen principalmente de dos fuentes. La primera corresponde a la afiliación de un mayor número de usuarios ya que por cada afiliado el SGSSS reconoce a la EPS una UPC, generando así ingresos adicionales. La segunda fuente de ingresos deriva, por un lado, del ajuste en el valor de la UPC para compensar insuficiencias en la cobertura de los costos asociados al PBS y, por otro lado, del incremento en los recobros por servicios de salud no incluidos en la UPC. Adicionalmente, se han establecido mecanismos de cobro directo a los afiliados, como las cuotas moderadoras[15] y los copagos[16], que son recaudados directamente por las EPS. Estos pagos corresponden a sumas que los afiliados deben pagar en función de sus ingresos[17] para acceder a determinados servicios de salud.
En materia de recobros por servicios de salud, se ha dispuesto que los costos en que incurran las EPS para financiar tecnologías o servicios no imputables a la UPC -es decir, aquellos no incluidos en el PBS- deben ser asumidos por la ADRES a través de las cuentas de recobro, cuyo fin es resarcir los gastos inicialmente cubiertos por las EPS[18]. Por lo tanto, las EPS pueden verse incentivadas a competir al incluir en sus coberturas servicios de salud no contemplados en el PBS o, por el contrario, al negar la prestación de servicios incluidos o no en el PBS, con el objetivo de presentar mayores recobros ante la ADRES y así aumentar sus ingresos mediante el reconocimiento y pago de las tecnologías y servicios efectivamente prestados a sus afiliados y beneficiarios[19].
En conclusión, en el mercado colombiano de aseguramiento en salud, la variable económica relevante no es el precio, dado que este se encuentra regulado, sino la cantidad de afiliados que cada EPS logra captar. En este contexto, las EPS compiten fundamentalmente a través de estrategias de diferenciación orientadas a hacer más atractiva su oferta de servicios frente a los usuarios. Esta diferenciación se materializa en diversos aspectos: la calidad técnica y administrativa del servicio reflejada en la pertinencia y oportunidad de los tratamientos, la idoneidad del personal médico contratado y las condiciones de infraestructura y logística de las instituciones prestadoras de servicios de salud afiliadas; la cobertura geográfica, que implica garantizar al usuario el acceso efectivo y oportuno a la red de servicios en todo el territorio nacional, minimizando las barreras de distancia; la amplitud y claridad en la cobertura del aseguramiento, mediante mecanismos efectivos de información sobre los derechos en salud y la red de prestadores disponibles; y, finalmente, la facilidad y oportunidad en el acceso a los servicios, evaluada en términos de la agilidad en los trámites administrativos, los tiempos de asignación de citas, la dispensación de medicamentos y la realización de procedimientos clínicos[20].
5.1.2. Mercado de provisión de servicios y tecnologías en salud
En el mercado de provisión de servicios[21] y tecnologías en salud[22], los proveedores compiten por ofrecer sus productos a las aseguradoras, que actúan como compradoras en representación de sus afiliados. En este mercado, las aseguradoras seleccionan y negocian con proveedores públicos y/o privados buscando obtener la mejor combinación posible entre precio y calidad, con el fin de optimizar los recursos y maximizar el bienestar de los afiliados.
Dentro de los proveedores en el mercado de salud se encuentra:
i. Prestadores de Servicios de Salud (PSS): se consideran como tales las Instituciones Prestadoras de servicios de salud (en adelante, IPS), los profesionales independientes de salud y el transporte especial de pacientes, que estén inscritos en el Registro Especial de Prestadores de Servicios de Salud -REPS y cuenten con servicios habilitados. Esto no incluye a las entidades con objeto social diferente, teniendo en cuenta que sus servicios no se financian con cargo a los recursos del Sistema General de Seguridad Social en Salud -SGSSS[23].
ii. Proveedores de Tecnologías en Salud (PTS): se considera toda persona natural o jurídica que realice la disposición, almacenamiento, venta o entrega de tecnologías en salud, incluyendo a los operadores logísticos de tecnologías en salud, gestores farmacéuticos, organizaciones no gubernamentales, universidades y otras entidades privadas que realicen estas actividades[24].
Cabe resaltar que las IPS (públicas, privadas o mixtas) desarrollan actividades de atención en los distintos niveles de complejidad. Estas instituciones incluyen desde consultorios y centros de salud de primer nivel hasta hospitales generales y especializados de segundo y tercer nivel, así como unidades de urgencias, entre otras.
Por su parte, los proveedores de tecnologías en salud abarcan a los fabricantes, importadores y distribuidores de medicamentos, dispositivos médicos, reactivos de laboratorio, equipos de diagnóstico, sistemas de información clínica, etc. Estos proveedores deben registrar sus productos ante el INVIMA y cumplir con los requisitos de calidad, seguridad y eficacia establecidos en la Ley 100 de 1993 y en el Decreto 780 de 2016, que reglamenta, entre otros, el mantenimiento de equipos de tecnologías de información y comunicaciones utilizados en la atención en salud. Este actor es quien, normalmente, asegura la logística de distribución y ofrece mantenimiento y capacitación sobre el uso correcto de equipos, formando así un eslabón esencial para que las EPS e IPS cumplan con su misión de brindar servicios integrales y de alto estándar técnico.
En consecuencia, el desarrollo de la industria de la salud en Colombia se encuentra enmarcado dentro del régimen normativo del SGSSS, el cual se fundamenta en el concepto de pluralismo estructurado[25]. Este modelo combina la dinámica competitiva de los mercados de aseguramiento y de provisión de servicios y tecnologías en salud, con una intensa intervención estatal. En efecto, el Estado, a través de sus entidades centralizadas y descentralizadas en materia de salud, define tanto los contenidos del servicio (el producto) como su remuneración (el precio), los cuales deben ser ofrecidos por las aseguradoras públicas y privadas a los usuarios del sistema.
5.1.3. Interacción entre el mercado de aseguramiento y el mercado de provisión de servicios y tecnologías en salud
La interacción entre el mercado de aseguramiento y el mercado de provisión de servicios y tecnologías en salud en Colombia está reglamentada principalmente por el Decreto 780 de 2016, en especial por el Capítulo 4 del Título 3 de la Parte 5, el cual fue sustituido en su totalidad por el Decreto 441 de 2022. Este cuerpo normativo establece el marco jurídico que rige las relaciones contractuales entre las Entidades Responsables de Pago (ERP) -como las EPS- y los Prestadores de Servicios de Salud (PSS) y Proveedores de Tecnologías en Salud (PTS), regulando las fases precontractual, contractual y postcontractual de dichas relaciones, así como mecanismos de protección al usuario.
Es importante precisar que tanto el artículo 156 como el artículo 179 de la Ley 100 de 1993[26] establecieron la posibilidad de que las EPS presten directamente los servicios de salud o contraten con IPS y/o profesionales de la salud para que sean estos agentes quienes se encarguen de prestar el servicio. A saber:
"ARTÍCULO 156. CARACTERÍSTICAS BÁSICAS DEL SISTEMA GENERAL DE SEGURIDAD SOCIAL EN SALUD. El Sistema General de Seguridad Social en Salud tendrá las siguientes características: (...)
k) Las Entidades Promotoras de Salud podrán prestar servicios directos a sus afiliados por medio de sus propias Instituciones Prestadoras de Salud, o contratar con Instituciones Prestadoras y profesionales independientes o con grupos de práctica profesional, debidamente constituidos”. (Subrayado propio)
"ARTÍCULO 179. CAMPO DE ACCIÓN DE LAS ENTIDADES
PROMOTORAS DE SALUD. Para garantizar el Plan de Salud Obligatorio a sus afiliados, las Entidades Promotoras de Salud prestarán directamente o contratarán los servicios de salud con las Instituciones Prestadoras y los profesionales. Para racionalizar la demanda por servicios, las Entidades Promotoras de Salud podrán adoptar modalidades de contratación y pago tales como capitación, protocolos o presupuestos globales fijos, de tal manera que incentiven las actividades de promoción y prevención y el control de costos. Cada Entidad Promotora deberá ofrecer a sus afiliados varias alternativas de Instituciones Prestadoras de Salud, salvo cuando la restricción de oferta lo impida, de conformidad con el reglamento que para el efecto expida el Consejo Nacional de Seguridad Social en Salud (...)." (Subrayado propio)
En este contexto, el régimen de interacción se desarrolla en las siguientes etapas:
En primer lugar, frente a la etapa precontractual, el artículo 2.5.3.4.2.1 del Decreto 780 de 2016 estableció que la negociación entre las partes debe contar con información mínima que permita una correcta identificación de las condiciones de prestación. Las Entidades Responsables de Pago (ERP) deben suministrar la caracterización de la población y el modelo de atención en salud. Los Prestadores de Servicios de Salud (PSS) deben presentar su modelo de prestación, la oferta de servicios habilitados y su capacidad instalada; mientras que los Proveedores de Tecnologías en Salud (PTS) deben describir su modelo de disposición de tecnologías, su capacidad logística y su oferta de productos.
En segundo lugar, frente a la etapa contractual, el artículo 2.5.3.4.2.2 del Decreto 780 de 2016 señaló un contenido mínimo obligatorio para los acuerdos de voluntades, que incluye, entre otros, el objeto del acuerdo, la duración y condiciones de ejecución, el lugar de prestación o provisión, las redes habilitadas de prestación, las modalidades de pago, las tarifas, las guías clínicas, las rutas integrales de atención en salud, los indicadores de calidad y el procedimiento de seguimiento contractual. Igualmente, los acuerdos deben prever los plazos de pago conforme a las Leyes 1122 de 2007, 1438 de 2011 y 2024 de 2020, así como los mecanismos de solución de controversias.
Con respecto a las modalidades de pago, el artículo 2.5.3.4.2.3 del Decreto 780 de 2016 estableció la posibilidad de que las Entidades Responsables de Pago (ERP) y los Prestadores de Servicios de Salud (PSS) o Proveedores de Tecnologías en Salud (PTS) pacten libremente una o varias modalidades de pago en los acuerdos de voluntades, de acuerdo con el objeto contractual y las obligaciones asumidas por las partes. Estas modalidades deben corresponder a los servicios y tecnologías en salud incluidos en el PBS o en el Plan de Intervenciones Colectivas[27]. En particular, la norma citada prevé cuatro modalidades principales: Pago individual por caso[28], pago global prospectivo[29], pago por capitación[30] y pago por evento[31].
Ahora bien, de acuerdo con el parágrafo 1 del artículo 2.5.3.4.2.3 del Decreto 780 de 2016, cuando se pacten modalidades de pago prospectivas, es obligatorio incorporar una nota técnica como instrumento de soporte técnico y financiero del acuerdo. Esta nota técnica, regulada en el artículo 2.5.3.4.2.4 del Decreto 780 de 2016, debe incluir como mínimo: (i) la población objeto total y susceptible de atención, caracterizada epidemiológicamente y en términos de riesgo; (ii) las frecuencias de uso previstas de los servicios y tecnologías durante la vigencia del acuerdo; (iii) los costos unitarios acordados para cada servicio o tecnología; y (iv) la periodicidad de evaluación y monitoreo del cumplimiento de las proyecciones. La nota técnica debe elaborarse utilizando los códigos estandarizados definidos por el Ministerio de Salud y el INVIMA, garantizando uniformidad en la referencia de los servicios y tecnologías. Su contenido constituye un anexo obligatorio del acuerdo de voluntades y un insumo esencial para la activación de mecanismos de ajuste de riesgos en caso de desviaciones significativas entre las proyecciones y la ejecución real.
En tercer lugar, en la etapa postcontractual, los artículos 2.5.3.4.3.1 y siguientes del Decreto 780 de 2016 regularon el seguimiento a la ejecución de los acuerdos de voluntades. Particularmente, se estableció la obligatoriedad de utilizar indicadores de estructura, proceso y resultado para medir la calidad asistencial, la gestión administrativa y los resultados en salud. Así mismo, se creó la obligación de realizar auditorías administrativas, financieras, técnico- científicas, de calidad, de cuentas médicas conforme al Manual Único de Devoluciones, Glosas y Respuestas.
Respecto a los reconocimientos económicos, los artículos 2.5.3.4.5.1 a 2.5.3.4.5.8 del Decreto 780 de 2016 introdujeron medidas destinadas a incentivar el cumplimiento contractual y sancionar las prácticas dilatorias. En cuanto a la duración, renovación y liquidación de los acuerdos de voluntades, el artículo 2.5.3.4.6.1 del decreto en mención estableció que se debe identificar su plazo de vigencia, prever fórmulas de actualización de valores y regular la renovación automática. Además, el artículo 2.5.3.4.6.2 dispuso que la liquidación contractual debe realizarse dentro de los cuatro meses siguientes a la terminación del acuerdo.
En cuarto lugar, en relación con los mecanismos de protección al usuario, el Decreto 780 de 2016 reforzó las obligaciones de las Entidades Responsables de Pago (ERP) para garantizar el acceso efectivo a los servicios de salud.
En conclusión, el marco normativo vigente establece un régimen de contratación en el sistema de salud que busca armonizar la interacción entre el mercado de aseguramiento y el mercado de provisión de servicios y tecnologías en salud, garantizando condiciones de transparencia, eficiencia, calidad, protección de los usuarios y sostenibilidad financiera del Sistema General de Seguridad Social en Salud.
5.2. El sector salud como sector básico de la economía
El artículo 49 de la Constitución Política señala que la salud es un servicio público a cargo del Estado, cuyo acceso debe ser garantizado a todas las personas bajo los principios de eficiencia, universalidad y solidaridad. Esta disposición impone al Estado el deber de organizar, dirigir y reglamentar el sistema de salud, asegurando que los servicios de promoción, prevención, diagnóstico, tratamiento, rehabilitación y paliación sean prestados de manera integral, accesible, oportuna, continua y universal[32].
Por su parte, la Corte Constitucional, a través de su jurisprudencia reiterada y en aplicación del artículo 2o de la Ley Estatutaria 1751 de 2015, ha definido el derecho a la salud como un derecho fundamental autónomo e irrenunciable, cuya protección abarca ámbitos individuales y colectivos de la vida humana[33]. La Corte ha señalado que la salud, en su dimensión de servicio público a cargo del Estado[34], debe ser prestada conforme a los principios de dignidad humana, igualdad, equidad, eficiencia, calidad, solidaridad y sostenibilidad, los cuales orientan la prestación de los servicios de salud y se materializan a través del denominado Sistema de Salud[35].
Ahora, desde una perspectiva económica, el sector salud se considera un sector básico de la economía nacional por dos razones principales. Por un lado, actúa como un bien público con efectos positivos sobre la productividad agregada, dado que el estado de salud de la población influye directamente en la acumulación de capital humano y la eficiencia de los factores productivos[36]. Esta externalidad positiva posiciona al sector salud como un determinante del crecimiento económico[37], razón por la cual su estabilidad y capacidad de respuesta deben entenderse como bienes transcendentales para la economía. Por otro lado, a nivel macroeconómico, el gasto en salud representa una proporción creciente del PIB, reflejo del envejecimiento demográfico, la transición epidemiológica y la consolidación institucional del sistema de aseguramiento. En efecto, el financiamiento del sistema a través de rentas parafiscales, transferencias del gobierno nacional y gasto de bolsillo configura un flujo de recursos que dinamiza la demanda interna, con efectos multiplicadores sobre otros sectores productivos, como la industria farmacéutica, el comercio especializado y los servicios profesionales[38].
En virtud de lo anterior, esta Superintendencia considera que se encuentra acreditada la hipótesis prevista en el parágrafo del artículo 1o de la Ley 155 de 1959, relativa a la caracterización del sector salud como un sector básico de la producción de bienes y servicios de interés para la economía general. La adecuada operación del sector salud resulta indispensable para estructurar racionalmente la economía nacional y garantizar el bienestar general de la población. Así, en su doble dimensión como derecho fundamental de rango constitucional y como servicio público esencial, el sector salud ostenta una naturaleza inequívoca que justifica su reconocimiento como un sector estratégico, cuya estabilidad y funcionamiento adecuado constituyen condiciones necesarias para el desarrollo de los fines del Estado social de derecho. En todo caso, es de señalar que el numeral 1 del artículo 1 del Decreto 1304 de 1964 estableció como sector básico todo lo que tiene que ver con los temas relacionados con "sanidad”.
5.3. Información relevante del sector de acuerdo con el capítulo primero del título VII de la Circular Única de la Superintendencia de Industria y Comercio
Como se mencionó en el numeral anterior, el mercado en el que se desarrollará el acuerdo objeto de análisis está clasificado como un "sector básico de la producción de bienes o servicios”. Adicionalmente, es necesario describir, primero, la Clasificación Industrial Internacional Uniforme en la que se puede ubicar el sector específico en el que se ejecutaría el acuerdo objeto de análisis. En segundo lugar, se definirá el porcentaje del PIB asociado al sector analizado. Luego, se realizará una caracterización de los empleos generados por el sector. Finalmente, se describirá la interdependencia del sector objeto de análisis con otros sectores de la economía.
5.3.1. Clasificación Industrial Internacional Uniforme (CIIU)
Las Intervinientes en esta operación, de acuerdo con la información suministrada en este trámite administrativo, participan en dos mercados relevantes. El primero, es el mercado de aseguramiento en salud en el cual gestionan los recursos de la salud y garantizan la prestación de los servicios a través de la red de atención y el suministro de TES. El segundo es el mercado institucional de TES que incluye la compra, distribución y provisión de medicamentos, dispositivos médicos, APME y otros insumos[39]. En este caso las EPS tiene la función de adquirir las TES con el fin de prestarle atención a los pacientes y, actualmente, esto lo hacen a través de los Gestores Farmacéuticos. Los CIIU de las actividades económicas que se verían involucrados en el acuerdo objeto de análisis son los siguientes:
Tabla No. 2. CIIU del mercado aseguramiento en salud.
| Código CIIU | Descripción | Nota explicativa |
| 8610 | Actividades de hospitales y clínicas, con internación | Comprende los servicios médicos a corto y largo plazo, actividades de diagnóstico, tratamiento y rehabilitación, suministrados a pacientes internos en hospitales o clínicas. También se incluyen los sanatorios (preventorios), clínicas de reposo, asilos, instituciones hospitalarias para enfermos mentales, y centros de rehabilitación, que posean un componente importante de supervisión y vigilancia directa de médicos titulados, y otras instituciones sanitarias con servicio de alojamiento, incluso los hospitales de bases militares y prisiones, que realizan actividades de atención médica y técnico-quirúrgica como diagnóstico, tratamiento, operaciones, análisis, servicios de urgencias, etc. Esta clase incluye: - Las actividades que consisten principalmente en la atención de pacientes internos, que se realizan bajo la supervisión directa de médicos y abarcan: - La atención odontológica a pacientes internos en hospitales cuando se presta por profesionales vinculados a la institución de internación. - El servicio de personal médico general y especializado y paramédico en: - Servicio de apoyo diagnóstico: imagenología (rayos x, ecografía, TAC, RMN, gamagrafía, etc.), laboratorio clínico, endoscopia, patología etc., cuando se prestan a pacientes internos. - Servicio de complementación terapéutica: rehabilitación (por terapistas), optometría, psicología, nutrición, fonoaudiología, etc., cuando se prestan a pacientes internos. - Servicios de urgencias. - Servicios de quirófanos, servicios de farmacia, servicios de comida a pacientes internos y otros servicios hospitalarios. - Servicios de centros de planificación familiar que proporcionan tratamiento médico tales como esterilización e interrupción del embarazo, cuando se realizan con internación. |
| 8621 | Actividades de la práctica médica, sin internación | Esta clase incluye: - Las actividades de consulta y tratamiento médico en el campo de la medicina general y especializada, realizada por médicos generales, especialistas y cirujanos. - La práctica médica realizada a pacientes externos o ambulatorios, en consultorios privados, centros médicos, puestos de salud, clínicas asociadas con empresas, escuelas, hogares para ancianos, organizaciones sindicales y asociaciones profesionales, así como en el domicilio de los pacientes. - Los centros de planificación familiar que proporcionan tratamiento médico, tales como esterilización y la terminación de embarazo, sin internación. - Los servicios de consulta médica a pacientes internos ejercida por médicos no vinculados a la institución de internación. |
| 8691 | Actividades de apoyo diagnóstico | Esta clase incluye - Las actividades relacionadas con la salud humana, realizadas por unidades independientes a las instituciones prestadoras de servicios de salud con internación. - Las actividades de laboratorios médicos como: - Laboratorios de radiología y otros centros de diagnósticos por imagen. - Laboratorios de análisis de sangre. - Laboratorios de medicina forense. |
Fuente: Cámara de Comercio de Bogotá, httDs://linea.ccb.ora.co/descripcionciiu/. fecha de consulta 23/05/2025
Tabla No. 3. CIIU del mercado institucional de TES
| Código CIIU | Descripción | Nota explicativa |
| 2100 | Fabricación de productos farmacéuticos, sustancias químicas medicinales productos botánicos de uso farmacéutico | Comprende la fabricación de productos y preparaciones farmacéuticos para uso humano o veterinario. Estos productos químicos deben ser grado farmacéutico, aptos para consumo humano o aplicación medicinal o veterinaria.Esta clase incluye:- La fabricación de sustancias químicas utilizadas en la preparación de productos químicos farmacéuticos, ya sea mediante cultivos de microorganismos o mediante procesos químicos y que constituyen los ingredientes activos.- La fabricación de ampollas, tabletas, cápsulas, ampolletas, ungüentos, polvos o soluciones de medicamentos, etc.- Las vitaminas básicas, incluso proteínas, aminoácidos esenciales; el ácido ascórbico (vitamina C) y sus sales, complementos vitamínicos, etc.- La producción de ácido salicílico y acetilsalicílico con sus sales y ésteres. - La fabricación de medicamentos que actúan en la sangre: inhibidores de la coagulación; preparaciones antianémicas, sueros, antisueros, plasmas y otras fracciones de la sangre. - La fabricación de antiinfecciosos en general: antibióticos sistémicos; agentes sistémicos para infecciones por hongos; antimicobacterianos; antivirales y vacunas. - La fabricación de productos químicos anticonceptivos de uso externo y de medicamentos anticonceptivos hormonales. - La fabricación de sustancias de diagnóstico: pruebas de diagnóstico (test de embarazo y ovulación). - La fabricación de sustancias radiactivas para realizar diagnósticos in vitro. - La fabricación de productos de biotecnología. - La fabricación de azúcares químicamente puros como glucosa, dextrosa, galactosa y glucósidos. - La fabricación de apósitos médicos impregnados, guatas medicinales, vendajes para fracturas y otros productos para suturas. - Los productos botánicos pulverizados, graduados, molidos o preparados; incluye los productos homeopáticos sólidos, líquidos o glóbulos, para uso farmacéutico. - Los derivados del opio, como la morfina, la cocaína y sus derivados para uso terapéutico. - Los demás alcaloides vegetales y glucósidos extraídos de plantas o semillas, como la quinina y la atropina, para uso terapéutico. - Las sulfas, sulfamidas y derivados, utilizados generalmente como antibióticos. - La fabricación de soluciones de uso hospitalario: soluciones intravenosas, soluciones de irrigación y la producción de agua esterilizada para ampolletas. - La elaboración de productos endocrinos y fabricación de extractos endocrinos, etc. |
| - La fabricación de medicamentos que actúan en la sangre: inhibidores de la coagulación; preparaciones antianémicas, sueros, antisueros, plasmas y otras fracciones de la sangre. - La fabricación de antiinfecciosos en general: antibióticos sistémicos; agentes sistémicos para infecciones por hongos; antimicobacterianos; antivirales y vacunas. - La fabricación de productos químicos anticonceptivos de uso externo y de medicamentos anticonceptivos hormonales. - La fabricación de sustancias de diagnóstico: pruebas de diagnóstico (test de embarazo y ovulación). - La fabricación de sustancias radiactivas para realizar diagnósticos in vitro. - La fabricación de productos de biotecnología. - La fabricación de azúcares químicamente puros como glucosa, dextrosa, galactosa y glucósidos. - La fabricación de apósitos médicos impregnados, guatas medicinales, vendajes para fracturas y otros productos para suturas. - Los productos botánicos pulverizados, graduados, molidos o preparados; incluye los productos homeopáticos sólidos, líquidos o glóbulos, para uso farmacéutico. - Los derivados del opio, como la morfina, la cocaína y sus derivados para uso terapéutico. - Los demás alcaloides vegetales y glucósidos extraídos de plantas o semillas, como la quinina y la atropina, para uso terapéutico. - Las sulfas, sulfamidas y derivados, utilizados generalmente como antibióticos. - La fabricación de soluciones de uso hospitalario: soluciones intravenosas, soluciones de irrigación y la producción de agua esterilizada para ampolletas. - La elaboración de productos endocrinos y fabricación de extractos endocrinos, etc. | ||
| 4773 | Comercio al por menor de productos farmacéuticos y medicinales, cosméticos y artículos de tocador en establecimientos especializados | Esta clase incluye: - El comercio al por menor de productos farmacéuticos, medicinales, botánicos, homeopáticos, ortopédicos, ortésicos y protésicos, y artículos de perfumería y cosméticos. - El comercio al por menor de productos farmacéuticos veterinarios. - Las actividades de las tiendas naturistas. |
Fuente: Cámara de Comercio de Bogotá, httDs://linea.ccb.ora.co/descripcionciiu/. fecha de consulta 23/05/2025
5.3.2. Porcentaje del Producto Interno Bruto (PIB) asociado con el sector salud
Durante el 2022 y 2023, el sector salud ha mantenido una participación relevante y sostenida dentro del Producto Interno Bruto (PIB) colombiano. Según cifras del Banco de la República, el gasto público en salud representó el 5,1% del PIB en 2022[40]. Para el año 2023, se estimó que la participación del sector en el PIB se ha mantenido en niveles similares, con proyecciones que lo ubican alrededor del 5,0% a 5,2% del PIB[41]. Además, las proyecciones señalan que, debido a factores como el envejecimiento de la población, la convergencia del gasto per cápita entre los regímenes contributivo y subsidiado, y el incremento sostenido en los costos de tecnologías en salud, el gasto en salud podría aumentar entre 1,5 y 2 puntos del PIB durante los próximos ocho años[42].
De acuerdo con la información enviada por las Intervinientes, la forma en la que se analizó el porcentaje del PIB asociado con el sector salud lo dividieron en dos. Por un lado, el porcentaje del gasto en salud en general. Por otro lado, la participación del gasto respecto de los medicamentos. Es de señalar que la forma en la que las Intervinientes calcularon la participación de la producción de medicamentos en el PIB lo hicieron a través de mecanismos indirectos. Además, para el cálculo del gasto en salud, las Intervinientes tuvieron en cuenta "el monto de gasto del Gobierno (G) en la financiación del Sistema General de Seguridad Social a través de la Unidad de Pago por Capitación -UPC-, el gasto en salud pública y el consumo de los hogares, el cual se encuentra publicado por el DANE”[43]. El resultado del análisis de la participación antes descrita es el siguiente:
Tabla No. 5. Gasto en Salud en relación con el PIB (miles de millones de pesos)
| Indicadores | 2022 | 2023 | 2024 | 2025[44] |
| % Crecimiento | 7,30% | 0,70% | 1,70% | 2,50% |
| PIB | 1.471.079 | 1.584.562 | 1.611.500 | 1.651.787 |
| UPC | 37.682 | 47.685 | 60.678 | 63.945 |
| SGP - Salud Pública | 1.163 | 1.287 | 1.644 | 1.911 |
| SGP - Subsidio a la Oferta | 349 | 386 | 493 | 573 |
| Gasto Salud Gobierno | 39.194 | 49.359 | 62.816 | 66.429 |
| Gasto Salud Hogares | 83.839 | 95.817 | 97.446 | 99.882 |
| Total, Gasto Salud | 123.033 | 157.097 | 175.431 | 182.297 |
| Porcentaje PIB | 8,36% | 9,91% | 10,89% | 11,04% |
Fuente: Elaborado por las Intervinientes de acuerdo con los datos del DANE, DNP y Ministerio de Salud.[45]
Para el análisis de la participación del mercado de medicamentos es necesario tener en cuenta dos factores. El primero es la balanza comercial deficitaria debido a que en Colombia la importación de medicamentos es el 92% aproximadamente y la producción nacional es del 8%, aproximadamente. El segundo factor es que la distribución de medicamentos se realiza a través de dos canales: el comercial y el institucional. En el canal institucional se consumió el 64% de la producción y el valor restante en el canal comercial. De acuerdo con esto, la relación entre el gasto en medicamentes y el PIB es la siguiente:
Tabla No. 6. Gasto en medicamentos en relación con el PIB (miles de millones de pesos)
| Indicadores | 2022 | 2023 | 2024 | 202546 1 |
| % Crecimiento | 7,30% | 0,70% | 1,70% | 2,50% |
| PIB | 1.471.079 | 1.584.562 | 1.611.500 | 1.651.787 |
| Canal Institucional | 14.100 | 17.000 | 17.676 | 18.983 |
| Canal Comercial | 8.500 | 8.400 | 9.943 | 10.222 |
| Total | 22.600 | 25.400 | 27.620 | 29.206 |
| %PIB | 1,54% | 1,60% | 1,71% | 1,77% |
Fuente: Elaborado por las Intervinientes de acuerdo con los datos de la ANDI y datos propios.[47]
5.3.3. Número de empleos generados por el sector
El sector salud constituye una fuente relevante de generación de empleo en Colombia. En 2021, se encontraban registradas 885.341 personas trabajando en el sector salud. De ese total, 435.132 correspondían a profesionales. La composición ocupacional del sector también se distingue por su formalización contractual: el 58% de los trabajadores contaba con un contrato a término, el 97,1 % disponía de un contrato escrito, el 98,8 % estaba afiliado a una EPS y el 89% cotizaba al sistema pensional[48].
Desde una perspectiva ocupacional, los profesionales en medicina general representaban el grupo más numeroso, con 123.561 personas; seguidos por los de enfermería (77.190), psicología (76.835) y odontología (43.788). En el ámbito técnico y operativo, los auxiliares de enfermería constituían el mayor grupo dentro del talento humano no profesional, con 332.276 personas, lo que equivale al 37,5% del total registrado en el sector[49].
Por su parte, las Intervinientes señalaron que, conforme con la información estadística publicada por el DANE, para el 2020, el sector salud en Colombia generó aproximadamente 1.001.647 empleos directos, cifra que corresponde al 4,49 % del total de la población ocupada del país. Dentro de esta participación, las actividades que registraron el mayor volumen de empleo fueron las relacionadas con hospitales y clínicas con internación, que concentraron 316.071 empleos. De igual forma, las actividades de práctica médica y odontológica sin internación aportaron 256.383 empleos. Asimismo, las actividades de atención relacionadas con la salud humana, distintas de la hospitalaria, representaron 100.096 empleos[50].
En el segmento de fabricación de productos farmacéuticos, sustancias químicas medicinales y productos botánicos de uso farmacéutico, las Intervinientes señalaron que este segmento generó 42.486 empleos, lo que representó el 0,19 % de la ocupación nacional para el 2022. A su vez, las actividades de asistencia social sin alojamiento, particularmente aquellas enfocadas en personas mayores y discapacitadas, sumaron aproximadamente 227.280 empleos, lo que representa el 1,02 % de la población ocupada para el mismo año[51].
Las cifras antes descritas hacen referencia únicamente a empleos directos relacionados con actividades principales del sector salud. No obstante, las Intervinientes advirtieron que esta medición no incluye otros empleos indirectos estrechamente vinculados con la operación del sector[52].
5.3.4. Interdependencia con otros sectores económicos
El sector salud mantiene una alta interdependencia con múltiples sectores económicos, lo cual refuerza su carácter estratégico dentro del aparato productivo nacional. Su operación cotidiana depende, en primer lugar, del suministro constante de bienes provenientes de la industria farmacéutica y del sector de dispositivos médicos, cuyo abastecimiento resulta esencial para garantizar la continuidad y calidad de los servicios asistenciales.
A su vez, requiere de la infraestructura educativa para la formación, cualificación y actualización del talento humano en salud, y del sector tecnológico para el desarrollo e implementación de soluciones digitales que optimicen los procesos clínicos, administrativos y de atención remota. También se apoya en el sector de infraestructura para la construcción, adecuación y mantenimiento de clínicas, hospitales y centros de atención. Por otra parte, establece vínculos operativos con los sectores logístico y de transporte, indispensables para la distribución eficiente de insumos médicos y la movilidad oportuna de pacientes y personal sanitario.
Así mismo, se articula con el sector financiero, especialmente en lo relativo al aseguramiento en salud y a los flujos de financiación, tanto pública como privada, que sostienen el modelo de atención. Esta compleja red de interacciones sectoriales refleja que el sector salud en Colombia ostenta una interdependencia importante de la economía nacional, lo cual justifica su clasificación como un sector básico dentro de la estructura económica del país.
Sobre el particular, las Intervinientes señalaron que el acuerdo propuesto tiene efectos en sectores estratégicos del país. Sobre el sector logístico, destacaron la ampliación de la cobertura territorial y la eficiencia en la entrega de tecnologías en salud, especialmente en zonas rurales. En el sector financiero, resaltaron la contribución a la sostenibilidad operativa y a la formalización de relaciones contractuales, así como el incentivo a la participación de instituciones bancarias y aseguradoras en esquemas de prepago y riesgo compartido. Para el sector educativo y científico, identificaron una demanda creciente de capital humano especializado en farmacoeconomía, biotecnología e innovación clínica.
Respecto al sector tecnológico, subrayaron la importancia de la digitalización, la trazabilidad de medicamentos y la interoperabilidad de plataformas de información en salud. En el ámbito regulatorio y fiscal, enfatizaron el fortalecimiento de la gobernanza institucional, la transparencia en la contratación y la confianza pública. En relación con el comercio exterior e industrial, destacaron el potencial de reducir la dependencia de insumos importados y de fomentar la producción nacional de biosimilares y medicamentos genéricos. Finalmente, respecto al sector asegurador, precisaron que el acuerdo permitirá optimizar la gestión del riesgo, garantizar la continuidad de los tratamientos y controlar los eventos de alto costo.[53]
En conclusión, la alta interdependencia funcional y estratégica del sector salud con múltiples sectores económicos confirma su carácter de sector básico dentro de la estructura productiva nacional. Esta interacción sostiene la operación cotidiana del sistema de salud y potencia efectos transversales sobre la logística, la educación, la tecnología, la infraestructura, las finanzas y el comercio exterior, aspectos que refuerzan la necesidad de proteger su estabilidad en atención a su relevancia económica y social.
SEXTO: El acuerdo objeto de análisis surge por algunas situaciones críticas que se vienen presentando en el SGSSS, como lo identificaron las Intervinientes, el Ministerio de Salud y la SNS en los escritos radicados ante esta entidad. Con el fin de analizar el contexto en el que se da el acuerdo y su alcance, en este acápite la Superintendencia analizará cuatro elementos. Primero, el problema concreto que se pretende subsanar con el acuerdo. Segundo, el modelo que se quiere implementar con este acuerdo. Tercero, el alcance del acuerdo propuesto por las Intervinientes. Finalmente, se definirá la duración del acuerdo.
6.1. Problemas en el SGSSS identificados por las Intervinientes y la SNS
De acuerdo con las Intervinientes, una de las razones por las que el SGSSS está presentando algunos inconvenientes es el incumplimiento en la entrega de las Tecnologías en Salud (en adelante, TES) -como lo es el caso de los medicamentos, dispositivos médicos y alimentos de propósitos medico especial (APME)- a los pacientes. Esta crisis se ve reflejada en el número de peticiones, quejas, reclamos y sugerencias (en adelante, PQRS) presentadas ante la SNS en las que el objeto principal era las dificultades para recibir medicamentos esenciales y/o dispositivos médicos. Así, la crisis se viene intensificando si se tiene en cuenta que la tendencia en el número de quejas va en aumento, como se muestra a continuación:
Tabla No. 4. Número de PQRS presentadas en el 2023 y 2024 contra las EPS
| Num. | Vigilado | 2023 | 2024 | Total General | % Participación |
| 1 | NUEVA EPS | 40.323 | 80.489 | 120.812 | 22.09% |
| 2 | SANITAS | 25.810 | 42.675 | 68.485 | 12,52% |
| 3 | SALUD TOTAL | 18.088 | 49.464 | 67.552 | 12,35% |
| 4 | EPS SURA | 21.596 | 25.748 | 47.344 | 8,66% |
| 5 | COOSALUD | 16.130 | 18.889 | 35.019 | 6,40% |
| 6 | COMPENSAR | 7.717 | 17.568 | 25.285 | 4,62% |
| 7 | FAMISANAR | 3.112 | 12.926 | 16.038 | 4,03% |
| 8 | SAVIA SALUD EPS | 8.879 | 11.928 | 20.807 | 3,80% |
| 9 | ASMET SALUD | 12.659 | 7.859 | 20.518 | 3,75% |
| 10 | MAGISTERIO | 7.309 | 11.988 | 19.297 | 3,53% |
| Total TOP 10 vigilados | 167.624 | 279.534 | 447.158 | 81,76% | |
| Total general | 209.606 | 337.277 | 546.883 | 100,00% | |
Fuente: Base de datos reclamos en salud SNS años 2023-2024 (Fecha de descarga 5 de febrero de 2025)[54]
De acuerdo con la SNS, en el primer trimestre del 2025 se han presentado 141.294 casos en los que los pacientes presentaron PQRS por incumplimiento en el tiempo de entrega de medicamentos o incumplimiento total de entregas. Para la SNS si esta tendencia se mantiene durante este año, podría superar el número de reclamos que se presentaron en años anteriores[55]. Esta situación también fue descrita por las Intervinientes quienes analizaron el número de quejas presentadas por cada 10.000 afiliados entre abril de 2024 y marzo de 2025. Las quejas que se han presentado y que se muestran a continuación se centran en situaciones específicas de "no entrega, entrega parcial o demoras en el suministro de medicamentos formulados”:
ESPACIO EN BLANCO
Gráfica No. 1. Tasa de quejas relacionadas con las Intervinientes entre abril de 2024 y marzo de 2025 por no entrega o entrega parcial de medicamentos
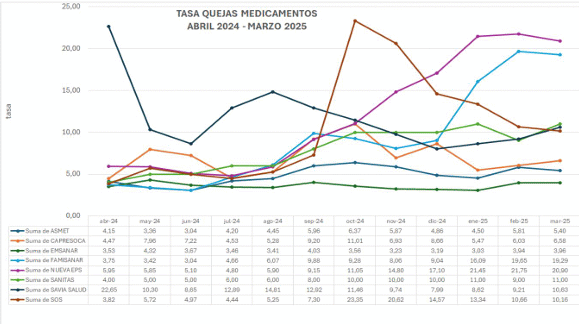
Fuente. Información entregada por las Intervinientes[56].
Igualmente, la SNS, en el concepto técnico de viabilidad que emitió sobre el acuerdo propuesto por las Intervinientes, manifestó que la falta de cumplimiento en la entrega de los medicamentos no tenía una salida pronta y tampoco una causa determinante de esta situación, entre las probables causas está el desabastecimiento y la demora en los tiempos de entrega derivada de la intermediación que existe actualmente en la adquisición de medicamentos[57]. Por lo anterior, es necesario tomar medidas encaminadas a mitigar o, incluso, solucionar el problema que se viene presentando con la entrega de medicamentos en el país.
El Ministerio de Salud, en su concepto técnico de viabilidad del acuerdo objeto de análisis, también identificó los mismos problemas previamente descritos y, además, manifestó que era necesaria la implementación de acciones estructurales y coordinadas para reducir o incluso eliminar cualquier tipo de incumplimiento en el suministro de TES. Una medida como la establecida en el Acuerdo estaría alineada con el Plan Nacional de Desarrollo "Colombia Potencia Mundial de la Vida” (en adelante, PND). En el PND se estableció que, entre otros, se debía promover la formulación de políticas y estrategias que mejoren el acceso y distribución de medicamentos. Además, contempla la necesidad de identificar los medicamentos usados para enfermedades de alto costo o huérfanas con el fin de garantizar la disponibilidad de estos y el acceso oportuno[58].
Debido a esto, y de acuerdo con los elementos del acuerdo propuesto por las Intervinientes los cuales se expondrán en esta Resolución, el Ministerio de Salud[59] y la SNS[60] emitieron concepto favorable. Para el Ministerio de Salud la implementación de un acuerdo como este "es una medida urgente, técnica, legal y económicamente viable [que] permitiría resolver barreras críticas de acceso, aumentar la equidad territorial, reducir el gasto público y garantizar el goce efectivo del derecho fundamental a la salud”[61].
6.2. Modelo de negociación conjunta de Tecnologías en Salud que se quiere implementar con el acuerdo objeto de análisis
Como ya se ha mencionado previamente, el acuerdo tiene por objeto permitir que las Intervinientes, que en este caso son las EPS intervenidas por la SNS, puedan negociar de manera conjunta y directa la compra de los medicamentos con los laboratorios productores e importadores. Con este modelo se busca que haya más poder de negociación desde el lado de la demanda y, además, que se reduzca la intermediación lo que podría hacer más eficiente la entrega de los medicamentos. Para comprender cuál es la forma en la que se configuraría el acuerdo, en este acápite se presentará cómo funciona el modelo de negociación y compra de medicamentos actualmente. Luego, se explicará el antecedente directo que se tiene en Colombia sobre la compra de medicamentos de manera directa. Finalmente, se expondrán las dos formas de negociación que proponen las intervinientes.
De acuerdo con lo expuesto por la SNS en el concepto de viabilidad que emitió para este trámite, actualmente la negociación y compra de medicamentos en el SGSSS funciona en tres partes, en términos generales[62]. Primero, las EPS contratan con la Gestores Farmacéuticos para que adquieran y dispensen las TES o las envíen a las Instituciones Prestadoras de Salud (en adelante, IPS) para que sean administradas a los pacientes. En la segunda etapa, los Gestores Farmacéuticos realizan las negociaciones con los laboratorios y, posteriormente, hacen la distribución de las TES. En la tercera etapa, los Gestores Farmacéuticos reciben las TES y las distribuyen, ya sea en los puntos de dispensación o a través de las IPS.
Uno de los principales problemas identificados por la SNS[63] respecto de este modelo de negociación se da en los casos en que los Gestores Farmacéuticos no cumplen con los pagos a los laboratorios. En estos casos los laboratorios pueden bloquear o hacer despachos parciales a los Gestores Farmacéuticos hasta que se realizaran los pagos de la cartera antigua. Esta situación generaba que las entregas parciales afectaran a los usuarios de las EPS que tuvieran que acudir a con el Gestor Farmacéutico sin importar a qué EPS estuvieran vinculados. Esto debido a que el laboratorio no distingue la EPS destinataria de los TES, puesto que las TES no las compra directamente cada EPS sino un intermediario, en este caso el Gestor Farmacéutico.
Es de resaltar que esta situación también fue identificada por las Intervinientes en la información suministrada. Lo que señalaron fue que en los últimos tres años ha habido una tendencia a la baja en la entrega completa de las TES. Algunas causas de esta situación identificadas por las Intervinientes son, por ejemplo,
"un cálculo insuficiente para hacer abastecimiento y distribución en algunas moléculas, lo que tiene como consecuencia la generación de pendiente, pero adicionalmente hay factores asociados a la industria
farmacéutica como los bloqueos en los despachos de medicamentos de manera total o parcial por razones financieras que imposibilitan la entrega de las órdenes de compra generadas por los gestores farmacéuticos y bajos niveles de servicio y desabastecimientos que se traduce en producción insuficiente de algunas moléculas para la demanda que tiene el país actualmente".[64]
El modelo de negociación de medicamentos que se quiere implementar por parte de las Intervinientes tiene el objetivo modificar la negociación a través de intermediarios y poder realizar una negociación directa entre EPS y laboratorios. De acuerdo con lo manifestado por la SNS[65] y por las Intervinientes, este tipo de negociación no es novedosa, por el contrario, se realiza esta negociación para algunos tipos de medicamentos.
En términos generales existen dos tipos de TES, los dispensables y los administrables. En el primer caso, las TES son entregadas al paciente en su domicilio o en establecimientos farmacéuticos. En el caso de los administrables se requiere que el paciente vaya a una IPS para que se le administre el medicamento. En el caso de las TES administrables las EPS contratan directamente con los laboratorios. Ahora bien, el contrato que se celebra con las IPS que aplican las TES puede estar en cabeza de los laboratorios o de las EPS[66]. Este es el tipo de modelo que quiere ser implementado por parte de las Intervinientes para los demás medicamentos, sin importar si son administrables o dispensables.
Las Intervinientes mencionaron en la información enviada a esta Superintendencia que la negociación la realizarían de manera abierta o cerrada[67]. En caso de las negociaciones abiertas las Intervinientes plantean que se realice a través de procesos abiertos en los que los proveedores interesados presenten ofertas de acuerdo con las condiciones previamente establecidas por las EPS participantes. Por otro lado, las negociaciones cerradas están previstas como un escenario complementario en los casos en que, por la naturaleza o necesidad del medicamento, no sea viable realizar un proceso abierto[68].
6.3. Alcance del acuerdo de negociación conjunta de Tecnologías en Salud
Como se ha expuesto a lo largo de este acto administrativo, el objetivo del acuerdo es realizar una negociación conjunta por parte de las EPS intervenidas para la compra de medicamentos directamente a los laboratorios. Este acuerdo, como se mencionó en el numeral 6.2., implica un cambio en el modelo de negociación tradicional el cual requería un intermediario, en este caso, los Gestores Farmacéuticos. Para analizar el alcance del acuerdo propuesto por las Intervinientes, en este acápite se describirá las condiciones preliminares del acuerdo, conforme con lo informado por las Intervinientes, y el rol de los agentes que participarían en las transacciones.
El principal objetivo del acuerdo que las Intervinientes pretenden llevar a cabo es la negociación conjunta de las TES[69]. Esta negociación conjunta tiene la finalidad esencial de atender la demanda de los afiliados con la capacidad de respuesta necesaria. Las Intervinientes consideran que, con la negociación conjunta de medicamentos, se logaría mejores condiciones de precios, oportunidad y calidad de los medicamentos. De acuerdo con lo expuesto por las Intervinientes, a través de este acuerdo solo se realizará una negociación conjunta de las condiciones de adquisición de los medicamentos, sin embargo, no hay una compra conjunta, como se expone a continuación:
"Técnicamente no hay una compra conjunta, esto es, no se tendrá un fondo de recursos comunes destinados para el pago de medicamentos; ni tampoco una única negociación, cada EPS se encargará de negociar y establecer sus propias condiciones de precios y entrega; el volumen de medicamentos a comprar lo define cada EPS.
El negocio jurídico lo establece cada EPS dentro del marco de su propio manual de contratación, respetando las políticas de SARLAFT/SICOF establecido y bajo la concertación propia de entrega, y demás procedimientos internos aplicables a cada EPS, de manera independiente.”[70]
A pesar de que cada EPS se hará responsable de la negociación particular de acuerdo con sus necesidades, lo cierto es que, al momento de realizar la negociación -ya sea de manera abierta o cerrada como se expuso en el numeral
4.2. anterior-, las Intervinientes realizarán unos estudios técnicos conjuntos que tendrán un análisis integral con, al menos, tres componentes:
[INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL]
Con estos estudios se pretende poder determinar elementos relevantes para la negociación como lo es el volumen de TES requeridos, los medicamentos necesarios de acuerdo con las patologías que se atienden y la forma en la que se realizará la distribución. En ese sentido, las Intervinientes tendrán en cuenta la siguiente información al momento de realizar la negociación con el fin de determinar cantidades reales de acuerdo con las necesidades de salud de los afiliados y, así, evitar sobrecostos por exceso o riesgo de desabastecimiento por subestimación:
[INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL]
[INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL]
Es de resaltar que, a pesar de que cada EPS mantendrá la autonomía para la compra de los medicamentos, entre otros motivos porque el número de pacientes atendidos, las patologías y la ubicación de estos es diferente de acuerdo con cada EPS, lo cierto es que las Intervinientes pretenden establecer algunas condiciones comunes entre ellas. Entre esas condiciones están: "precios techo, cláusulas mínimas contractuales, modelos de riesgo compartido y auditoría”[73].
Aunque pareciera que este acuerdo tiene implicaciones directas solo en las EPS, específicamente las intervenidas por la SNS, lo cierto es que este acuerdo tiene implicaciones en varios agentes del mercado que son eslabones en la cadena de valor de la prestación del servicio de salud en Colombia. En ese sentido, es necesario identificar cada uno de estos agentes y establecer el rol que tendrían en el caso de llevarse a cabo el acuerdo objeto de análisis. De acuerdo con la información suministrada por las Intervinientes, la SNS y el Ministerio de Salud, los agentes que se verían de alguna forma implicados con esta operación son: las EPS, los agentes del sector farmacéutico que en este caso serían los laboratorios, los Gestores Farmacéuticos, los operadores logísticos -que, con este acuerdo, serían nuevos agentes en el mercado-, las IPS y las Empresas Sociales del Estado (en adelante, ESE).
- Participación de las EPS intervenidas y de las demás EPS en el acuerdo
Las principales implicadas en este acuerdo son las nueve (9) EPS intervenidas. Estas EPS asumirán el rol de negociar de manera directa las TES con los laboratorios. El objetivo, como se ha venido mencionando a lo largo de esta resolución es lograr mejores precios, mayor cobertura, eficiencia en la distribución y mejor calidad. Las EPS intervenidas consideran que negociar de manera conjunta les da mayor poder de negociación que si lo hicieran de manera individual. De acuerdo con la información suministrada por las Intervinientes, las nueve (9) EPS intervenidas reúnen a más de veintinueve millones cuatrocientos mil (29'400.000) afiliados, lo que representa el 57.6% del total nacional[74]. Sin embargo, en el mercado propiamente de compra de TES, las intervinientes tienen el 20% en las compras institucionales[75].
La diferencia entre la participación de las Intervinientes en el mercado medido desde el punto de vista del número de afiliados y el de la participación de estas en el mercado de compra de TES se explica por varios motivos. El primero es que no toda la población afiliada demanda las mismas TES, eso depende de las patologías que se estén tratando. Adicionalmente, algunas de las EPS intervenidas tienen varios afiliados en zonas rurales, con menor prestación de servicios de salud y menor consumo histórico de TES. De acuerdo con esto, con el acuerdo también se podrá conciliar las cifras entre el número de pacientes y la posibilidad de suministrar las TES necesarias para el tratamiento de las diferentes patologías que tenga que tratar cada EPS[76].
De acuerdo con lo manifestado por las Intervinientes, con este acuerdo no se pretende "controlar el mercado ni excluir a otros actores, sino mejorar las condiciones de acceso para un grupo históricamente vulnerable y en situación de intervención estatal”[77]. Por el contrario, con este acuerdo se busca tener mayor poder de negociación para poder adquirir las TES en la mejor relación precio/calidad. Debido a esto, en caso de que una o varias EPS no intervenidas quieran hacerse parte de este acuerdo y beneficiarse de las eficiencias que se quieran adquirir, lo puedan hacer[78]. Igualmente, las Intervinientes manifestaron que en caso de que una EPS no intervenida quisiera hacerse parte del acuerdo, debería cumplir con las siguientes condiciones:
- "La EPS no debe tener medida de intervención para liquidar.
- Suscribir los acuerdos de confidencialidad a que haya lugar con cada uno de los laboratorios
- No establecer propuestas o acuerdos de niveles de servicios con los cuales se busque hacer mercadeo entre la población para lograr traslados a su EPS.
- Participar en las reuniones fijados por los aliados.
- Abstener de convenir prácticas con el potencial vendedor que configuren competencia desleal o restricción de mercado.
- Suscribir actos jurídicos enmarcados en el artículo 9 de la Ley 1430 de 2009 o aquella que la modifique, adicione o sustituya.”[79]
Para esta Superintendencia es importante que las EPS no intervenidas puedan hacer parte de un acuerdo que pretende resolver algunos de los problemas más importantes que tiene el SGSSS. También es claro que para que una EPS pueda entrar en el acuerdo objeto de análisis debe cumplir con las condiciones necesarias para que el acuerdo pueda ser llevado a cabo. En todo caso, las condiciones que las Intervinientes establecen para que las EPS no intervenidas puedan hacerse parte del acuerdo, a primera vista, parecen razonables. Sin embargo, estos requisitos deberían ser cumplidos por todas las EPS que quieran participar en el acuerdo, lo que incluye al EPS intervenidas y en ningún caso se podrá exigir condiciones diferentes o discriminatorias entre las EPS interesadas en hacerse parte del acuerdo objeto de análisis.
- Participación de la industria farmacéutica, en este caso, laboratorios productores o importadores de TES
Como se describió en el numeral 4.2. de esta Resolución, el principal cambio que tendría la forma en la que se negocian las TES es que ahora las EPS negociarán directamente con los laboratorios -ya sean productores o importadores-. Además de la negociación directa, hay un cambio sustancial en la forma en la que los laboratorios vienen ofreciendo las TES y es que se buscará que los laboratorios vendan directamente a las EPS y asuman el costo de dispensación o administración de las TES[80]. Este costo actualmente se paga al Gestor Farmacéutico. En aquellos casos en los que los laboratorios no puedan hacer la dispensación de las TES, esta se hará a través de operadores logísticos.
Las Intervinientes, con la negociación en bloque, también quieren buscar que los laboratorios ofrezcan las moléculas de acuerdo con su capacidad instalada. Esto generaría que no haya una centralización en un único proveedor, sino que se diversificaría la oferta para, de esta forma, generar mayor competencia entre los laboratorios. En ese sentido, se buscaría garantizar un suministro que cubra las necesidades de los pacientes. Igualmente, para garantizar el abastecimiento de las TES que las Intervinientes quieren adquirir y, en términos generales para cumplir con el acuerdo y mitigar los riesgos de incumplimiento, algunas de las cláusulas que se incluirían en los contratos con los laboratorios son las siguientes:
[INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL]
[INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL]
[INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL]
[INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL]
[INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL]
[INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL]
[INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL]
[INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL] [INFORMACIÓN CONFIDENCIAL].
De acuerdo con lo expuesto por las Intervinientes, el rol que tendría los laboratorios en el mercado de TES cambiaría. Lo primero es que los laboratorios entrarían a negociar directamente con las EPS, lo que implicaría que, aunque la negociación general sobre las TES es conjunta, los detalles de las necesidades de cada EPS serían contratadas de manera individual. Lo mismo pasaría con el pago de las TES adquiridas por las EPS, debido a que cada una se haría responsable del pago. Además, los laboratorios también entrarían a tener la función de distribución de los medicamentos, lo que implica un cambio sustancial en la forma en la que operaban los laboratorios en el mercado colombiano.
- Participación de los Gestores Farmacéuticos en el nuevo modelo de negociación conjunta de TES
Como se expuso en el numeral 6.2., con el acuerdo propuesto por las Intervinientes se busca que se elimine un eslabón en la cadena de compra de TES que específicamente es el de la intermediación para la compra y distribución de los TES. En este caso, los Gestores Farmacéuticos ya no realizarían esa intermediación, sin embargo, esto no implica que vayan a salir del mercado. De acuerdo con lo manifestado por las Intervinientes, el rol de los Gestores se podría centrar con el cumplimiento de funciones técnicas, operativas y logísticas. Estas funciones las identificó así la SNS y las Intervinientes:
- "Dispensación ambulatoria, puesto que son indispensables para entregar los medicamentos con la respectiva información farmacéutica a los afiliados. La diferencia está en que no serán contratantes directos con la industria farmacéutica y que su cobro al SGSSS será de una porción mucho menor, correspondiente a la simple entrega del medicamento a los afiliados.
- Apoyo en trazabilidad, control y seguimiento de consumo.
- Validación de prescripciones y gestión farmacoterapéutica, mediante procesos de farmacovigilancia y tecnovigilancia.
- Reporte sistemático de indicadores de oportunidad en entregas y fallas de acceso.
- Agentes que estarían involucrados en la operación objeto de análisis.”[82]
Es importante resaltar que la EPS que no se hagan parte del acuerdo objeto de análisis continuarán adquiriendo las TES a través de los Gestores Farmacéuticos, como se ha realizado en el modelo tradicional.
- Participación de los Operadores logísticos en el nuevo modelo de negociación de las TES
Con el acuerdo objeto de análisis la distribución de las TES, en principio, se realizará a través de los laboratorios. Sin embargo, en los casos en que los laboratorios no puedan realizar la distribución, esta se hará a través de Operadores Logísticos. Estos operadores se harían cargo del transporte, almacenamiento y distribución de los TES[83]. El operador logístico se diferencia del Gestor Farmacéutico no ofrecería seguimiento al tratamiento farmacoterapéutico, gestión de autorizaciones y atención al usuario. Esta situación genera que la responsabilidad del tratamiento y seguimiento estará a cargo del médico y las EPS[84].
Es de resaltar que las Intervinientes sí han previsto las zonas en las que sería necesario contratar con Operadores logísticos. Las zonas identificadas son las rurales, dispersas y de difícil acceso "como Vaupés, Guainía, Chocó, Guajira, sur del Meta y regiones del Pacífico nariñense”. En estas zonas las Intervinientes y la SNS identificaron que podría haber limitaciones de acceso debido a temas de infraestructura y ausencia de canales de distribución directa, por lo que es necesario contar con operadores especializados para cumplir con la dispensación de las TES en las zonas identificadas[85].
- Participación de las IPS y las ESE en el nuevo modelo de negociación de TES
Las IPS y las ESE, en el marco del acuerdo objeto de análisis, podrán dispensar de manera ambulatoria las TES, además de los medicamentos administrables. Esto de acuerdo con lo establecido en el Decreto 780 de 2016[86]. Sin embargo,
en el concepto técnico la SNS afirmó que los laboratorios deben "priorizar la subcontratación de las Empresas Sociales del Estado para que dispensen o administren las TES en su territorio”[87]. Con esta condición lo que se busca es que se lleve "a todos los rincones del país los medicamentos a los afiliados y eliminar la barrera geográfica para su entrega oportuna”[88].
6.4. Duración del acuerdo objeto de análisis
En la solicitud de autorización, las Intervinientes establecieron que la duración del acuerdo sería de un (1) año prorrogable por otro año. En este tiempo se pretende "garantizar la oportunidad, suficiencia y continuidad de los tratamientos de los pacientes que así lo requieran”[89]. El acuerdo entraría en vigor a partir de la fecha del primer contrato celebrado por una de las EPS con uno o varios de los proveedores seleccionados[90]. Es de resaltar que la fase previa de estructuración técnica, análisis del mercado, publicación de las condiciones de contratación y negociación conjunta no hace parte del año de duración del acuerdo. Esta fase, que para efectos de esta resolución se denominará precontractual, podrá tener una duración aproximada de entre treinta (30) y sesenta (60) días[91].
Adicionalmente, las Intervinientes prevén la posibilidad de que coexistan negociaciones individuales con las negociaciones en bloque en casos como "tecnologías no incluidas en el acuerdo conjunto, situaciones de desabastecimiento o urgencia y necesidades territoriales específicas no cubierta por el proveedor seleccionado”[92]. Estas negociaciones las podrá llevar a cabo cada EPS "siempre y cuando no vulnere los principios del acuerdo conjunto y se mantenga la trazabilidad, los precios techo y las condiciones marco definidas por el grupo de EPS”. Las Intervinientes han previsto que estas negociaciones individuales se puedan realizar en un término que no exceda los sesenta (60) días calendario a partir de la identificación de la necesidad[93].
Los términos antes descritos solo podrán empezar a correr una vez esta resolución sea comunicada a las Intervinientes. En todo caso, la Superintendencia podrá dar por terminado el acuerdo objeto de análisis antes del plazo previsto en el caso de que "las condiciones de mercado que llevaron a la celebración del acuerdo [hayan] sido superadas y el sector se encuentre estable”[94].
SÉPTIMO: Que, una vez descrito el acuerdo objeto de análisis, esta Superintendencia estudiará los casos que pueden ser utilizados como precedentes sobre la autorización de acuerdos en los términos del parágrafo único de la Ley 155 de 1959. Además, la Superintendencia hará un análisis de los casos internaciones en los que se haya negociado la compra de medicamentos de manera conjunta.
7.1. Casos previamente decididos por la Superintendencia de Industria y Comercio en aplicación del parágrafo único del artículo 1 de la Ley 155 de 1959
La Superintendencia tiene dos antecedentes en los que se decidió aplicar la excepción establecida en el parágrafo único del artículo 1 de la Ley 155 de 1959. Las resoluciones por las que se decidió autorizar los acuerdos que, no obstante, al limitar la libre competencia económica tenían la finalidad de defender la estabilidad de un sector básico de la producción, son la Resolución No. 04332 del 25 de febrero de 2003 y la Resolución No. 35696 del 1 de junio de 2012. A continuación, la Superintendencia expondrá los principales elementos de estas dos decisiones.
A través de la Resolución No. 4332 del 2003 la Superintendencia aprobó el acuerdo propuesto por Manufacturas Eliot Ltda., Industrias Zafra Ltda., Sajatex Ltda., Protela S.A., el cual tenía por objeto realizar un "acuerdo de buena voluntad para la cadena de filamentos de poliéster y textil suscrito dentro del marco de convenio de competitividad exportadora para la cadena algodón- fibras-textil-confecciones”. El acuerdo se centraba en que las suscriptoras de este le comprarían a Enka de Colombia S.A., en forma separada y sin vínculos de solidaridad, "filamentos texturizados 167 decitex”. Lo que se buscaba con este acuerdo era:
- "El fortalecimiento de la producción nacional, optimizar la eficiencia en los diferentes eslabones de la cadena, así como lograr una mayor integración entre los mismo, la consolidación del mercado interno la necesidad de ampliar y consolidar la participación y la voluntad de las empresas nacionales de adquirir tal oferta.
- Facilitar a Enka de Colombia una mejor utilización de su capacidad instalada y a los empresarios textileros obtener materias primas en condiciones adecuadas de cantidad, oportunidad y precios aceptables para ambas partes”[95]
El problema que dio origen a esta solicitud de autorización de un acuerdo que podría limitar la libre competencia es una investigación de Antidumping que adelantó el Ministerio de Comercio, Industria y Turismo contra las empresas que importaban filamento texturizado con origen Malasia, Taiwán, Indonesia y Tailandia. La denuncia de este caso fue presentada por Enka Colombia S.A. como único productor de ese tipo de filamento a nivel nacional. Esta investigación concluyó a través de la Resolución No. 908 del 24 de junio de 2002 debido a la celebración del acuerdo que analizó la Superintendencia[96].
El acuerdo del que tuvo conocimiento el Ministerio de Comercio, Industria y Turismo fue radicado el 27 de mayo de 2002 por Enka de Colombia S.A. (productor nacional) y Manufacturas Eliot Ltda., Industrias Zafra Ltda., Sajatex Ltda., Protela S. A. En este documento, las empresas importadoras del filamento texturizado (empresas que representaban más del 50% de los importadores del producto objeto de análisis y similares). Estas empresas se comprometieron a comprarle a Enka de Colombia S.A. el filamento mencionado, el cual era de producción nacional. Con este acuerdo, se buscaba fortalecer la producción nacional y lograr mayor integración de los eslabones de la cadena de algodón-fibras-textil-confecciones, con lo cual se consolidaba el mercado interno. Con este acuerdo de buena voluntad, la denunciante solicitó la terminación de la investigación por Dumping[97].
Para la Superintendencia, a este tipo de acuerdo le era aplicable la excepción establecida en el parágrafo único del artículo 1 de la Ley 155 de 1959 debido a que la fibra de poliéster 167 "es un insumo básico para producción de textiles cuyos consumidores nacionales son todas aquellas empresas que se dedican a estas actividades”[98]. Además, es una de las excepciones descritas en el artículo 1 del Decreto 1302 de 1964, al ser un proceso de producción y distribución destinado a satisfacer las necesidades de "vestido”. Este acuerdo fue previsto para ser ejecutado en un (1) año prorrogable por otro y el seguimiento se haría a través de la remisión de las actas de las reuniones periódicas que realizaría el comité de seguimiento creado en el marco del acuerdo analizado99.
El segundo caso que analizó la Superintendencia fue el acuerdo que se autorizó con el fin de "defender la estabilidad de un sector de la construcción destinado a satisfacer las necesidades de vivienda de interés prioritario, suscrito por los participantes de los mercados de la producción, distribución y comercialización de cemento, hierro e insumos para redes hidráulicas de acueducto y alcantarillado”. La iniciativa de esta solicitud fue del Gobierno Nacional a través del Ministerio de Vivienda, Ciudad y Territorio y tenía el objetivo de poder ejecutar los proyectos de vivienda de Interés Social Prioritario (VIP). Con esta iniciativa se pretendía evitar que, con la ejecución de proyecto de las VIP que implicaba la construcción de cien mi (100.000) viviendas en un año, se generara una presión alcista en los precios de los insumos básicos para la construcción, como lo es, entre otros, el cemento, el hierro y los tubos[100].
En la Resolución No. 35696 del 1 de junio de 2012, la Superintendencia aprobó este acuerdo por considerar que tenía la finalidad de defender un sector básico de la economía como era el de la vivienda de la población colombiana y el servicio de acueducto. Además, el acuerdo fue aprobado por el término de un (1) año prorrogable por otro año. Es de resaltar que la Superintendencia estableció que verificaría y vigilaría las variables económicas del sector básico, por lo que solicitaría información económica, financiera y contable de las empresas integrantes de sectores de producción como el de cemento, hierro e insumos para redes hidráulicas. También requeriría información contable de las empresas que participaban en ese momento en los sectores antes mencionados. Finalmente, requirió información económica, financiera y contable de los proyectos de las VIP[101].
Los dos antecedentes descritos dan una línea de ruta clara de los elementos que deben ser analizados por la Superintendencia al momento de analizar estos casos. Igualmente, muestran los lineamientos que debe dar la Superintendencia para que, una vez autorizado el acuerdo, este se cumpla y, además, no afecte la libre competencia económica de maneras no previstas por la autoridad de competencia al momento de analizar la solicitud de autorización. Los elementos generales son cuatro (4). Primero, el objeto del acuerdo y su relación con un sector básico de la producción y las intervinientes, que para el caso objeto de análisis se describió en el considerando tercero y el numeral 5.2. del considerando quinto. Segundo, el problema que dio origen a la solicitud de autorización de un acuerdo, así como el alcance de este, tal y como se analizó en el considerando sexto de esta resolución. Tercero, la duración del acuerdo el cual fue descrito en el numeral 6.4. del considerando sexto de esta resolución. Finalmente, se debe establecer la estrategia de seguimiento del acuerdo, la cual será descrita en el considerando octavo de esta decisión.
7.2. Casos internacionales sobre negociación y compra conjunta o agregada de TES
Como se mencionó, en Colombia se ha evaluado y autorizado dos solicitudes de acuerdos que se enmarcaban en la excepción establecida en el parágrafo único del artículo 1 de la Ley 155 de 1959. Estos antecedentes han sido relevantes para este caso concreto porque han servido como fundamento para poder determinar los elementos que deben ser analizados y tenidos en cuenta por la Autoridad de Competencia al momento de analizar la excepción descrita. Sin embargo, ninguno de esos antecedentes está relacionados con el sector salud o, más específicamente, con el mercado de TES. Debido a esto, la Superintendencia estudiará casos internacionales en los que se negoció la compra conjunta de medicamentos. Esto con el fin de poder identificar la forma en la que ha operado este tipo de acuerdos y los resultados de estos en el mercado.
A continuación, se expondrán tres casos internacionales -Países Bajos, China y México- como una muestra de casos en los que se ha realizado la negociación y compra conjunta de medicamentos. En estos tres casos de análisis se expondrán cuál fue el acuerdo que se realizó, cuál es el mecanismo de compra de medicamentos y el resultado de estos procesos.
Tabla No. 5. Exposición de casos internacionales sobre compra en bloque de medicamentos
| Nombre del acuerdo | Objeto del acuerdo de compra conjunta de medicamentos | Mecanismo de compra | Resultados |
| Guía de[102] "Adquisición colectiva de medicamentos recetados para atención médica especializada (MSC)" de la Autoridad de Holanda (Países Bajos) para el Consumidor y el Mercado (ACM) (2016) | La ACM, con la expedición de la guía para la adquisición de medicamentos, buscaba conciliar la posibilidad de comprar medicamentos de manera colectiva con las reglas de competencia[103]. La idea con la expedición de esta guía era eliminar la incertidumbre y facilitar la negociación efectiva con el fin de lograr menores costos en los medicamentos. Para lograr esta finalidad, la ACM creó el concepto de "puerto seguro” (safe harbor) como una forma de asumir que en el marco de ese "puerto” la adquisición de medicamentos estaba permitida y no limitaba la libre competencia. Este concepto reunía tres elementos | En la guía la ACM identificó la forma en la que se negociaría los medicamentos de manera conjunta a través de la segmentación del mercado de acuerdo con su grado de competencia por precio: medicamentos de monopolio, de oligopolio, en competencia y de múltiples fuentes[105]. Para lograr fomentar el poder de negociación, en la Guía se definieron cinco (5) pasos para adquirir medicamentos: (i) determinar la política de medicamentos y volumen por parte de los médicos especialistas; (ii) expedición del "mandato de adquisición” en el que se establecen las reglas de negociación de los | Medicamentos de Oligopolio: La guía permitió la creación de una organización nacional de adquisición entre la Federación Holandesa a de Centros Médicos Universitarios (NFU), la Asociación Holandesa de Hospitales (NVZ) y la Federación de Aseguradoras de Salud (ZN). Los resultados de la negociación conjunta en este caso no fueron necesariamente positivos. Por un lado, en la negociación se encontró que las que se hacían de manera descentralizada tenían mejor éxito por la recepción de los fabricantes a negociar[109]. Para las organizaciones de |
| importantes: (i) armonización de una parte de los costos hospitalarios y de las aseguradoras; (ii) la admisión de agentes en la negociación conjunta de medicamentos debe decidirse sobre la base de criterios objetivos; (iii) no se debe imponer restricciones innecesarias a los participantes en cuanto al periodo de participación, las obligaciones de compra y la terminación de su participación[104]. En esta compra colectiva de medicamentos, los principales agentes que podían participar son las organizaciones de atención médica (como hospitales) y las aseguradoras en salud. Estos agentes podían actuar de forma individual o a través de estructuras colaborativas. | medicamentos; (iii) negociación con fabricante; (iv) implementación de la política de compra de medicamentos; (v) monitoreo de la política prescripción y compra de medicamentos. [106] De acuerdo con cada segmento, se han implementado estrategias de negociación, así[107]: 1. Para los medicamentos de oligopolio, la guía facilitó la creación de una nueva organización nacional de adquisición entre la Federación Holandesa de Centros Médicos Universitarios (NFU), la Asociación Holandesa de Hospitales (NVZ) y la Federación de Aseguradoras de Salud (ZN)[108]. 2. Para los medicamentos de monopolio la guía contribuyó a reducir los costos y posiblemente a una cierta reducción de los precios, ya que las aseguradoras sanitarias adoptaron una posición colectiva en la adquisición de estos medicamentos. 3. Para los medicamentos que estaban en el segmento de "competencia” la guía no tuvo un impacto real porque la compra conjunta de medicamentos había sido implementada décadas atrás. | compra de medicamentos ya existente como el caso de las organizaciones que compraban medicamentos para el tratamiento de la hemofilia la guía dio mayor claridad sobre el alcance de las negociaciones conjuntas[110]. Medicamentos de Monopolio: La organización ZN negoció precios para varios medicamentos de monopolio. En algunos medicamentos lograron descuentos relevantes mientras que en otros no se pudo establecer una diferencia significativa.[111] | |
| "Adquisición centralizada de medicamentos basada en volumen”[112] República Popular de China (2018) | La Administración Nacional de Seguridad Sanitaria de China[113] promovió la política de "adquisición centralizada de medicamentos basada en volumen”. Con esta política se implementó la compra centralizada a través del departamento de salud como un comprador estratégico. El objetivo es poder negociar un volumen grande de medicamentos con el fin de lograr mejores precios. Con esto | La forma de compra de medicamentos es través de procesos de licitación, por lo que son las empresas farmacéuticas las que deben participar en la licitación. Las empresas que participan y gana en el proceso adquieren una participación relevante en el mercado debido a que son incluidas en la centralización de adquisiciones. Además, las empresas tienen una participación continua y | Algunos de los resultados de la implementación de la política analizada son los siguientes: Reducción precios: con las licitaciones se evidenció una reducción del precio en los medicamentos de hasta el 53%, de acuerdo con los datos analizados.116 Ahorro de Costos: La política ha generado ahorros |
| se buscaba controlar el alza de los gastos médicos y reducir la carga económica de los pacientes. También busca reducir los precios, aumentar la cantidad y optimizar la calidad en el suministro de medicamentos a largo plazo.[114] | estable en el mercado chino. Estas empresas deben ofrecer un mejor precio en el mercado a cambio del volumen de medicamentos que es adquirido. La implementación de la compra es gradual, por rondas o lotes de adquisición, las cuales se expanden de acuerdo con los medicamentos incluidos[115]. | acumulados de más de 260 mil millones de yuanes en los primeros seis lotes. [117] Reorganización de la industria y competencia: de acuerdo con el estudio realizado sobre la implementación de la política, en las licitaciones públicas hubo un aumento en la competencia, pero a la vez se generó la eliminación de algunas empresas que no tenían la capacidad de competir en las condiciones establecidas, lo que también ocasionó una mayor concentración del mercado.[118] El aumento del volumen de compra de medicamentos no compensa la pérdida de beneficios: las empresas farmacéuticas obtuvieron una mayor cuota del mercado y mayores ventas en términos de volumen, este aumento no compensa totalmente la pérdida de beneficios causa por el bajo precio en el que se negocian los medicamentos. Esto ocasiona que las farmacéuticas tengan un menor margen de utilidades lo que genera que, a futuro, el volumen de producción no necesariamente aumente. [119] Impacto en la innovación: con esta política se busca, también, que haya mayor innovación. Sin embargo, en la práctica persisten problemas de capacidad y no hay motivación suficiente para la innovación por parte de las farmacéuticas.[120] | |
| "Sistema de compra consolidada del sector salud” Gobierno de México (2021 - 2026) | En México se creó una plataforma para la compra consolidada de medicamentos y dispositivos médicos. Con esto se busca asegurar las mejores condiciones de calidad, efectividad y precio. A través de la plataforma se busca | La forma en la que se realiza la contratación de los medicamentos es a través de la plataforma la cual solicita, primero, que haya una planeación estratégica en la que se identifiquen las necesidades a contratar. | En este tipo de compras, el Gobierno de México ha evidenciado eficiencia en volumen de entrega y tiempos de entrega, así como alcance en el suministro de medicamentos.[123] Sin |
| identificar las necesidades del sector salud y se generan procesos de contratación pública con los que se supliría las necesidades en medicamentos de manera transparente. En estos procesos pueden participar empresas nacionales y extranjeras.[121] | Segundo, se realiza un proceso de contratación ágil a través de procesos digitales de compras consolidadas. Tercero, se crearon sistemas con el fin de lograr la apertura y transparencia de los contratos que se realicen sobre medicamentos.[122] | embargo, a diferencia de los dos casos analizados antes, este sistema en particular permite que haya más transparencia en las comprar públicas, con lo cual es posible hacer un seguimiento detallado de lo que el Gobierno está adquiriendo en temas de salud. Para esto, cuentan con una plataforma de monitore de medicamentos e insumos de salud la cual tiene el objetivo de "transparentar y monitorear el proceso, estado y fase de adjudicación de medicamentos e insumos médicos incluidos en la compra consolidada 2025- 2026[124]. | |
Fuente: Elaborado por la Superintendencia de Industria y Comercio.
Del análisis de los tres ejemplos antes descritos, es importante tener en cuenta que uno de los temas más relevantes es el de competencia y transparencia de la información. Aunque es claro que todas las políticas de compra conjunta (sean de iniciativa pública o privada) tienen el objetivo de superar las dificultades en cuanto al volumen de medicamentos necesario, así como el precio de adquisición, no necesariamente se obtienen los resultados esperados en el corto plazo, pero sí puede ser un mecanismo que genera eficiencias en el mercado.
OCTAVO: Que, esta Superintendencia expondrá los principales beneficios que se pretenden generar con el acuerdo objeto de análisis. Es de señalar que estos beneficios son los esperados, pero no son beneficios sobre los que, a la fecha, se pueda tener un resultado cuantificable. En todo caso, estos beneficios podrán ser evaluados una vez entre en operación el acuerdo de negociación conjunta de medicamentos. La forma en la que se realizará la evaluación de estos beneficios esperados se expondrá en el considerando noveno de esta resolución.
Como se ha expuesto a lo largo de esta resolución, con el acuerdo objeto de análisis se busca reducir los costos, entre otros de transacción, que se generan por la intermediación en la negociación y compra de medicamentos. Igualmente, se quiere disminuir la intermediación en la distribución de los medicamentos. Con estos dos elementos principales del acuerdo se podrían generar economías de escalas eficientes que redundan en beneficios para el sector salud. A continuación, la Superintendencia expondrá siete (7) beneficios que se esperarían obtener con la ejecución del acuerdo.
1. Mejorar la disponibilidad y abastecimiento de las TES
Una de las mejoras que se pretenden generar con la negociación conjunta de TES es asegurar la disponibilidad para responder por las necesidades en salud en todo el país. Esto implica no solo que haya una disminución en el precio, sino que las cantidades disponibles sean suficientes y, además, se pueda contar con la estrategia logística para cubrir todo el territorio nacional. Al generar transacciones que sean directa, sin intermediador, se facilitaría los procesos de adquisición y distribución.[125]
Además, con la posibilidad de mejorar el abastecimiento, también se podría reducir la inequidad territorial que en este momento se puede estar generando. Con la negociación conjunta de las TES se podría priorizar territorios que por la débil presencia institucional en salud no reciben de manera oportuna las TES requeridas. De esta forma se podría garantizar el cubrimiento del derecho a la salud en condiciones de igualdad y, además, estandarizar los procesos de entrega oportuna y completa de las TES requeridas de acuerdo con la situación epidemiológica que sea necesaria atender sin importar la región del país en la que se presente.[126]
Igualmente, con la posibilidad de tener mayor abastecimiento y disponibilidad de medicamentos, se puede fortalecer la capacidad preventiva del SGSSS al poder responder a eventos sanitarios que puedan ser críticos. Con la negociación conjunta de TES se puede mantener un "inventarios estratégicos para enfermedades prevalentes o emergentes” y, también, "integrar la planificación de compras con el sistema de vigilancia en salud pública”.[127]
2. Mayor liquidez derivada de la reducción de los costos de intermediación y prevención del aumento de cartera por concepto en pago de TES
La posibilidad de comprar de manera masiva TES hace que los precios a los que ofrezcan los medicamentos puedan ser más competitivos debido al poder de negociación de las adquirientes frente a la industria farmacéutica. De acuerdo con el Ministerio de Salud, esta situación se vio reflejada en casos como la negociación de TES para el tratamiento del VIH y la Hepatitis C en los que fue posible obtener un descuento sobre estas. La reducción en los costos de los medicamentos -tanto por la eliminación de la intermediación como por la posibilidad de obtener descuentos por compras agregadas- lleva a la reducción del gasto pública, al incremento de los recursos que puede ser destinados a inversión en el sector y aumentar la capacidad de atención a más pacientes.[128]
Además de las mejorías que puede traer para el SGSSS la reducción de los costos en las TES, también puede tener un efecto positivo en la posibilidad de reducir la cartera pasada derivada del no cumplimiento de los pagos por las TES adquiridas. Esto se debe a que la reducción de los costos puede generar liquidez suficiente tanto para pagar deudas pasadas, como prevenir la configuración de una deuda mayor a futuro. Con esto, las Intervinientes podrían contar con más recursos para empezar a cumplir con algunas situaciones financieras que las llevaron a ser intervenidas por parte de la SNS.
Finalmente, es de señalar que, con la reducción de los costos en las TES, las EPS también pueden tener un mejor ahorro operacional. Esto si se tiene en cuenta que los ingresos operacionales pueden empezar a ser mayores que los costos operacionales.
3. Disminución de los incumplimientos en las entregas de los medicamentos y mejoramiento en la vigilancia directa por parte de las EPS respecto de la entrega de medicamentos a los pacientes
Con la negociación conjunta y directa para la adquisición de las TES, las Intervinientes también buscan optimizar los tiempos de entrega si se tiene en cuenta que, como se mencionó en esta Resolución, se intentará eliminar al máximo la intermediación en la distribución de los medicamentos. Con esto se evitaría la fragmentación logística y se podría consolidar el proceso de suministro y distribución de TES en uno (1) o pocos actores en el mercado. Además, se espera lograr una reducción en los tiempos de espera para los pacientes, evitar la interrupción de tratamientos esenciales y mejorar los procesos de programación y distribución de medicamentos, así como el seguimiento a los procesos de dispensación de medicamentos.[129]
De acuerdo con lo señalado por las Intervinientes, con este acuerdo también se quiere cumplir con el tiempo de entrega de medicamentos señalados en la Resolución No. 1604 del 17 de mayo 2013 expedida por el Ministerio de Salud. En este acto administrativo se reglamentó el término de cuarenta y ocho horas (48) para hacer la entrega, en el domicilio que autorice el afiliado, de los medicamentos que no fueron entregados de manera completa al paciente una vez este hizo la reclamación de las TES ordenadas por el médico tratante[130]. El hecho de que no exista una intermediación en la dispensación de medicamentos hace que sea más eficiente tanto la vigilancia como el cumplimiento en las entregas.
4. Mayores inversiones encaminadas en mejorar el servicio en el SGSSS
En la negociación que proponen las Intervinientes se buscará que, dentro del componente técnico, se definan niveles de servicio con el fin de asegurar la calidad, continuidad y oportunidad en las entregas de los medicamentos. Con esto se busca prevenir la comercialización de medicamentos adulterado o de contrabando[131]. Además, el hecho de poder reducir costos en un rubro como el de la adquisición de TES puede generar que las EPS reinviertan ese excedente de ahorro en nuevas tecnologías y mejoramiento del servicio.
5. Disminución en el número de PQRS relacionadas con el incumplimiento en las entregas de medicamentos a los pacientes
Como se menciona en esta Resolución, el número de quejas por incumplimiento tanto en entrega completa como parcial de medicamentos ha aumentado. La propuesta de la negoción conjunta y directa entre las Intervinientes (y la demás EPS que se quieran hacer parte) con las farmacéuticas y laboratorios tiene la intención de que la entrega de las TES se haga de manera eficiente y cumpliendo los tiempos de atención que requieren los pacientes. Por esto, si hay un cumplimiento efectivo en la dispensación de las TES, necesariamente tendría que haber una reducción en el número de PQRS presentadas por ese concepto. El dato de la disminución en el número de quejas demostraría, de manera preliminar, que la ejecución del acuerdo estaría cumpliendo con el objeto por el que fue propuesto.
6. Transparencia de la información y claridad en la situación económica de las negociaciones de las TES
La posibilidad de centralizar y agregar la negociación para la adquisición de las TES permite que haya mayor trazabilidad y visibilidad de los procesos contractuales para la adquisición y dispensación de medicamentos[132]. Con esto se podría disminuir el riesgo de corrupción en los procesos de contratación y, a la vez, se podría fortalecer la rendición de cuenta sobre el uso de los recursos destinados al SGSSS[133]. Adicionalmente, gracias a la transparencia de la información que puede generarse en el marco de la negociación conjunta, se podría contar con datos claros y concretos para poder hacer un análisis preciso sobre la logística en la dispensación de medicamentos, lo puede ser una herramienta útil para mejorar el servicio.
7. Efectos positivos que se podrían generar para la libre competencia económica en el SGSSS
Aunque es claro que el acuerdo objeto de análisis es una excepción a las reglas de competencia, lo cierto es que se espera que las dinámicas que se produzcan en el mercado no generen mayores restricciones de las previstas y, además, se espera que haya beneficios directos en el mercado. En este caso, el sistema de negociación conjunta va a permitir que agentes, como las farmacéuticas y laboratorios, participen de manera libre y competitiva en el proceso de negociación que se adelante. Con esto, las Intervinientes (así como las EPS que se unan a la negociación colectiva) podrán crear escenarios de competencia en los que pueden cubrir las necesidades de abastecimiento a los mejores precios y con la calidad requerida para atender las epidemiologías que sean necesarias[134].
Adicionalmente, con la negociación conjunta se podría generar herramientas útiles para garantizar la seguridad, eficacia y calidad técnica uniforme de las TES contratadas. Al igual que, gracias a la transparencia en la forma de negociación de las TES, se podría fomentar un entorno de competencia justa basado en la selección objetiva.[135]
NOVENO: Que, una vez revisados los elementos del acuerdo objeto de análisis, la Superintendencia definirá el esquema de seguimiento como mecanismo de vigilancia. Este esquema se definirá de acuerdo con lo señalado en el numeral 1.4. del capítulo primero del título VII de la Circular Única de la Superintendencia, el cual indica:
"Deberá señalarse el mecanismo que permita que la Superintendencia vigile el comportamiento de las variables económicas del sector, con detalle de la información que deben suministrar los participantes en el acuerdo. En caso de que la Superintendencia de Industria y Comercio considere que las condiciones del mercado que llevaron a la celebración del acuerdo han sido superadas y el sector se encuentra estable, podrá dar por terminado el acuerdo aun antes del plazo previsto.”
En este acápite se desarrollarán tres elementos para realizar el seguimiento del acuerdo. En primer lugar, se establecerán el mecanismo de seguimiento y vigilancia de la implementación de acuerdo objeto de análisis. En segundo lugar, se establecerá el cronograma del seguimiento. Finalmente, se realizará la Delegación de las funciones de vigilancia y seguimiento en la Dirección de Cumplimiento de la Delegatura para la Protección de la Competencia.
9.1. Seguimiento y vigilancia de la implementación del acuerdo objeto de análisis
Como se mencionó, el numeral 1.4. del capítulo primero del título VII de la Circular Única de la Superintendencia de Industria y Comercio establece que es necesario definir mecanismos de vigilancia que le permita a la Autoridad de Competencia monitorear "el comportamiento de las variables económicas del sector, con detalle de la información que deben suministrar los participantes en el acuerdo”. Las Intervinientes, en la solicitud de autorización del acuerdo objeto de análisis, propusieron entregar informes trimestrales con información relacionada con "las compras directas a los laboratorios y/o proveedores farmacéuticos”[136]. Además, especificaron que esos informes trimestrales tendrían esta información:
- "Indicadores financieros que se impacten con la nueva política, para identificar disminución de costos de moléculas y resultado frente a la siniestralidad por territorial y en el nivel nacional.
- Impactos de la disminución del costo actual, frente a las eficiencias de los recursos disponibles en la gestión administrativa de la EPS.
- Probables impactos de la disminución del costo operativo, frente a los Planes de Acción diseñados por la intervención actual de la EPS.
- Oportunidad en la entrega de medicamentos, desde la prescripción, la autorización hasta la dispensación, buscando dinamizar el proceso para garantizar en todo momento la entrega oportuna y completa de las moléculas.
- Entrega efectiva a los usuarios plenamente identificados como usuarios de las prescripciones entregadas, con vigilancia aleatoria de prescripciones, se identificarán usuarios, moléculas prescritas, profesional quien prescribe, IPS desde donde se prescribe, municipio y territorial, para identificar moléculas, frecuencias, costos y prescriptores.
- Seguimiento a los indicadores en Salud, frente a la estrategia de la disminución de la siniestralidad esperado con esta nueva estrategia comercial.
- Monitoreo PQR, Tutelas, desacatos y sanciones, con la nueva estrategia implementada. Se hará seguimiento con indicadores.”[137]
Con el fin de unificar la información que proponen entregar las Intervinientes en los informes, así como la información que requiere la Superintendencia para realizar un seguimiento adecuado, en este acápite se definirá la información y los indicadores que deberán entregar las Intervinientes. Primero, la Superintendencia indicará la información que deberán enviar las Intervinientes en relación con la implementación y gestión del acuerdo objeto de análisis. En segundo lugar, la Superintendencia definirá los indicadores de seguimiento encaminados a verificar las eficiencias operativas que se esperan con la implementación del acuerdo objeto de análisis. Por último, se definirán los indicadores financieros.
La información requerida y los datos que deben ser incluidos en los indicadores que se exponen en los numerales 9.1.1., 9.1.2. y 9.1.3. tendrán una periodicidad trimestral. Además, en el caso de los indicadores establecidos en los literales del "a” al "f” del numeral 9.1.2.2. y todos los indicadores establecidos en el numeral 9.1.3. tendrán que presentarse para el trimestre de ejecución del acuerdo y, además, el mismo trimestre del año inmediatamente anterior. Por ejemplo, si la información del trimestre de ejecución del acuerdo es de agosto a octubre de 2025, se deberá presentar los indicadores para ese periodo y, además, los mismos indicadores del periodo agosto a octubre de 2024.
Las Intervinientes deberán entregar los soportes documentales que den cuenta de la información utilizada para desarrollar cada uno de los indicadores. Estos soportes deberán estar auditados por el revisor fiscal. Los documentos deberán ser entregados en formato digital al correo electrónico contactenos@sic.gov.co. La información relacionada con datos presentados en tablas e información relacionada con valores debe ser enviada en Excel o archivo plano, los demás documentos en formato PDF.
9.1.1. Información sobre la implementación y gestión del acuerdo objeto de análisis
Con la expedición de esta Resolución, las Intervinientes podrán iniciar las negociaciones de compra conjunta. Además, es de resaltar que empezará a correr el término de duración del acuerdo cuando se suscriba el primer contrato de compra, como se mencionó en el numeral 6.4. del considerando sexto de esta Resolución. Con el fin de poder realizar el seguimiento de las condiciones generales de la ejecución del acuerdo, tanto en la etapa de negociación como en la de contratación, la Superintendencia solicitará tres tipos de información. Primero, información general relacionada con las negociaciones en bloque y la compra individual de TES. Segundo, información de las modificaciones o cambios en el acuerdo analizado. Tercero, conformación de un comité para el seguimiento y ejecución del acuerdo objeto de análisis.
9.1.1.1. Información general relacionada con las negociaciones en bloque y la compra individual de TES
De acuerdo con la solicitud de autorización presentada por las Intervinientes y la información enviada en este trámite administrativo, las (9) EPS propusieron presentar informes trimestrales en los que se exponga la información relacionada con las compras directas a los laboratorios y/o proveedores farmacéuticos. La información del informe será recolectada por SANITAS E.P.S. S.A.S.[138] Además, de la información que las Intervinientes se comprometieron a enviar, la Superintendencia requiere que el informe trimestral tenga la siguiente información:
a. Los estudios técnicos mencionados en el numeral 6.3. del considerando sexto de esta Resolución que serán utilizados para realizar la negociación conjunta con los agentes farmacéuticos (laboratorios o proveedores).
b. La lista de agentes farmacéuticos con los que se realizarán las negociaciones.
c. Las condiciones acordadas y resultados de la negociación conjunta.
d. Copia de los contratos celebrados de manera directa entre las EPS y los agentes farmacéuticos. Debido a que el término de un (1) año de duración del acuerdo empieza a contar a partir de la suscripción del primer contrato, las intervinientes deberán informar esta situación a la Superintendencia dentro de los diez (10) días siguientes a la fecha de suscripción del primer contrato. Esto de acuerdo con lo previsto en el numeral 6.4. del considerando sexto de esta Resolución.
e. La lista de las patologías que serán atendidas en la primera etapa del acuerdo objeto de análisis con indicación de los medicamentos utilizados para el tratamiento de esa patología, lista de los TES que serán negociados en la segunda etapa y lista de los medicamentos que serán negociados en la tercera etapa de acuerdo con las siguientes tablas:
Tabla No. 6. Identificación de medicamentos por patologías para la primera etapa del acuerdo "Medicamentos de alto costo, en sus diferentes presentaciones y concentraciones, los cuales están destinados a tratar enfermedades raras o crónicas graves en pacientes cuyas condiciones de salud requieren tratamientos especiales y prolongados”.
| Patología | Descripción de la molécula en Denominación Común Internacional (DCI) | Agente Farmacéutico (i.e. laboratorios) |
Tabla No. 7. Identificación de TES para la segunda etapa del acuerdo "Dispositivos médicos como pañales desechables en sus diferentes marcas, características y tallas, más Alimentos de Propósito Médico Especial - APME, en sus diferentes marcas, presentaciones y/o concentraciones”
| Dispositivos médicos y Alimentos de Propósito Médico Especial (APME) | Agente Farmacéutico (i.e. laboratorios) |
Tabla No. 8. Identificación de medicamentos para la tercera etapa del acuerdo "Medicamentos genéricos o de bajo costo por el alto volumen en su consumo, en sus diferentes presentaciones y concentraciones”
| Descripción de la molécula en Denominación Común Internacional (DCI) | Agente Farmacéutico (i.e. laboratorios) |
f. Información específica relacionada con las negociaciones y contratos individuales de compra de medicamentos celebrados entre las EPS y los agentes farmacéuticos. Para esto, las EPS deberán enviar las órdenes de compra y convenios suscritos de manera individual con los agentes farmacéuticos. Además, deberán diligenciar la siguiente tabla:
Tabla No. 9. Información de contratos individuales celebrado por cada EPS y los
agentes farmacéuticos.
| Agente farmacéutico (i.e. laboratorio) | NIT | Contacto | Objeto del Contrato | TES adquirida | Volumen | Precio Unitario | Condiciones de entrega | |
9.1.1.2. Información relacionada con las modificaciones o cambios en el acuerdo objeto de análisis
En el mismo informe general mencionado en el anterior literal, las Intervinientes deberán informar cualquier tipo de cambio o modificación que se de en el marco del acuerdo objeto de análisis. Algunos ejemplos de cambios o modificaciones del acuerdo inicialmente analizado pueden ser, sin limitarse, los siguientes:
a. Información sobre EPS que quieran hacerse parte o se hagan parte de le negociación conjunta diferentes a las nueve (9) EPS intervenidas, como se expuso en el numeral 6.3 del considerando sexto de esta Resolución.
b. Inicio de la primer, segunda y tercera etapa de negociación en bloque de TES.
c. Renovación o terminación del acuerdo objeto de análisis.
9.1.1.3. Conformación de un comité para el seguimiento y ejecución del acuerdo objeto de análisis
De acuerdo con la información suministrada por las Intervinientes, las EPS que participen en el acuerdo (tanto las EPS intervenidas como las EPS que no estén intervenidas) realizaran varias actividades de manera conjunta a lo largo de la ejecución de este. Primero, centralizarán los informes que propusieron presentar a la Superintendencia como mecanismo de monitoreo del acuerdo, esto lo realizarán a través de SANITAS E.P.S. S.A.S.[139]. Segundo, establecieron que se realizarían reuniones con los aliados[140]. Tercero, manifestaron que se realizaría evaluaciones conjuntas para llevar a cabo las negociaciones, revisiones periódicas y auditorias de la ejecución del acuerdo objeto de análisis[141].
Con el fin de poder ejecutar todas las funciones antes mencionadas y que haya transparencia frente a la forma en la que estas actividades se realizan, la Superintendencia solicita que se conforme un comité que esté integrado por todas las EPS que hagan parte del acuerdo. Las intervinientes deberán informar a la Superintendencia lo siguiente:
a. La fecha de conformación y documento privado por el que se conforma el comité. Deberán indicar las funciones generales y específicas que realizará el comité en el marco de la ejecución del acuerdo objeto de análisis.
b. Conformación del comité, lista de los representantes de cada EPS que participarán en el comité y reglas de elección de los representantes.
c. Estructura del comité (i.e. presidente, secretario, etc.) en caso de que aplique.
d. Información sobre el cronograma de reuniones y las reuniones que se realicen a lo largo de la ejecución del acuerdo objeto de análisis. También deberán indicar la forma en la que se realizarán la convocatoria de las reuniones ordinarias y extraordinarias.
e. Mecanismos en los que se tomaran las decisiones en el marco del comité, lo que debe incluir el quorum para deliberar y decidir, si es el caso.
f. Mecanismos de resolución de controversias que se den en el marco de la ejecución del acuerdo objeto de análisis.
g. Copia de las actas de las reuniones realizadas.
h. Copia de los reportes de evaluación y auditoría que sean analizados por este comité.
Este comité deberá ser creado antes del inicio de las negociaciones conjuntas y su conformación deberá ser informada a la Superintendencia dentro de los diez (10) días siguientes a su formación.
9.1.2. Indicadores de seguimiento encaminados a verificar la eficiencia operativa
Este acuerdo en bloque presenta como eficiencias esperadas la disponibilidad de TES en todo el país, el abastecimiento completo de TES, y la disminución de la inequidad territorial en cuanto al suministro de TES. De la misma manera, este acuerdo busca optimizar los procesos de suministro y dispensación de TES y, como consecuencia, mejorar la calidad de las entregas de TES a los afiliados. De esta manera, los indicadores de eficiencia operativa permitirán detallar el cumplimiento de las eficiencias esperadas. Así, las Intervinientes propusieron seis (6) indicadores y esta Superintendencia formuló siete (7) indicadores adicionales. Con estos indicadores se quiere verificar trimestralmente las variaciones mensuales de las entregas a tiempo de TES, variación en el número las PQRS, el abastecimiento de TES y las TES con novedades de escasez, entre otros elementos.
9.1.2.1. Indicadores de eficiencia operativa propuestos por las Intervinientes
Las Intervinientes, tanto en la solicitud de autorización del acuerdo objeto de análisis como en la información enviada en este trámite administrativo, propusieron un sistema de seguimiento del acuerdo. Para esto, formularon el análisis de dos elementos del acuerdo. Por un lado, manifestaron la necesidad de medir el cumplimiento de la ejecución operativa y de la calidad en el acceso a medicamentos. Por otro, establecieron que es necesario tener información sobre las necesidades de compra de medicamentos para poder, de manera eficiente, realizar las negociaciones con los agentes farmacéuticos.
Para poder medir las eficiencias en la gestión operativa, las Intervinientes propusieron seis (6) como se muestra a continuación:
- "Porcentaje de cumplimiento en entrega según cronograma (meta: mayor o igual a 95%).
- Porcentaje de abastecimiento sin ruptura de stock (meta: mayor
o igual a 98%).
- Número de reclamaciones por no entrega o entrega tardía (meta: menor o igual a 2%).
- Porcentaje de TES entregadas con trazabilidad completa.
- Porcentaje de adherencia de protocolos clínicos establecidos.
- Número de hallazgos o alertas derivadas de auditoría técnica o farmacovigilancia.”[142]
Adicional a estos indicadores, las Intervinientes y la SNS establecieron que, para poder cuantificar de manera técnica y real las cantidades requeridas de medicamentos se realizaría un análisis de las siguientes variables técnicas:
- "La sumatoria del consumo histórico consolidado de cada una de las EPS intervenidas, con base en reportes de prescripción, dispensación y facturación.
- Proyecciones ajustadas por tendencia epidemiológica y distribución geográfica de la población afiliada.
- Análisis de caracterización por cohortes clínicas (enfermedades crónicas, alto costo, patologías prevalentes, incidentes y eventos catastróficos).
- Identificación de eventos de no entrega, reclamaciones (PQR) y patrones de judicialización asociados a medicamentos.”[143]
Con el fin de tener información completa para realizar el seguimiento y vigilancia del acuerdo objeto de análisis, la Superintendencia le solicitará a las Intervinientes que envíen en el informe trimestral la información y datos que resulten de los indicadores y variables antes mencionadas. Esta información debe ser enviada con los anexos y soportes a los que haya lugar.
9.1.2.2. Indicadores de eficiencia operativa requeridos por la Superintendencia de Industria y Comercio
La Superintendencia, para desarrollar un seguimiento adecuado del cumplimiento de las eficiencias y los beneficios esperados del acuerdo en bloque, requerirá trimestralmente la información mensual de ocho (8) indicadores operativos. En particular, estos indicadores se construyen a partir de nueve (9) variables de cada una de las EPS participantes del acuerdo. Es importante resaltar que, aunque la información para calcular los indicadores y sus respectivos soportes serán requeridas trimestralmente, esta información deberá estar discriminada por cada uno de los tres meses del periodo. Por ejemplo, si se evalúa el trimestre de agosto a octubre, la información solicitada deberá presentarse de forma desagregada para cada uno de los meses -agosto, septiembre y octubre-.
a. PQRS recibidas relacionadas con calidad, suministro o dispensación de TES por cada 10.000 afiliados
Uno de los principales efectos de las eficiencias esperadas se define como el número de PQRS recibidas relacionas con calidad, suministro o dispensación de TES por cada 10.000 afiliados. En específico, este indicador presenta la cantidad de este tipo de PQRS recibidas si la EPS analizada presentara 10.000 de afiliados.
![]()
De esta manera, la variable de "PQRS recibidas” relacionadas con calidad, suministro o dispensación de TES se considera una aproximación robusta para describir la calidad de prestación de servicio de una EPS con el suministro de TES. Así, una reducción en las PQRS recibidas en relación con las TES implicaría una mejora en la prestación del servicio de salud.
En específico, este indicador se constituye por cada 10.000 afiliados para facilitar la comparación entre EPS participantes del acuerdo y, también, para afectar el análisis del indicador frente a posibles variaciones en el número de afiliados. Por ejemplo, en el caso de que se analice únicamente la variable de PQRS recibidas, un incremento de afiliados podría elevar el número de PQRS recibidas, a pesar de que alguna Interviniente mejore su calidad en el suministro de TES.
Finalmente, además de que la información de las variables de este indicador se envíe en sus totales, se requerirá que ésta sea desagregada también entre departamentos y Bogotá, D.C.
b. Porcentaje de PQRS recibidas relacionadas con calidad, suministro o dispensación de TES con relación al total de PQRS recibidas
En concordancia con lo anterior, el porcentaje de PQRS relacionadas con la calidad, suministro o dispensación de TES con respecto al total PQRS recibidas da cuenta de la mejora de la calidad en el servicio de salud con las TES.
![]()
Estrictamente, este indicador -en línea con el indicador anterior- permite analizar variaciones reales de las PQRS recibidas por TES y no por cambios asociados a disminuciones de afiliados y del total de PQRS recibidas. Dicho de otra forma, una posible disminución de afiliados podría retratar una disminución del total de PQRS recibidas por TES y también del total de PQRS recibidas, a pesar de que la calidad en el suministro y dispensación en medicamentos no haya presentado una variación.
Por último, se requiere que las dos variables de este indicador, además de que se envíen en su totalidad, se desagreguen por los 32 departamentos y Bogotá D.C. Esto permitirá realizar un seguimiento directo sobre las variaciones en la calidad de la dispensación y suministro de TES desde un enfoque descentralizado. Adicionalmente, se solicita que la información de estas dos variables también se encuentre desagregada por las patologías de seguimiento de la primera etapa, las cuales serán reportadas por las EPS participantes del acuerdo tal como se estipula en el literal "e” del numeral 9.1.1.1.
c. Porcentaje de PQRS recibidas por no entrega de TES con relación al total de PQRS recibidas
De forma particular, la no entrega de TES puede generar una mayor afectación y riesgo a la salud de afiliados que una entrega de TES atrasada. Por esta razón se define un indicador con el fin de determina las variaciones de las PQRS recibidas relacionadas con la no entrega de TES.
![]()
Es imperativo abordar el seguimiento de este indicador desde un análisis comparativo entre los departamentos del país. Esto, con el propósito de evidenciar las mejoras en la calidad desde un enfoque territorial. Debido a esto, la información de las dos variables de este indicador deberá ser enviada de forma desagregada por los 32 departamentos y Bogotá D.C.
d. Porcentaje de PQRS relacionadas con TES a las que se les dio respuesta de manera oportuna
La Superintendencia considera importante que se dé respuesta oportuna a las PQRS relacionadas con TES que las EPS reciban durante el tiempo de ejecución del acuerdo. Debido a esto, se formula el siguiente indicador con el fin de tener, en valores porcentuales, la respuesta efectivas a las PQRS relacionadas con las TES:
![]()
El seguimiento de este indicador se realizará de manera comparativa entre los departamentos del país. Esto, con el propósito de evidenciar las mejoras en la calidad desde un enfoque territorial. La información de las dos variables de este indicador deberá ser enviada de forma desagregada por los 32 departamentos y Bogotá D.C.
e. Porcentaje de entregas a tiempo con respecto al total de TES suministradas y dispensadas
Las Intervinientes establecieron que el acuerdo en bloque y la compra directa de TES mejorarán la cadena de suministro y la operación logística de la dispensación y suministro de éstas[144]. Las mejoras se verán reflejadas en el cumplimiento del cronograma de suministro y dispensación de TES. De ahí que, el porcentaje de las entregas de TES a tiempo del total de TES dispensadas y suministradas es una aproximación acertada para realizar el seguimiento a esta eficiencia.
![]()
El seguimiento de este indicador se realizará de forma comparativa entre departamentos del país, por lo que se solicitará la información desagregada por los 32 departamentos y Bogotá D.C. para las dos variables de este indicador.
f. Porcentaje de TES con novedad de "escaseado” o "Bajo nivel de servicio” frente a las 238 TES reportadas por las Intervinientes como "escaseado” o "bajo nivel de servicio”[145]
Otra de las eficiencias que se espera obtener con este acuerdo es el abastecimiento de TES. En particular, las Intervinientes identificaron 238 TES[146] que tiene la novedad de "Escaseado” o "Bajo nivel de servicio”[147]. Por lo que, es relevante realizar un seguimiento al cambio de estado de novedad de este grupo de 238 TES. Para esto, el presente indicador se conforma por el número de TES del grupo de 238 TES presentadas por las Intervinientes que aún se encuentren dentro de las novedades de "Escaseado” o "Bajo nivel de servicio” en el periodo en relación con el total de 238 TES con reportadas estas novedades en abril de 2025:
![]()
Este indicador se puede presentar como:
![]()
Debido a la naturaleza de la información de este indicador, estos datos en específico no deben ser enviados de forma desagregada por EPS.
g. Número de TES con novedad de "Escaseado” o "Bajo nivel de servicio”, y su lista.
En relación con lo anterior, es importante conocer el estado de las TES -en palabras de las Intervinientes- "más representativas” con novedad de "escaseado” o "bajo nivel de servicio” en el país148. De esta manera, para este seguimiento, la Superintendencia solicita la cantidad y la lista de estas TES que tengan esas características, paro lo cual deberán presentar el siguiente indicador:
![]()
Además, deberán diligenciar la siguiente tabla:
Tabla No. 10. Identificación de TES en condición de "escaseado” o "bajo nivel de servicio”
| Agente Farmacéutico (i.e. Laboratorio) | Descripción de la molécula en Denominación Común Internacional (DCI) | Grupo terapéutico | Novedad relacionada |
h. Variación de afiliados
La Superintendencia también requiere el número de afiliados de cada una de las EPS firmantes del acuerdo.
![]()
Además del dato total de afiliados, las EPS que participen en el acuerdo deben enviar la información del número de afiliados discriminados por (i) departamentos y Bogotá D.C., y (ii) por patología que, para este caso, deberán las patologías identificadas en la tabla No. 6.
Tabla No. 11. Número de afiliados discriminados por departamento y patología
| Departamento | Patología (de las identificadas en la Tabla No. 6) | Número de afiliados |
9.1.3. Indicadores financieros
Como se ha mencionado a lo largo de esta Resolución, la compra directa de TES puede generar economías de escala y aumento de poder de negociación de las EPS participantes de este acuerdo. Estas situaciones podrían contribuir a la disminución de los costos de compra y dispensación de las TES. Con esta reducción en los costos, las EPS podrían cubrir las obligaciones a corto plazo, los pasivos y, también, aligerar la carga de cartera vencida. Incluso, podría aumentar la inversión en capital y, por tanto, mejorar la calidad de los servicios. Con el fin de hacer seguimiento a la materialización de las eficiencias financiera, esta Superintendencia formuló ocho (8) indicadores financieros conformados por doce (11) variables.
a. Porcentaje de los costos en compras y en dispensación de las TES del total de costos operacionales.
Con el fin de evidenciar la variación de los costos en la compra y dispensación de TES frente a los costos operacionales, se formula el siguiente indicador:
![]()
Este indicador permite comparar el porcentaje de los costos en compra y dispensación en TES antes de la firma del acuerdo y después del acuerdo, así como también la posible mejora constante después del acuerdo. De esta manera, el modelo de compra directa de TES puede disminuir los costos de compra en contraposición con la compra a través de intermediarios. En específico, las Intervinientes estiman que se pueden optimizar los costos de compra de las TES en $396.535 millones de pesos por año[149].
Es preciso tener presente que la adecuación de lo pactado o la dispensación también puede incurrir en costos adicionales que no se encontraban en la compra de TES a través de intermediarios. Por lo tanto, la Superintendencia considera incluir, además de los costos de compra, los costos de dispensación de TES dentro de este indicador. No obstante, es posible que los costos de dispensación se interioricen en el precio de venta de TES por parte de los agentes farmacéuticos, lo que haría que los costos de compra de TES y los costos analizados en este indicador sean los mismos, lo cual dependerá de lo pactado en las negociaciones entre las Intervinientes y los agentes farmacéuticos.
Por otro lado, después de la firma del acuerdo, existe la posibilidad de que las eficiencias esperadas presenten mejoras de forma gradual debido a mejoras del acondicionamiento de los procesos y aprendizaje de estos, y economías de escala. De ahí que, es imperativo realizar una comparación de los indicadores entre los trimestres de análisis.
Por último, es importante recalcar que la información de la variable "Costos en compra y dispensación de TES” de este indicador se solicita de forma, además de su valor total, desagregada geográficamente entre los 32 departamentos y Bogotá D.C. Asimismo, se solicita que la información de esta misma variable se desagregue por las patologías de la primera etapa determinadas por las Intervinientes, de acuerdo con lo señalado en la Tabla No. 6 del literal "e” del numeral 9.1.1.1.
b. Costos en compra y en dispensación de TES por afiliado
En complemento con el indicador anterior, para determinar la disminución de los costos en compra y en dispensación de las TES de cada EPS por afiliado se formula el siguiente indicador que permite evaluar las eficiencias esperadas por parte de las Intervinientes del acuerdo en el periodo t.
![]()
En esencia, el costo en compra y dispensación de TES per cápita hace que posibles aumentos en el número de afiliados no alteren el análisis. En particular, a pesar de una mejora en la eficiencia en este costo, un aumento de afiliados incrementaría los costos en compra y dispensación de TES, lo que afectaría el análisis. Por lo tanto, realizar un control con el número de afiliados -en línea con el indicador anterior- evitaría esta situación.
Más aún, este indicador permite evidenciar las eficiencias en los costos en compra y dispensación de TES para cada uno de los departamentos del país y de Bogotá, así como identificar las diferencias en las eficiencias entre las mismas EPS al comparar entre sí sus datos. De ahí que se solicita que la información de las dos variables de este indicador, además de incluir su total, se encuentren desagregadas geográficamente entre los 32 departamentos y Bogotá D.C., así como por las patologías de la primera etapa establecidas por las Intervinientes en la Tabla No. 6 del literal "e” del numeral
c. Costos en compra y en dispensación por unidad de TES
Aunado a lo anterior, este indicador evalúa los costos en la compra y en la dispensación por unidad de TES en su presentación comercial para cada EPS i en un periodo determinado t.
![]()
Particularmente, la disminución en los precios en la compra y en la dispensación de TES se podrá evidenciar en la variación del costo promedio de éstas por unidad de presentación comercial. Asimismo, este indicador permite realizar un análisis desagregado por patologías y los costos promedio por unidad de TES, lo que ayudaría al seguimiento y a la toma de decisiones de cada una de las Intervinientes enfocadas a las eficiencias de los procesos de compra directa.
Adicionalmente, es importante establecer que, según la composición de este indicador, un aumento en el costo de las compras de TES relacionado con el incremento de unidades compradas no afectará el valor final del indicador, ya que éste se encuentra controlado por la cantidad de TES compradas.
Por último, se solicita que la información de la variable "Costos en compra y dispensación de TES” presente desagregación geográfica, entre los 32 departamentos y Bogotá, D.C.
d. Gastos administrativos por cada 10.000 afiliados
Si bien este acuerdo en bloque entre EPS se enfoca en reducir los costos en la compra y adquisición de las TES, se considera necesario hacer un seguimiento a los gastos administrativos de cada EPS firmante. En particular, los acuerdos que se establezcan con los agentes farmacéuticos y los operadores logísticos podrían generar cambios en las EPS involucradas que elevasen algunas de sus cuentas de gasto. De esta manera, se propone realizar un seguimiento de los gastos administrativos de cada EPS por cada 10.000 afiliados.
![]()
Específicamente, este indicador analiza los gastos administrativos per cápita en los que incurriría una EPS i en un periodo t, lo que permite analizar posibles variaciones de los gastos al ponderar por la cantidad de afiliados. Por ejemplo, a pesar de que el acuerdo en bloque haya mejorado la eficiencia de los gastos administrativos, un incremento en el número de afiliados podría elevar los gastos administrativos y, por tanto, no permitiría un análisis riguroso.
e. Rentabilidad operacional
Por su parte, la diferencia entre los ingresos operacionales y los costos operacionales de una organización presenta una lectura de la capacidad operativa de ésta. Ahora bien, para que pueda ser comparable con otras organizaciones, esta diferencia se puede dividir entre los mismos ingresos operacionales. Este indicador se le conoce como la rentabilidad operacional y da cuenta del porcentaje que equivale esta diferencia con respecto al total de los ingresos operacionales.
![]()
De ahí que, un alto porcentaje de este indicador indica una alta capacidad de liquidez, de inversión y de sostenibilidad, en tanto que los ingresos operacionales son mayores en gran medida que los costos operacionales. Así, este indicador permite el seguimiento de las diferentes eficiencias esperadas en este acuerdo en bloque; en particular, la disminución de los costos en compras y dispensación de las TES. Más aún, que este indicador se encuentre como un porcentaje de la razón entre el flujo de caja operacional sobre los ingresos operacionales de una EPS permite que pueda ser comparable con otras EPS, como las firmantes de este acuerdo.
f. Razón corriente
La liquidez es un concepto financiero importante que permite evaluar la capacidad de una entidad para cubrir sus obligaciones en el corto plazo. De ahí que, una liquidez saludable contribuye a no aumentar la cartera vencida, poder atender coyunturas y permitir la operación en una organización. Ésta se define como la división entre los activos corrientes y los pasivos corrientes.
![]()
Ahora bien, como resultado del acuerdo en bloque, se espera que este indicador presente un aumento debido a la disminución de las cuentas por pagar relacionadas con la compra y dispensación de TES. No obstante, se considera necesario que este indicador se complemente con los indicadores anteriores en tanto que una mayor capacidad de pago en el corto plazo puede ser utilizada para reducir la cartera vencida o ser invertida para desarrollar mejores servicios y, por tanto, no evidenciarse en el análisis.
Finalmente, este indicador se constituye como aproximación acertada para evaluar la capacidad de pago de obligaciones en el corto plazo. No obstante, es importante tener en cuenta que las cuentas por cobrar -dentro del rubro de activos corrientes- pueden presentan diferentes niveles de riesgo de no recuperación y deterioros, particularmente dentro del sector salud. A pesar de esto, la razón corriente sigue siendo un indicador eficaz para evaluar la liquidez saludable de una organización.
g. Razón de endeudamiento
En paralelo con el indicador anterior, la razón de endeudamiento evalúa la diferencia entre los pasivos y los activos de una organización y, por tanto, su seguimiento permite evidenciar si las eficiencias esperadas de este acuerdo en bloque contribuyen a mejorar las condiciones financieras de las Intervinientes.
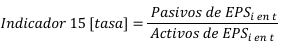
Este indicador se constituye como una razón en tanto que los pasivos de varias Intervinientes son mayores que los activos. De la misma forma, una razón hace que los valores entre diferentes EPS sean comparables. En general, siguiendo las eficiencias planteadas anteriormente, se espera que este indicador disminuya después de la firma del acuerdo en bloque y, a su vez, decrezca constantemente durante el acuerdo en bloque.
Esta situación implicaría, por un lado, que la liquidez generada por la disminución de los costos de compra de TES se dirija a cubrir los diferentes pasivos y, por tanto, hacer que estos disminuyan en comparación con los activos. De otra manera, esto también podría significar que la disminución en los costos de compra de TES fomente la inversión en nuevos activos que puedan mejorar la calidad en la prestación de los servicios de salud de la Intervinientes.
h. Cartera vencida por cada 10.000 afiliados
Aunado con lo anterior, la disminución de la cartera vencida permite mejorar las condiciones financieras de una organización. En específico, las Intervinientes que tengan una cartera vencida pueden tratar esta situación al utilizar las eficiencias esperadas por este acuerdo en bloque y dirigir ahorros en costos para cubrir estas obligaciones vencidas. De esta manera, el seguimiento a la cartera vencida es importante para dar cuenta del aprovechamiento de esas eficiencias.
![]()
Un decrecimiento de este indicador entre periodos de análisis daría cuenta de que la cartera vencida de una EPS presentaría una disminución. Es importante resaltar que este indicador se presenta "por cada 10.000 afiliados” con el propósito de contrastar las variaciones entre las EPS participantes del acuerdo e, incluso, con otras EPS que no hagan parte del acuerdo en bloque.
9.2. Cronograma de seguimiento y vigilancia de acuerdo objeto de análisis en esta resolución
Con el fin de unificar las fechas de entrega de la información descrita en el numeral 9.1., a continuación, se presenta el cronograma de entrega:
Tabla No. 12. Cronograma de seguimiento para la vigilancia del acuerdo objeto de análisis
| Información requerida | Fecha de entrega | Observaciones | |
| Numeral 9.1.1.1. | La información deberá ser entregada de manera trimestral. | En caso de que, para la fecha de entrega de los informes, no | |
| Para la entrega del primer informe, el trimestre empezará a contar desde la fecha de expedición de esta resolución. Los informes siguientes que deban entregar las Intervinientes se unificarán con la fecha de entrega de los numerales 9.1.2. y 9.1.3. La entrega de cada informe se deberá hacer dentro de los diez (10) días hábiles siguientes a la terminación del trimestre que se va a reportar. | tenga la información requerida, deberá solicitar la prórroga correspondiente antes del vencimiento del plazo establecido. En caso de que no haya un cambio en la información previamente enviada, debe manifestarlo de forma expresa. | ||
| Literal "d” del numeral 9.1.1.1. | La información relacionada con la suscripción del primer contrato de compra de medicamentos deberá ser enviada dentro de los diez (10) días siguientes a la fecha de suscripción del primer contrato. | Esta fecha marcará el inicio del acuerdo objeto de análisis, de acuerdo con lo establecido en el numeral 6.4. del considerando sexto de esta Resolución. | |
| Numeral 9.1.1.2. | La información deberá ser entregada en la misma fecha indicada para el numeral 9.1.1.1. | En caso de que, para la fecha de entrega de los informes, no tenga la información requerida, deberá solicitar la prórroga correspondiente antes del vencimiento del plazo establecido. En caso de que no haya un cambio en la información previamente enviada, debe manifestarlo de forma expresa. | |
| Numeral 9.1.1.3. | La información sobre la conformación del Comité deberá ser enviada dentro de los diez (10) días siguientes a su formación. | La conformación del comité se deberá realizar antes del inicio de las negociaciones en bloque. | |
| Literales "a” al "h” del numeral 9.1.1.3. | La información deberá ser entregada en la misma fecha indicada para el numeral 9.1.1.1. | En caso de que, para la fecha de entrega de los informes, no tenga la información requerida, deberá solicitar la prórroga correspondiente antes del vencimiento del plazo establecido. En caso de que no haya un cambio en la información previamente enviada, debe manifestarlo de forma expresa. | |
| Numeral 9.1.2.1. | La información deberá ser entregada de manera trimestral. El periodo trimestral por analizar iniciará el primer día del mes siguiente de la fecha de inicio del acuerdo (numeral 6.4. del considerando sexto). A manera de ejemplo, si la fecha de inicio de ejecución del acuerdo es el 17 de julio, el trimestre de seguimiento empezaría el 1 de agosto y finalizaría 31 de octubre. (Esto no aplica si la fecha de inicio del acuerdo es el 1 día del mes). Al final, el cuarto periodo de seguimiento finalizará el último día calendario del doceavo mes de seguimiento. La fecha de entrega de la información será dentro de los diez (10) días siguientes a la finalización del trimestre a analizar. | En caso de que, para la fecha de entrega de los informes, no tenga la información requerida, deberá solicitar la prórroga correspondiente antes del vencimiento del plazo establecido. En caso de que no haya un cambio en la información previamente enviada, debe manifestarlo de forma expresa. | |
| literales del "a” al "g” del numeral 9.1.2.2. | La información deberá ser entregada en la misma fecha indicada para el numeral 9.1.2.1. | La información de los indicadores desarrollados en los literales "a” al "g” tendrán que presentarse para el trimestre de ejecución del acuerdo y, además, el mismo trimestre del año inmediatamente anterior. Por ejemplo, si la información del trimestre de ejecución del acuerdo es de agosto a octubre de 2025, se deberá presentar los indicadores para ese periodo y, además, los mismos indicadores del periodo agosto a octubre de 2024. En caso de que para la fecha de entrega de los informes no tenga la información requerida o no haya un cambio en la información previamente enviada, debe manifestar esta situación. | |
| Literal "h” del numeral 9.1.2.2. | La información deberá ser entregada en la misma fecha indicada para el numeral 9.1.2.1. | La información del literal "h” solo tendrá que presentarse para para el trimestre de ejecución del acuerdo. En caso de que para la fecha de entrega de los informes no tenga la información requerida o no haya un cambio en la información previamente enviada, debe manifestar esta situación. | |
| Numeral 9.1.3. | La información deberá ser entregada en la misma fecha indicada para el numeral 9.1.2.1. | La información tendrá que ser entregada con las mismas condiciones establecidas para el numeral 9.1.2.2. literales del "a” al "g”, es decir, con la información comparada para el año inmediatamente anterior. | |
Fuente: Elaborado por la Superintendencia de Industria y Comercio.
9.3. Delegación, en la Dirección de Cumplimiento de la Delegatura para la Protección de la Competencia, de la función de vigilancia y seguimiento del acuerdo objeto de análisis en esta resolución
De acuerdo con el numeral 8 del artículo 1 y el numeral 10 del artículo 3 del Decreto 092 de 2022, el Despacho de la Superintendente de Industria y Comercio autorizará los acuerdos de que trata el parágrafo único del artículo 1 de la Ley 155 de 1959. Además, en el numeral 1.4. del capítulo primero del título VII de la Circular Única de la Superintendencia se estableció que se debe definir un mecanismo que le permita a la Superintendencia vigilar "el comportamiento de las variables económicas del sector, con detalle de la información que deben suministrar los participantes en el acuerdo”. Con el fin de realizar esta vigilancia de manera adecuada, la Superintendente de Industria y Comercio delegará esta función en la Dirección de Cumplimiento de la Delegatura para la Protección de la Competencia. Es de resaltar que la función que se delega está encaminada a realizar la vigilancia del acuerdo objeto de análisis, de acuerdo con los parámetros establecidos en esta resolución.
Este acto de delegación[150] se realiza de acuerdo con las dos condiciones previstas en el artículo 9 de la Ley 489 de 1998[151] -(i) delegación en empleados públicos de nivel directivo y asesores y (ii) que ejerza funciones afines o complementarias-. Por una parte, la Superintendente delega una función asignada a la Entidad en una dependencia con funcionarios de nivel directivo. Como se puede verificar en el Organigrama de la Entidad, la Dirección de Cumplimiento está en cabeza de un funcionario de nivel directivo. Además, la Dirección de Cumplimiento hace parte de la Delegatura para la Protección de la Competencia que, también, está en cabeza de una funcionaria del nivel directivo, la Superintendente Delegada para la Protección de la Competencia.
De otra pare, la Dirección de Cumplimiento cumple con funciones afines y complementarias a la que se delega en este acto administrativo. Los numerales 1 y 2 del artículo 5 del Decreto 092 de 2022[152] establecen que la Dirección de Cumplimiento tiene las funciones de realizar seguimiento de las garantías aceptadas por la Superintendente por las que se archiva de manera anticipada una investigación y, además, vigila el cumplimiento de los condicionamientos establecidos por la Superintendente en las solicitudes de integraciones empresariales. Las funciones antes descritas muestran que la Dirección de Cumplimiento cuenta con experiencia en el seguimiento y vigilancia de las instrucciones impartidas a agentes del mercado en procesos administrativos las cuales son funciones similares a las establecidas en el numeral 1.4. del capítulo primero del título VII de la Circular Única de la Superintendencia de Industria y Comercio.
Es de señalar que esta delegación también cumple con los requisitos establecidos en el artículo 10 de la misma ley[153] en el sentido de que se establece de manera concreta que, primero, la autoridad Delegataria es la Dirección de Cumplimiento de la Delegatura para la Protección de la Competencia y, segundo, las funciones específicas que se transfieren, como se mencionó antes, es el seguimiento y la vigilancia del acuerdo objeto de análisis en esta resolución. Finalmente, es de resaltar que la delegación de las funciones descritas no son funciones indelegables de acuerdo con el artículo 11 de la ley antes mencionada[154].
DÉCIMO: Que la Superintendencia realizará algunas recomendaciones a las Intervinientes con el fin de proteger la libre competencia económica durante la ejecución del acuerdo objeto de análisis. Estas recomendaciones no son taxativas sino enunciativas y lo que buscan es poder dar unos lineamientos de buenas prácticas en temas de libre competencia.
En primer lugar, el acuerdo objeto de análisis en esta Resolución no está relacionado con conductas objeto de investigación por prácticas anticompetitivas. Tampoco ha sido sancionada una conducta idéntica a la analizada ni que involucre a las Intervinientes. Debido a esto, este acuerdo cumple con lo establecido en el numeral 1.5. del capítulo primero del título VII de la Circular Única de la Superintendencia de Industria y Comercio[155].
En segundo lugar, como se mencionó en el numeral 9.3. del considerando noveno, la Dirección de Cumplimiento llevará acabo el seguimiento y vigilancia de la ejecución del acuerdo que se autoriza en esta Resolución. La Dirección de Cumplimiento podrá realizar los requerimientos de información que considere necesarios para ejercer sus funciones, así como solicitar aclaraciones frente a la información suministrada por las Intervinientes[156]. En los casos en que la información sea entregada de manera errónea, incompleta o fuera del término fijado, las Intervinientes podrían incurrir en la conducta prevista en el artículo 25 de la Ley 1340 de 2009 y podrían ser sancionadas con la multa establecida en ese artículo[157].
En tercer lugar, la Dirección de Cumplimiento podrá realizar sesiones de capacitaciones en temas de cumplimiento relacionados con la libre competencia económica[158]. La asistencia a estas sesiones, en caso de ser citadas, será obligatoria por parte de las Intervinientes y de las EPS que se hagan parte del acuerdo objeto de análisis. Con esto se busca, por un lado, promover una cultura de la libre competencia económica y, por otro lado, que las EPS implementen programas de cumplimiento en materia de libre competencia económica[159].
En cuarto lugar, las Intervinientes deberán prevenir la configuración de cualquier conducta anticompetitiva. Por lo anterior, esta Superintendencia hace un llamado a evitar que se realicen conductas que puedan configurar abusos derivados del nuevo poder de negociación que adquieren las EPS. En ese sentido, las Intervinientes no podrán establecer condiciones que obstruyan la participación de las EPS no intervenidas en el acuerdo. Además, las EPS deberán realizar las negociones conjuntas de manera transparente y objetiva. Con esto se busca que las Intervinientes actúen de manera leal en el mercado. Igualmente, las Intervinientes deberán adoptar las medidas necesarias para evitar la transferencia de información sensible entre EPS que no tenga relación con el acuerdo objeto de análisis.
Por último, la Superintendencia publicará en la página web de la entidad la versión pública de esta Resolución. Esto con el fin de dar a conocer a la ciudadanía esta decisión, la cual tiene un impacto directo en un sector básico de la economía como se describió en el numeral 5.2. del considerando quinto de esta Resolución.
En mérito de lo expuesto, este Despacho,
RESUELVE
ARTÍCULO 1. AUTORIZAR. El acuerdo para defender la estabilidad del sistema general de seguridad social en salud en Colombia, de acuerdo con las condiciones previstas en esta Resolución.
PARÁGRAFO. Este acuerdo tendrá una duración de un (1) año a partir de la firma del primer contrato de compra de medicamentos, de acuerdo con lo previsto en el numeral 6.4. considerando sexto de esta Resolución, y podrá será prorrogado por otro año más. No obstante, los efectos de esta Resolución son aplicables desde su expedición y cobijan la etapa de negociación conjunta.
ARTÍCULO 2. DELEGAR. En la Dirección de Cumplimiento la función de seguimiento y vigilancia de la implementación y ejecución del acuerdo objeto de análisis en esta Resolución, de acuerdo con lo establecido en el numeral 9.3. del considerando noveno de esta Resolución.
ARTÍCULO 3. ORDENAR. A E.P.S. SANITAS S.A.S., ASMET SALUD EPS S.A.S., EMSSANAR EPS S.A.S., EPS FAMISANAR S.A.S., NUEVA EPS S.A., SAVIA SALUD EPS, EPS-SOS S.A., CAPRESOCA EPS y COOSALUD EPS S.A. cumplir con el envío de la información establecida en los considerandos noveno y décimo de esta Resolución, de acuerdo con los términos definidos por la Superintendencia de Industria y Comercio.
ARTÍCULO 4. INSTAR. A E.P.S. SANITAS S.A.S., ASMET SALUD EPS S.A.S., EMSSANAR EPS S.A.S., EPS FAMISANAR S.A.S., NUEVA EPS S.A., SAVIA SALUD EPS, EPS-SOS S.A., CAPRESOCA EPS y COOSALUD EPS S.A. acoger e implementar las recomendaciones realizadas por la Superintendencia de Industria y Comercio en el considerando décimo de esta Resolución.
ARTÍCULO 5. COMUNICAR. El contenido de esta Resolución a E.P.S. SANITAS S.A.S., ASMET SALUD EPS S.A.S., EMSSANAR EPS S.A.S., EPS FAMISANAR S.A.S., NUEVA EPS S.A., SAVIA SALUD EPS, EPS-SOS S.A., CAPRESOCA EPS, COOSALUD EPS S.A.[160], la SUPERINTENDENCIA NACIONAL DE SALUD y el MINISTERIO DE SALUD Y PROTECCIÓN SOCIAL.
ARTÍCULO 6. PUBLICAR. En la página web de la Superintendencia de Industria y Comercio la versión pública de esta Resolución por el término de diez (10) días, de acuerdo con lo previsto en el considerando décimo de esta Resolución.
COMUNÍQUESE, PUBLÍQUESE Y CÚMPLASE
Dada en Bogotá D.C, a los 10 de junio de 2025.
CIELO ELAINNE RUSINQUE URREGO
La Superintendente de Industria y Comercio,
1. El Decreto 092 de 2022 modificó el Decreto 4886 de 2011. Para efectos de esta Resolución, los artículos a los que se hará referencia del Decreto 092 de 2022 y las modificaciones al Decreto 4886 de 2011 son los siguientes: Artículo 1 que modificó el artículo 1 del Decreto 4886 de 2011; artículo 2 que modificó artículo 2 del decreto 4886 de 2011; artículo 3 que modificó el artículo 3 del decreto 4886 de 2011; artículo 4 que modificó el artículo 9 del decreto 4886 de 2011 y; artículo 5 que modificó el artículo 10 del decreto 4886 de 2011.
2. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0012 Respuesta Requerimiento Supersalud, 25090192--0001200004.pdf, p. 3. "Respecto de su solicitud, es importante destacar que esta Superintendencia viene actuando con mucha rigurosidad hacia las Entidades Promotoras de Salud (en adelante EPS) intervenidas, a fin de que se subsanen cada una de las razones que dieron origen a la medida administrativa, entre ellas su función de aseguramiento (resultados en salud), la cual involucra, entre otros, la dispensación oportuna de TES a sus afiliados, toda vez que, en los últimos tres meses esta causa pasó a ser la principal queja en el SGSSS; sin perjuicio de sus consecuencias como el deterioro de la salud de los pacientes y consecuente aumento de demanda del servicio de urgencia en las Instituciones Prestadoras de Servicios de Salud (en adelante IPS), ya sea por su patología o como mecanismo alterno en la búsqueda de la entrega de sus medicamentos para evitar la interrupción del tratamiento. Por ello, es prudente precisar que la participación de la SNS es de precario acompañamiento en el proceso que se pretende desarrollar para garantizar transparencia y respetar la autonomía e independencia de las personas jurídicas participantes y no vernos inmersos en eventuales causales de incompatibilidad para revisar las conductas de los actores.
Es válido decir que la SNS, al momento de evaluar y/o determinar la decisión de intervenir administrativamente una entidad, realiza diferentes análisis a partir de un enfoque integral que vincula la evaluación financiera con el cumplimiento de los estándares de prestación de servicios, es decir, que, aunque una entidad aseguradora pueda mostrar razonables indicadores en cobertura, un deterioro financiero sostenido representa un riesgo sistémico que impacta negativamente su capacidad para garantizar la continuidad y calidad en la atención. Por ello, la Superintendencia analiza variables técnicas los resultados en salud, y financieras como la liquidez, el patrimonio adecuado y la capacidad de pago para determinar si la situación compromete la garantía del derecho a la salud y, en consecuencia, decide medidas como la toma de posesión o la intervención forzosa administrativa para administrar, de conformidad con los artículos 114 y 115 del Decreto 663 de 1993 - EOSF”.
3. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0000 Solicitud, 25090192-00000002(2).pdf, p. 10.
4. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0000 Solicitud, 25090192-00000002(2).pdf, p. 10 y 25-90192-0011 Respuesta requerimiento EPS, 25090192-0001100004 pdf, p. 10.
5. La solicitud del concepto técnico de viabilidad del acuerdo se realizó con la aplicación analógica del artículo 5 de la Ley 1340 de 2009. En este artículo se hace referencia a los acuerdos establecidos en el parágrafo del artículo 1 de la Ley 155 de 1959 para el sector agropecuario y se establece que "En tal virtud, el Ministerio de Agricultura y Desarrollo Rural deberá emitir concepto previo, vinculante y motivado, en relación con la autorización de acuerdos y convenios que tengan por o bjeto estabilizar ese sector de la economía”.
6. Ley 155 de 1959. Artículo 1, parágrafo.
7. "Autorizar, en los términos de la ley, los acuerdos o convenios que no obstante limitar la libre competencia, tengan por fin defender la estabilidad de un sector básico de la producción de bienes o servicios de interés para la economía general, a los que se refiere el parágrafo del artículo 1o de la Ley 155 de 1959, el artículo 5o de la Ley 1340 de 2009 o demás normas que la modifiquen o adicionen.”
8. Superintendencia de Industria y Comercio. Circular Única. Capítulo VII. Publicada el 19/04/2021.
Consulta en: https://www.sic.gov.co/repositorio-de-normatividad?field tipo de norma value=4&combine=&field numero value=&body value=&fie ldfecha de publicacion value%25255Bvalue%25255D%25255Byear%25255D=2020
9. Decreto 780 de 2016. Artículos 1.2.1.1. al 1.2.1.10. Instituto Nacional de Salud, Instituto Nacional de Vigilancia de Medicamentos y Alimentos, Fondo de Pasivo Social Ferrocarriles Nacionales de Colombia, Fondo de Previsión Social del Congreso de la República, Centro Dermatológico "Federico Lleras Acosta” - ESE, Instituto Nacional de Cancerología ESE, Sanatorio de Agua de Dios - ESE, Sanatorio de Contratación -ESE, Superintendencia Nacional de Salud, Administradora de los Recursos del Sistema General de Seguridad Social en Salud (ADRES).
10. Ibid. Artículo 1.2.2.1. Caja de Previsión Social de Comunicaciones (Caprecom).
11. En concreto, es la que efectúa el reconocimiento y pago de las Unidades de Pago por Capitación (UPC) y demás recursos del aseguramiento obligatorio en salud.
12. Ministerio de Salud y Protección Social. "Evaluación del plan obligatorio de salud de los regímenes Contributivo y subsidiado en el sistema general de seguridad social en salud colombiano y lineamientos para su reforma". Enthoven denomina managed competition, al conjunto de herramientas que define el Estado con el propósito de dirigir u orientar el mercado de manera que se logre subsanar las fallas de mercado inherentes a los mercados de salud y así, lograr simultáneamente eficiencia y equidad.
13. Ley 100 de 1993, artículo 156, literal f.
14. Ley 100 de 1993, artículo 182.
15. Decreto 1652 de 2022. "Artículo 2.10.4.2 Cuotas moderadoras. Las cuotas moderadoras son un aporte en dinero que corresponden al valor que deben cancelar los afiliados cotizantes y sus beneficiarios del Régimen Contributivo por la utilización de los servicios de salud con el objetivo de racionalizar y estimular el buen uso de estos.”
16. Ibid. "Artículo 2.10.4.1 Pagos compartidos o copagos. Los pagos compartidos o copagos son un aporte en dinero que corresponde a una parte del valor del servicio demandado con la finalidad de contribuir a financiar el Sistema y están a cargo de los afiliados beneficiarios en el Régimen Contributivo y de los afiliados del Régimen Subsidiado.
17. Ibid. "Artículo 2.10.4.4 Ingreso base para la aplicación de los pagos compartidos o copagos y cuotas moderadoras. Los pagos compartidos o copagos y cuotas moderadoras se aplicarán teniendo en cuenta el ingreso base de cotización del afiliado cotizante, reportado al momento de la prestación de los servicios de salud y conforme a la progresividad en el nivel socio económico, es decir que a mayor nivel de ingresos del afiliado será mayor el cobro de copago y cuota moderadora y viceversa.”
18. Corte Constitucional. Sentencia T-760 de 2008. Ver al respecto, entre otras, las sentencias T- 484 de 1992; T-505 de 1992 y T-548 de 1992.
19. Superintendencia de Industria y Comercio. INFORME MOTIVADO 21413 DE 2009. Radicado No. 09-021413. Págs. 30 a 31.
20. Ídem.
21. De acuerdo con lo establecido en la Resolución 3100 de 2019 expedida por el MINSALUD, un servicio de salud se define como la unidad básica habilitable del Sistema Único de Habilitación, conformado por procesos, procedimientos, actividades, recursos humanos, físicos, tecnológicos y de información con un alcance definido, que tiene por objeto satisfacer las necesidades en salud en el marco de la seguridad del paciente, y en cualquiera de las fases de la atención en salud (promoción, prevención, diagnóstico, tratamiento, rehabilitación o paliación de la enfermedad).
22. De acuerdo con la definición de la Red Internacional de Agencias de Evaluación de Tecnologías de la Salud, las tecnologías en salud son "cualquier intervención que se puede utilizar para promover la salud, para prevenir, diagnosticar o tratar enfermedades o para rehabilitación o de cuidado a largo plazo. Esto incluye los procedimientos médicos y quirúrgicos usados en la atención médica, los productos farmacéuticos, dispositivos y sistemas organizacionales en los cuidados de la salud".
23. Decreto 780 de 2016. Artículo 2.5.3.4.1.3. Numeral 7.
24. Decreto 780 de 2016. Artículo 2.5.3.4.1.3. Numeral 8.
25. T Londoño, J. L., y Frenk, J. (2011). Pluralismo estructurado: Hacia un modelo innovador para la reforma de los sistemas de salud en América Latina. https://doi.org/10.18235/0012013.
26. La Corte Constitucional analizó la constitucionalidad de estos dos preceptos a través de la Sentencia C-616 de 2001 y declaró la exequibilidad de la norma en relación con la posibilidad de las EPS de prestar directamente los servicios de salud.
27. Ministerio de Salud y Protección Social. "Es un plan de beneficios compuesto por intervenciones de promoción de la salud y gestión del riesgo, las cuales se enmarcan en las estrategias definidas en el Plan Territorial de Salud (PTS), y buscan impactar positivamente los determinantes sociales de la salud y alcanzar los resultados definidos en el PTS. Comprende un conjunto de intervenciones, procedimientos, actividades e insumos definidos en el anexo técnico de la Resolución 518 de 2015, los cuales se ejecutarán de manera complementaria a otros planes de beneficio.” Disponible en: https://www.minsalud.gov.co/salud/publica/Paginas/plan-de-intervenciones-colectivas.aspx.
28. Conjunto integral de atenciones, paquete o canasta, que constituye una modalidad prospectiva mediante la cual se acuerda anticipadamente un valor fijo a reconocer por cada caso atendido, asociado a un evento o conjunto de condiciones de salud relacionadas, que implican la prestación de un paquete definido de servicios y tecnologías.
29. Se pacta una suma global para la atención de un grupo determinado de personas durante un periodo definido, ajustando su valor por el nivel de riesgo en salud y las variaciones en los volúmenes poblacionales proyectados.
30. Consistente en el reconocimiento anticipado de una suma fija por usuario dentro de una población asignada, durante un tiempo determinado, aplicable especialmente a servicios de baja complejidad. Esta modalidad busca incentivar la gestión integral del riesgo y la eficiencia en la utilización de servicios.
31. Modalidad retrospectiva en la que se pacta una suma fija por cada unidad de servicio o tecnología efectivamente suministrada, liquidándose los valores al término de la prestación.
32. Consideraciones tomadas de la Sentencia T-184 de 2024. M.P Vladimir Fernández Andrade.
33. Corte Constitucional, Sentencia T-760 de 2008. M.P. Manuel José Cepeda Espinosa.
34. Corte Constitucional Sentencias T-017 de 2021 M.P. Cristina Pardo Schlesinger, T-117 de 2020 M.P. Gloria Stella Ortiz Delgado, T-402 de 2018 M.P. Diana Fajardo Rivera, T-036 de 2017 M.P. Alejandro Linares Cantillo y T-121 de 2015 M.P. Luis Guillermo Guerrero Pérez.
35. Corte Constitucional, Sentencia T-017 de 2021 M.P. Cristina Pardo Schlesinger.
36. Bloom, D. E., Canning, D., & Sevilla, J. (2004). The effect of health on economic growth: a production function approach. World Development, 32(1), 1-13.https://doi.org/10.1016Zi.worlddev.2003.07.002.
37. Weil, D. N. (2007). Accounting for the effect of health on economic growth. The Quarterly Journal of Economics, 122(3), 1265-1306. https://doi.org/10.1162/qjec.122.3.1265.
38. Banco de la República. (2023). Boletín Económico Regional: Información fiscal territorial 2022. Recuperado de: https://investiga.banrep.gov.co/es/be-1233.
39. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p.p. 16 - 17.
40. Banco de la República. (2024). Aspectos financieros y fiscales del sistema de salud en Colombia. ESPE No. 106. Recuperado de https://investiga.banrep.gov.co/es/espe/espe106.
41. Banco de la República. (2024). Macroeconomic Effects of Healthcare Financing in Colombia. Boletín Económico No. 1278. https://doi.org/10.32468/be.1278.
42. Ídem.
43. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0013 Respuesta Requerimiento Mauricio Camaro, 25090192--0001300004.pdf, p. 2.
44. "Los valores del PIB 2024 y 2025 fueron estimados de acuerdo con las metas de crecimiento de la economía; el gasto en salud con base en las proyecciones presupuestales y el valor de la UPC.” Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0013 Respuesta Requerimiento Mauricio Camaro, 25090192--0001300004.pdf, p. 5.
45. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0013 Respuesta Requerimiento Mauricio Camaro, 25090192--0001300004.pdf, p. 2.
46. "Los valores del PIB 2024 y 2025 fueron estimados de acuerdo con las metas de crecimiento de la economía; el gasto en salud con base en las proyecciones presupuestales y el valor de la UPC.” Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0013 Respuesta Requerimiento Mauricio Camaro, 25090192--0001300004.pdf, p. 5.
47. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0013 Respuesta Requerimiento Mauricio Camaro, 25090192--0001300004.pdf, p. 4.
48. García-Suaza, A., Holguín, C. F., Ríos, J., Rodríguez-Lesmes, P., & Romero-Torres, B. (2023). Radiografía del mercado laboral para los profesionales de la salud (Informe LaboUR No. 14), Universidad del Rosario.
49. Ibidem.
50. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 5.
51. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 6.
52. Ibidem.
53. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 19.
54. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0000 Solicitud, 25090192- 00000002(2).pdf, p. 3.
55. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0012 Respuesta Requerimiento Supersalud, 25090192--0001200004.pdf, p. 7.
56. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0013 Respuesta Requerimiento Mauricio Camaro, 25090192--0001300004.pdf, p. 6.
57. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0012 Respuesta Requerimiento Supersalud, 25090192--0001200004.pdf, p. 3.
58. Radicado No. 25-90192 Sector Salud - SGSS, acumulado 25-234102, 20-234102-0000 presentación, 20-234102-00000003.pdf, pp. 5 - 6.
59. Radicado No. 25-90192 Sector Salud - SGSS, acumulado 25-234102, 20-234102-0000 presentación, 20-234102-00000003.pdf, p. 25
60. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0012 Respuesta Requerimiento Supersalud, 25090192--0001200004.pdf, p. 16.
61. Radicado No. 25-90192 Sector Salud - SGSS, acumulado 25-234102, 20-234102-0000 presentación, 20-234102-00000003.pdf, p. 25
62. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0012 Respuesta Requerimiento Supersalud, 25090192--0001200004.pdf, pp. 12-13.
63. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0012 Respuesta Requerimiento Supersalud, 25090192--0001200004.pdf, p. 13
64. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 43.
65. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0012 Respuesta Requerimiento Supersalud, 25090192--0001200004.pdf, p.p. 13-14.
66. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 12.
67. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 11.
68. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0016 Comunicación Supersalud, 25- 90192-0001600002.pdf, pp. 10 - 11.
69. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0000 Solicitud, 25090192- 00000002(2).pdf, p. 7.
70. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 50.
71. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0016 Comunicación Supersalud, 25- 90192-0001600002.pdf, p. 10.
72. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0016 Comunicación Supersalud, 25- 90192-0001600002.pdf, p. 2.
73. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0016 Comunicación Supersalud, 25- 90192-0001600002.pdf, p. 12.
74. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 19.
75. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 4.
76. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0016 Comunicación Supersalud, 25- 90192-0001600002.pdf, pp. 4 - 5.
77. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0016 Comunicación Supersalud, 25- 90192-0001600002.pdf, p. 5.
78. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 26 y Radicado No. 25-90192 Sector Salud - SGSS, 25-901920012 Respuesta Requerimiento Supersalud, 25090192--0001200004.pdf, p. 14.
79. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 51.
80. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0012 Respuesta Requerimiento Supersalud, 25090192--0001200004.pdf, p.p. 13 - 14.
81. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 45
82. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0016 Comunicación Supersalud, 25- 90192-0001600002.pdf, p. 7.
83. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 10.
84. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0016 Comunicación Supersalud, 25- 90192-0001600002.pdf, p. 9.
85. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0016 Comunicación Supersalud, 25- 90192-0001600002.pdf, p. 9.
86. Decreto 780 de 2016. Artículo 2.5.3.10.5. Formas de prestación del servicio farmacéutico. (...) Parágrafo. Una Institución Prestadora de Servicios de Salud, además de distribuir intrahospitalariamente los medicamentos y dispositivos médicos a sus pacientes hospitalizados, en las mismas instalaciones puede dispensar los medicamentos y dispositivos médicos a sus pacientes ambulatorios, en las condiciones establecidas en el modelo de gestión del servicio farmacéutico.
87. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0012 Respuesta Requerimiento Supersalud, 25090192--0001200004.pdf, p. 14.
88. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0016 Comunicación Supersalud, 25- 90192-0001600002.pdf, pp. 11 - 12.
89. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 12.
90. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0016 Comunicación Supersalud, 25- 90192-0001600002.pdf, pp. 14.
91. Ibidem.
92. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0016 Comunicación Supersalud, 25- 90192-0001600002.pdf, p. 13.
93. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0016 Comunicación Supersalud, 25- 90192-0001600002.pdf, pp. 12.
94. Superintendencia de Industria y Comercio. Circular Única. Títulos VII. Capítulo primero. Numeral 1.4.
95. Superintendencia de Industria y Comercio. Resolución No. 4332 de 2003, p. 2.
96. Ibidem, pp. 2 - 3
97. Ministerio de Comercio, Industria y Turismo. Resolución No. 0908 del 24 de junio de 2002, publicada en el Diario Oficial 44.848.
98. Superintendencia de Industria y Comercio. Resolución No. 4332 de 2003, p. 4.
99. Superintendencia de Industria y Comercio. Resolución No. 4332 de 2003, artículo tercero.
100. Superintendencia de Industria y Comercio. Resolución No. 35696 del 1 de junio de 2012, pp. 2 - 3.
101. Ibidem, pp. 6 - 7
102. Título original de la guía: "Collective procurement of prescription drugs for medical specialist care (MSC)”. Dutch Authority for Consumers and Markets (ACM). Fuente: Strategies in Regulated Markets (SiMR). Clarification is helpful, but not a panacea Evaluation of the ACM guideline collective procurement of drugs. Utretcht, oct. 11/2019.
https://www.acm.nl/sites/default/files/documents/evaluation-acm-guidelines-collective- procurement-of-prescription-drugs-new.pdf
103. Ibidem, p. 3.
104. Ibidem, p. 6.
105. Ibidem.
106. Ibidem, p. 15.
107. Ibidem, p. 4.
108. NFU = Dutch Federation of University Medical Centers, NVZ = Dutch Hospital Association, ZN = The Federation of Health care insurers
109. Ibidem, p. 17.
110. Ibidem, p. 19.
111. Ibidem, p. 22.
112. Zongjun, Ke; Yue,Zhang; Dingqiang, Duan. Effect of centralized volume-basedprocurement of drugs on business performance of listedpharmaceutical enterprises. Faculty of Economics, Wuhan Textile University, Wuhan, 430200, China.
https://www.sciencedirect.com/science/article/pii/S2405844024092296
113. Nation Healthcare Security Administration.
114. Zongjun, Ke; Yue,Zhang; Dingqiang, Duan. Effect of centralized volume-basedprocurement of drugs on business performance of listedpharmaceutical enterprises. Faculty of Economics, Wuhan Textile University, Wuhan, 430200, China.
https://www.sciencedirect.com/science/article/pii/S2405844024092296, pp. 1 y 4
115. Ibidem, pp. 2-3.
116. Ibidem, pp. 1.
117. Ibidem, pp. 1.
118. Ibidem, pp. 2.
119. Ibidem, pp. 2 y 7.
120. Ibidem, pp. 2.
121. Gobierno de México. Plataforma de Compras Consolidadas del Sector Salud. https://compraconsolidada.salud.gob.mx/
122. Ibidem.
123. Gobierno de México. Adquisición Sectorial de Medicamentos e Insumos, feb. 22/2022 https://www.gob.mx/cms/uploads/attachment/file/739138/El Pulso de la Salud 22feb22.pdf
124. Gobierno de México. Plataforma de monitoreo de medicamentos.
https://monitoreocompra.salud.gob.mx/compra/
125. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p.13.
126. Radicado No. 25-90192 Sector Salud - SGSS, acumulado 25-234102, 20-234102-0000 presentación, 20-234102-00000003.pdf, pp. 24 - 25.
127. Ibidem.
128. Radicado No. 25-90192 Sector Salud - SGSS, acumulado 25-234102, 20-234102-0000 presentación, 20-234102-00000003.pdf, p. 24
129. Radicado No. 25-90192 Sector Salud - SGSS, acumulado 25-234102, 20-234102-0000 presentación, 20-234102-00000003.pdf, pp. 24 - 25.
130. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p.15.
131. Ibidem.
132. Ibidem.
133. Radicado No. 25-90192 Sector Salud - SGSS, acumulado 25-234102, 20-234102-0000 presentación, 20-234102-00000003.pdf, p. 24
134. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p.15.
135. Radicado No. 25-90192 Sector Salud - SGSS, acumulado 25-234102, 20-234102-0000 presentación, 20-234102-00000003.pdf, pp. 24 - 25.
136. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0000 Solicitud, 25090192- 00000002(2).pdf, p. 8.
137. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 16
138. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0000 Solicitud, 25090192- 00000002(2).pdf, p. 8.
139. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0000 Solicitud, 25090192- 00000002(2).pdf, p. 8.
140. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 51. "Participación de otras EPS. En la alianza para la negociación de medicamentos para uso exclusivo de los afiliados, está abierta para todas las EPS que operan en el país, sean del régimen contributivo o subsidiado. Condiciones: "(...) Participar en las reuniones fijados por los aliados.”
141. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p.p. 11 y 47. "e) ¿Cómo se tomarán las decisiones dentro del esquema de compra conjunta? ¿Existirá un comité de gestión o un órgano similar, y cómo estará conformado? ¿Cuál será el proceso para la toma de decisiones operativas y estratégicas del acuerdo? Existirán evaluaciones previas de acuerdo con los términos de referencia, las cuales estarán conformadas por las EPS participantes. Las decisiones se tomarán de manera conjunta entre las mismas. Dado que los contratos serán individuales, el único acuerdo conjunto dependerá de la mejor condición técnica y económica que exista entre ellos. Los demás criterios de legalización serán propios de cada EPS.” Y "19. ¿Se contempla alguna revisión periódica o auditoría independiente que evalúe la evolución de los precios, la calidad y el acceso? Durante los tres (3) primeros meses se estima un seguimiento semanal, al inicio del cuarto mes se realizarían evaluaciones quincenales y al inicio del quinto mes se realizaría el seguimiento mensual de manera indefinida mientras se encuentren suscritos los acuerdos de voluntades. Estos seguimientos contemplan una auditoria periódica del costeo y la calidad completa de las diferentes moléculas”
142. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0016 Comunicación Supersalud, 25- 90192-0001600002.pdf, p. 15.
143. Ibidem, p. 3.
144. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 13
145. Ibidem, p. 32
146. Las Intervinientes presentan estas TES en su denominación común internacional (DCI)
147. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p.p. 31
148. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p.p. 31 a 43.
149. Radicado No. 25-90192 Sector Salud - SGSS, 25-90192-0011 Respuesta Requerimiento EPS, 25090192--0001100004.pdf, p. 49
150. Departamento Administrativo de la Función Pública. Concepto 030771 de 2022. https://www.funcionpublica.gov.co/eva/gestornormativo/norma.php?i = 184875
151. Ley 489 de 1998. Artículo 9. Delegación. Las autoridades administrativas, en virtud de lo dispuesto en la Constitución Política y de conformidad con la presente Ley, podrán mediante acto de delegación, transferir el ejercicio de funciones a sus colaboradores o a otras autoridades, con funciones afines o complementarias.
Sin perjuicio de las delegaciones previstas en leyes orgánicas, en todo caso, los ministros, directores de departamento administrativo, superintendentes, representantes legales de organismos y entidades que posean una estructura independiente y autonomía administrativa podrán delegar la atención y decisión de los asuntos a ellos confiados por la ley y los actos orgánicos respectivos, en los empleados públicos de los niveles directivo y asesor vinculados al organismo correspondiente, con el propósito de dar desarrollo a los principios de la función administrativa enunciados en el Artículo 209 de la Constitución Política y en la presente Ley. (Destacado fuera del texto original)
152. Decreto 092 de 2022. Artículo 5. Modificación del artículo 10 del decreto 4886 de 2011. Modifíquese el artículo 10 del Decreto 4886 de 2011, el cual quedará así: Funciones de la Dirección de Cumplimiento. Son funciones de la Dirección de Cumplimiento: 1. Realizar el seguimiento de las garantías aceptadas por parte del Superintendente de Industria y Comercio, dentro de las investigaciones por violación a las normas sobre protección de la competencia y competencia desleal. 2. Realizar la vigilancia de los condicionamientos establecidos por el Superintendente de Industria y Comercio frente a las solicitudes de consolidación, integración, fusión y obtención del control de empresas vigiladas.
153. Ley 489 de 1998. Artículo 10. requisitos de la delegación. En el acto de delegación, que siempre será escrito, se determinará la autoridad delegataria y las funciones o asuntos específicos cuya atención y decisión se transfieren.
154. Ley 489 de 1998. Artículo 11. Funciones que no se pueden delegar. Sin perjuicio de lo que sobre el particular establezcan otras disposiciones, no podrán transferirse mediante delegación: 1. La expedición de reglamentos de carácter general, salvo en los casos expresamente autorizados por la ley. 2. Las funciones, atribuciones y potestades recibidas en virtud de delegación. 3. Las funciones que por su naturaleza o por mandato constitucional o legal no son susceptibles de delegación.
155. Superintendencia de Industria y Comercio. Circular Única. Título VII, capítulo primero. "1.5. Casos en los que no podrá solicitarse autorización para acuerdos o convenios que limiten la libre competencia En ningún caso podrá solicitarse autorización para acuerdos o convenios en proceso o ejecución, ni podrá versar respecto de conductas que sean objeto de investigación, que hayan sido sancionadas o respecto de las cuales haya existido orden de terminación o compromiso de modificación.”
156. Decreto 092 de 2022. Artículo 1. Funciones generales. (...) 57. Solicitar a las personas naturales y jurídicas el suministro de datos, informes, libros y papeles de comercio que se requieran para el correcto ejercicio de sus funciones.
157. Ley 1340 de 2009. Artículo 25. Monto de las multas a personas jurídicas. Por violación de cualquiera de las disposiciones sobre protección de la competencia, incluidas la omisión en acatar en debida forma las solicitudes de información, órdenes e instrucciones que imparta, la obstrucción de las investigaciones, el incumplimiento de las obligaciones de informar una operación de integración empresarial o las derivadas de su aprobación bajo condiciones o de la terminación de una investigación por aceptación de garantías, imponer, por cada violación y a cada infractor, multas a favor de la Superintendencia de Industria y Comercio hasta por la suma de 100.000 salarios mínimos mensuales vigentes o, si resulta ser mayor, hasta por el 150% de la utilidad derivada de la conducta por parte del infractor. (Destacado fuera del texto original)
158. Decreto 092 de 2022. Artículo 5. Funciones de la Dirección de Cumplimiento. Son funciones de la Dirección de Cumplimiento: (...) 9. Apoyar a la Oficina de Servicios al Consumidor y de Apoyo Empresarial en el desarrollo de actividades de divulgación, promoción y capacitación, relacionadas con el fomento y construcción de una cultura de cumplimiento en materia de libre competencia económica.
159. Para más información sobre los programas de cumplimiento, consultar la "Guía de Orientación para el Diseño de Programas de Cumplimiento en Materia de Libre Competencia Económica”. https://sedeelectronica.sic.gov.co/otras/guia-de-orientacion-para-el-diseno-de-programas-de- cumplimiento-en-materia-de-libre-competencia-economica
160. De acuerdo con la comunicación con Radicado No. 25-90192-18, las Intervinientes autorizaron que las comunicaciones y notificaciones de actos administrativos se realicen a un único correo electrónico: jsuarezs@famisanar.com.co


