RESOLUCIÓN 000117 DE 2026
(enero 27)
Diario Oficial No. 53.400 de 16 de febrero de 2026
MINISTERIO DE SALUD Y DE PROTECCIÓN SOCIAL
Por medio de la cual se actualiza el Anexo Técnico 1 de la Resolución 207 de 2024 "Por la cual se adoptan los lineamientos técnicos y operativos para el Programa de Tamiz aje Neonatal"
EL MINISTRO DE SALUD Y PROTECCIÓN SOCIAL
En ejercicio de sus facultades legales, en especial de las conferidas en el numeral 2 del artículo 02 del Decreto Ley 4107 de 2011, numeral 3 del artículo 173 de la Ley 100 de 1993, artículo 12 de la Ley 1438 de 2011, artículo 16 de la Ley 1804 de 2016, y en desarrollo de lo previsto en los artículos 04 y 05 de la Ley 1980 de 2019.
CONSIDERANDO
Que la Constitución Política de 1991 en su artículo 44, establece que son derechos fundamentales de los niños, entre otros, la vida, la integridad física, la salud, la seguridad social y la alimentación equilibrada; disposición que, además consagra la prevalencia de los derechos de los niños sobre los derechos de los demás.
Que, por su parte, la Ley Estatutaria 1751 de 2015 regula el derecho fundamental a la salud y reconoce a los niños, las niñas y los adolescentes como sujetos de especial protección por parte del Estado, contemplando dentro de los principios que lo rigen, el de la progresividad, entendido como la ampliación gradual y continua del acceso a servicios y tecnologías en salud y la reducción gradual y continua de brechas que impidan el goce efectivo del derecho a la salud.
Que la Ley 1438 de 2011 reconoce las enfermedades huérfanas como de especial interés, dado que, por su baja prevalencia en la población y su elevado costo de atención, requieren dentro de! Sistema General de Seguridad Social en Salud, un mecanismo de aseguramiento distinto al previsto para las enfermedades de carácter general; en ese sentido, el artículo 140 de la citada ley, que modificó eí artículo 02 de la Ley 1392 de 2010, establece, "Artículo 2o. Denominación de las enfermedades huérfanas. Las enfermedades huérfanas son aquellas crónicamente debilitantes, graves, que amenazan la vida y con una prevalencia menor de 1 por cada 5.000 personas, comprenden, las enfermedades raras, las ultrahuérfanas y olvidadas. Las enfermedades olvidadas son propias de los países en desarrollo y afectan ordinariamente a la población más pobre y no cuentan con tratamientos eficaces o adecuados y accesibles a la población afectada...".
Que, conforme al marco normativo vigente en materia de atención en salud para las personas que padecen este tipo de patologías, corresponde al Estado implementar las acciones necesarias para garantizar su atención, con el fin de mejorar la calidad y expectativa de vida de quienes las sufren; aspecto relevante si se considera que algunas de las patologías incluidas, o que podrán ser incluidas, en el Programa de Tamizaje Neonatal son consideradas enfermedades huérfanas, cuya detección temprana puede incidir de manera significativa en los resultados en salud de las personas con estas condiciones.
Que el Ministerio de Salud y Protección Social, mediante la Resolución 3280 de 2018, adoptó los lineamientos técnicos y operativos de la Ruta Integral de Atención para la Promoción y Mantenimiento de la Salud y de la Ruta Integra! de Atención en Salud Materno Perinatal, instrumentos operativos de obligatorio cumplimiento por parte de los integrantes del Sistema General de Seguridad Social en Salud, los cuales definen las intervenciones en salud de carácter individual, colectivo y poblacional, así como las acciones de gestión requeridas para la entrega efectiva; que tiene como propósito la identificación temprana y la gestión oportuna de las condiciones en salud que ponen en riesgo la vida de las gestantes y los recién nacidos.
Que la Ley 1980 de 2019, regula y amplía la práctica del tamizaje neonatal en Colombia, creando el Programa de Tamizaje Neonatal a cargo del Ministerio de Salud y Protección Social con apoyo del Instituto Nacional de Salud, requiriéndose en tal sentido, determinar los lineamientos técnicos y operativos que permitan su implementación.
Que este Ministerio, mediante la Resolución 207 de 2024, adoptó los lineamientos técnicos y operativos para el Programa de Tamizaje Neonatal, estableciendo en su anexo técnico las atenciones y tecnologías para la detección temprana de alteraciones mediante tamizaje auditivo, visual, cardiopatías congénitas complejas e hipotiroidismo congénito. No obstante, es necesaria la inclusión de seis (6) nuevas patologías: fenilcetonuria, galactosemia, fibrosis quística, hiperplasia suprarrenal congénita, déficit de biotinidasa y defectos de la hemoglobina, que hacen parte del tamizaje neonatal básico y no se encuentran contempladas en dicho anexo, razón por la cual se requiere su actualización.
Que mediante la Resolución 2764 de 2025, este Ministerio fijó el valor de la Unidad de Pago por Capitación (UPC) para la vigencia 2026, considerando las pruebas de tamizaje neonatal endocrino metabólico básico, incluyendo las pruebas confirmatorias y las atenciones iniciales en salud que se determinan en el presente acto administrativo, conforme a la progresividad y disponibilidad de recursos, según lo dispuesto en la Ley 1980 de 2019. En este orden, la definición de la progresividad de las atenciones de tamizaje neonatal básico quedará reseñada en la Resolución que fije el valor de la UPC cada año.
En mérito de lo expuesto,
RESUELVE
ARTÍCULO 1o. OBJETO. La presente resolución tiene por objeto actualizar el Anexo Técnico 1, mediante el cual se definen los "Lineamientos técnicos y operativos para el Programa de Tamizaje Neonatal", que hace parte integral de la Resolución 207 de 2024, de conformidad con la parte considerativa del presente acto administrativo.
ARTÍCULO 2o. VIGENCIA. La presente resolución rige a partir de la fecha de su expedición.
PUBLÍQUESE Y CÚMPLASE
Dada en Bogotá D.C., a los 27 de Enero de 2026
GUILLERMO ALFONSO JARAMILLO MARTÍNEZ
Ministro de Salud y Protección Social
LINEAMIENTOS TÉCNICOS Y OPERATIVOS PARA EL TAMIZAJE NEONATAL BÁSICO.
Contenido
| 1. | Generalidades |
| 2. | Estructura del Programa de Tamizaje Neonatal |
| 2.1 | Definición |
| 2.2 | Objetivos |
| 2.3. | Población sujeto |
| 3. | Gestión del programa |
| 3.1. | Desarrollo de capacidades y competencias |
| 3.2. | Ampliación y progresividad del programa |
| 3.3. | Consentimiento sustituto informado |
| 3.4. | Regulación de medicamentos y tecnologías en salud |
| 3.5. | Responsabilidad de los actores del SGSSS |
| 3.6. | Monitoreo y seguimiento a los resultados en salud |
| 4. | Líneas de tamizaje |
| 4.1 | Tamizaje endocrino metabólico básico |
| 4.1.1 | Tamizaje de hipotiroidismo congénito |
| 4.1.2 | Tamizaje de fenilcetonuria |
| 4.1.3 | Tamizaje de Galactosemia |
| 4.1.4 | Tamizaje Déficit de Biotinidasa |
| 4.1.5 | Tamizaje para Fibrosis Quística |
| 4.1.6 | Tamizaje de Hiperplasia Suprarrenal Congénita (HSC) |
| 4.1.7 | Tamizaje Defectos de la Hemoglobina |
| 4.2. | Tamizaje neonatal auditivo |
| 4.3. | Tamizaje neonatal visual |
| 4.4. | Tamizaje de cardiopatia congénita |
Bibliografía
Abreviaturas utilizadas
BPN - Bajo Peso al Nacer
CAE - Canal Auditivo Externo
DB - Déficit de Biotinidasa
DH - Defectos de la Hemoglobina
DTS - Direcciones Territoriales de Salud
EAPB - Entidades Administradoras de Planes de Beneficios
EOA - Emisiones Otoacústicas
EIM - Errores Innatos del Metabolismo
FQ - Fibrosis Quística
HPLC - Cromatografía Líquida de Alto Desempeño
HSC - Hiperplasia Suprarrenal Congénita
INS - Instituto Nacional de Salud
INVIMA - Instituto Nacional de Vigilancia de Medicamentos y Alimentos
IPS - Instituciones Prestadoras de Servicios de Salud
17 OHP - 17 Alfa Hidroxiprogesterona
PEAA - Potenciales Evocados Auditivos de Corta Latencia Automatizados
PHE - Fenilalanina
PKU - Fenilcetonuria
RATEA - Respuesta Auditiva del Tronco Encefálico
RELAB - Registro de Laboratorios
RIAMP - Ruta Integral de Atención Materno Perinatal
RPMS - Ruta Integral de Atención para la Promoción y Mantenimiento de la Salud
SIVIGILA - Sistema de Vigilancia en Salud Pública
SGSSS - Sistema General de Seguridad Social en Salud
UPC - Unidad de Pago por Capitación
UPGD - Unidades Primarias Generadoras de Datos
1. Generalidades
El tamizaje neonatal ha sido considerado en el ámbito internacional y nacional como un mecanismo importante de identificación de enfermedades que se presentan en niños aparentemente sanos, con una frecuencia relativamente baja, con posibilidad de ser detectadas en los primeros días u horas de nacimiento con beneficios en la salud y desarrollo de los niños y niñas. (1) Con este propósito, es indispensable garantizar el manejo integral y oportuno que parte de la detección temprana de casos probables, confirmación diagnóstica, inicio del tratamiento o abordaje terapéutico y seguimiento de la condición patológica diagnosticada.
Este programa recoge los avances en el país del tamizaje de hípotiroidismo congénito, las definiciones señaladas en el marco de la Ruta de Atención Integral Materno Perinatal, la Ruta de Promoción y Mantenimiento de la Salud (Resolución 3280 de 2018, modificada por la Resolución 276 de 2019) y otros desarrollos técnicos, normativos y pronunciamientos internacionales relacionados[1] y proyecta la incorporación progresiva de otras condiciones. El programa contempla una plataforma estratégica que permita garantizar el tamizaje neonatal, definiendo responsabilidades de los actores, valorando mecanismos para ampliación y progresividad, orientando técnica y operativamente en relación con las cuatro lineas del tamizaje y avanzando en mecanismos de monitoreo y seguimiento.
Se retoma el principio de progresividad definido en el artículo 6o, inciso 2o, literal g) de la Ley Estatutaria en salud en el que se indica que "(...) el Estado promoverá la correspondiente ampliación gradual y continua del acceso a los servicios y tecnologías de salud, la mejora en su prestación, la ampliación de capacidad instalada del sistema de salud y el mejoramiento del talento humano, así como la reducción gradual y continua de barreras culturales, económicas, geográficas, administrativas y tecnológicas que impidan el goce efectivo del derecho fundamental a la salud"
La carga de enfermedad, discapacidad y mortalidad asociada a las patologías objeto de tamizaje ha sido ampliamente estudiada. El INS reporta en el informe de evento para defectos congénitos, que las malformaciones congénitas afectan a uno de cada 33 bebés en el mundo y causan 3,2 millones de discapacidades al año. De acuerdo con la Organización Mundial de la Salud (OMS), anualmente, aproximadamente 240.000 recién nacidos fallecen en sus primeros 28 días de vida debido a anomalías congénitas. Además, se estima que nueve de cada diez niños que nacen con trastornos congénitos graves residen en países de ingresos bajos o medios reportadas en 2023. En el mismo contexto, cada año, 303.000 recién nacidos mueren durante las primeras cuatro semanas de vida a causa de estas anomalías. Los resultados adversos en el periodo perinatal, relacionados con los defectos congénitos contribuyen a la pérdida de 15 millones de años de vida saludable, resultado de muertes prematuras y discapacidades reportadas en 2023.
Según la información del sistema de vigilancia europea de anomalías congénitas (Eurocat), entre 2014 y 2022, la prevalencia fue de 270,5 por cada 10.000 nacidos vivos. En la región de las Américas, las anomalías congénitas representan aproximadamente el 10% de la mortalidad infantil, siendo la segunda causa después de la prematuridad. Es importante destacar que alrededor de una de cada tres muertes relacionadas con anomalías congénitas se debe a malformaciones del sistema circulatorio reportadas en 2023 (INS, 2024).
Se considera que el Hípotiroidismo Congénito es la causa más frecuente de discapacidad intelectual prevenible en todo el mundo, además de otros trastornos congénitos como la fenilcetonuria.
Los inicios del tamizaje en Colombia están referenciados en la detección de hípotiroidismo congénito (Guía de Práctica Clínica del recién nacido sano) donde se menciona la toma de sangre del segmento placentario del cordón para hemoclasificación, TSH y otras pruebas, y en el planteamiento más amplio definido en Guía de Práctica Clínica para la Detección de anomalías congénitas en el recién nacido (2013). (2) (3)
En esta última, se reseña la importancia de abordar al recién nacido, teniendo en cuenta sus antecedentes familiares y de exposición a teratógenos, examen físico (incluyendo la valoración de respuestas anómalas en la adaptación neonatal); así como la búsqueda de anomalías que no se detectan por examen físico o historia clínica (incluye cardiopatía, auditivo y Errores Innatos del Metabolismo (EIM) con una serie de patologías propuestas a ser tamizadas) y finalmente se abordan aspectos relacionados con la comunicación de los resultados.
La Resolución 3280 de 2018, modificada por la Resolución 276 de 2019, recoge el abordaje del recién nacido en la Ruta Integral de Atención Materno Perinatal, en el marco de la mayoría de procedimientos de atención descritos (respondiendo a una lógica de abordaje del dúo materno fetal) partiendo del cuidado preconcepcional hasta el cuidado del recién nacido, así como la atención para el seguimiento del recién nacido y la valoración integral en la primera infancia (donde se retoma la verificación de realización y resultados del tamizaje neonatal).
El tamizaje neonatal tiene como objetivo último evitar la progresión, secuelas, discapacidad o modificar la calidad o expectativa de vida de los recién nacidos, razón por la cual se considera que debe integrar condiciones metabólicas, endocrinológicas, cardiológicas, auditivas y visuales, teniendo en cuenta la incidencia de estas. En Colombia, según el reporte del INS en el informe de evento la prevalencia nacional de defectos congénitos, con la información preliminar de 2024, es de 253,0 casos por cada 10.000 nacidos vivos donde el 94,3% corresponden a malformaciones congénitas, el 4,7% a defectos metabólicos y el 1,1% a defectos sensoriales. Los desórdenes de la glándula tiroidea representan los defectos metabólicos más frecuentes con una prevalencia de 8,6 casos por cada 10.000 nacidos vivos; la hipoacusia es el defecto sensorial más notificado con una prevalencia de 2,5 casos por cada 10.000 nacidos vivos y de acuerdo con los principales grupos de malformaciones congénitas, los más notificados son las cardiopatías congénitas con una prevalencia para el país de 83,7 casos por cada 10.000 nacidos vivos.[2] (4)
Así, Wilson y Junger (1968) definieron 10 criterios[3] para incluir patologías en la práctica de tamizaje. Dichos criterios, así como otros, son referencia para la inclusión de patologías, por lo que a nivel mundial no existe un consenso único respecto a esto y regiones, países e incluso estados o zonas de un mismo país pueden tener esquemas diferentes de tamizaje[4]. El Colegio Americano de Medicina Genética (2000) en cuanto a los criterios de inclusión de patologías señala como esencial la disponibilidad de una prueba confiable de alta sensibilidad y especificidad y de bajo costo que permita la detección asintomática en los primeros días de vida, con unos beneficios de la detección temprana, la intervención oportuna y el tratamiento eficaz demostrado. En 2008, se realizó una actualización de los criterios de Wilson y Junger para incluir patologías en la práctica de tamizaje; estos criterios son: i) el programa de detección debe responder a una necesidad reconocida; ¡i) los objetivos del cribado deben definirse desde el principio; iii) debe haber una población objetivo definida; iv) debe haber evidencia científica de la efectividad del programa de detección; v) el programa debe integrar educación, pruebas, servicios clínicos y gestión del programa; vi) debe haber garantía de calidad, con mecanismos para minimizar los riesgos potenciales de detección; vii) el programa debe garantizar la elección informada, confidencialidad y respeto por la autonomía; viii) el programa debe promover la equidad y el acceso a la detección para toda la población objetivo; ix) la evaluación del programa debe planificarse desde el principio y x) los beneficios generales de las pruebas de detección deben ser mayores que los daños. (5)
La definición de las patologías a incorporar en un Programa de Tamizaje Neonatal debe valorar aspectos éticos relacionados con el tamizaje tales como consecuencias de falsos positivos(hospitalización con mayor frecuencia que en niños con resultados negativos, además de los riesgos de generar disfuncionalidad en la relación con los padres), así como las derivadas de detectar patologías que tienen significado clínico incierto o que no cuentan con un tratamiento efectivo a largo plazo[5]. Esto debe ser constantemente evaluado por los sistemas de salud de manera que pueda considerarse si se mantiene la detección de dichas patologías. En todo caso, el acompañamiento multidisciplinario a las familias es esencial, no solo por el abordaje de la patología sino también por los niveles de estrés y la reconfiguración de relaciones y redes de apoyo que puede implicar, requiriendo apoyo de psicología y trabajo social.
A un programa de tamizaje universal le corresponde valorar la tecnología de tamizaje, definir lo que se considera un resultado positivo, manejo de los casos positivos (es decir probables), definir la tecnología diagnóstica o confirmatoria, definir los casos en los que se hace necesario repetir la prueba y, para lo que corresponde a patologías endocrino metabólicas, definir los niveles del metabolito en el que se considera debe iniciarse tratamiento en tanto se aclara el diagnóstico, dado el riesgo de deterioro del recién nacido, entre otras.
Para muchos programas de tamizaje endocrino metabólico a nivel mundial, la definición de centralizar el procesamiento de las muestras para tamizaje está basado en consideraciones de costo y de mejoramiento de calidad, asociados al procesamiento de gran cantidad de muestras para condiciones relativamente raras.
Se parte de una práctica del tamizaje de Hipotiroidismo Congénito, con una cobertura según reporte de Repositorio de Tamizaje Neonatal del INS, de aproximadamente 72% con una tasa de rellamado para la toma de muestra para diagnóstico cercano al 50% y sin un seguimiento a los casos diagnosticados, frente a unos programas que en la región alcanzan coberturas de hasta el 99,5%, con inclusión de otras patologías y donde destacan experiencias como la de Uruguay, Costa Rica, Chile y Cuba. (6) (7)
Para dar cumplimiento al objetivo de la Ley de tamizaje neonatal, se debe garantizar que la práctica del tamizaje neonatal se gestione desde la estructura de un programa, en el que a cada niño o niña con un resultado alterado en el tamizaje, se le garantice la realización de pruebas complementarias que permitan descartar o confirmar la presencia de la enfermedad estudiada, y se le brinde la atención integral que requiera de forma oportuna (lo que implica el inicio temprano del tratamiento y el establecimiento del plan de cuidado por parte del profesional definido). En el programa deben quedar claras las responsabilidades de los diferentes actores del sistema frente al tamizaje, el diagnóstico, el tratamiento y el inicio del seguimiento, para cada una de las patologías detectadas por medio del tamizaje. Además, en el que se cuente con los mecanismos necesarios para garantizar la calidad del tamizaje y la información para su monitoreo y seguimiento.
Así mismo, para garantizar que se cuente con información suficiente al momento de avanzar en la inclusión de nuevas patologías, el Programa de Tamizaje Neonatal convocará las mesas de expertos que correspondan.
2. Estructura del Programa de Tamizaje Neonatal
2.1 Definición
Es el conjunto de acciones de gestión y definiciones técnicas y operativas que permiten garantizar la organización, mantenimiento y seguimiento a la operatividad del tamizaje neonatal y a los resultados en salud. Define las orientaciones técnicas para los diferentes actores del sistema de salud involucrados en la atención de los niños y niñas recién nacidos, según sus competencias, acorde con los lineamientos de los organismos internacionales sobre la materia.
La práctica del tamizaje neonatal en el país debe realizarse bajo la estructura de un Programa de Tamizaje Neonatal en los términos que se establecen en los lineamientos técnicos y operativos del presente anexo.
2.2 Objetivos
Objetivo general
Establecer los lineamientos técnicos y operativos para la detección temprana y diagnóstico oportuno de los defectos congénitos, en el marco de la atención integral en salud de los recién nacidos y sus familias.
Objetivos específicos
1. Fortalecer la detección temprana, el diagnóstico, el tratamiento oportuno y el seguimiento a los recién nacidos con defectos congénitos detectables en las primeras horas o días de nacimiento.
2. Gestionar y hacer seguimiento a la atención integral en salud asociadas al tamizaje neonatal y a los resultados en salud establecidos en el programa, en el marco del Sistema General de Seguridad Social en Salud.
3. Orientar, articular y fortalecer las Redes de Prestación de Servicios, Red de Laboratorios e Instituciones de Diagnóstico en sus procesos de registro de información, seguimiento, calidad y desarrollo de capacidades.
4. Fortalecer el proceso de vigilancia en salud pública y gestión de la atención de los defectos congénitos en el marco del programa, tanto en el componente epidemiológico a través del Repositorio de Tamizaje Neonatal de la mano con la información disponible en RELAB.
5. Desarrollar acciones de gestión y de atención en salud que permitan orientar a las familias y otros actores, en los contenidos y especificaciones de la atención relacionada con el tamizaje, para potenciar la acción del sector y mejorar el seguimiento a las condiciones tamizadas.
2.3. Población sujeto
El Programa de Tamizaje Neonatal está dirigido a todos los recién nacidos en el territorio colombiano y a sus familias.
En el marco de la atención materno perinatal (al binomio madre - hijo durante la gestación), se retoma lo planteado en la Ruta de Atención Materno Perinatal para la prevención y detección antenatal de defectos congénitos, asi como las demás definiciones establecidas en las Resoluciones 3280 de 2018 y 276 de 2019, y la normatividad que las modifique.
Resultados en salud
Son aquellos que evidencian el impacto de la gestión y atención integral en salud que se brinda de manera oportuna y con calidad, en desarrollo de las responsabilidades y competencias de los actores del sector salud y con participación activa de las familias de los niños y niñas recién nacidos.
Resultados de Impacto
- Niños y niñas con tratamiento oportuno de patologías objeto de tamizaje neonatal.
- Niños y niñas sin morbilidad evitable.
- Niños y niñas sin mortalidad evitable.
3. Gestión del programa
3.1. Desarrollo de capacidades y competencias.
A partir de lo establecido en la Ley 1164 de 2007, la Resolución 1444 de 2025 por la cual se adopta la Política Pública del Talento Humano en Salud, y demás normatividad vigente, en relación con las competencias y formación del Talento Humano en Salud; el Ministerio de
Salud y Protección Social avanzará en la incorporación de competencias relacionadas con la Atención Integral en la Primera Infancia y el Programa de Tamizaje Neonatal
Este Ministerio, en articulación con las asociaciones científicas, academia, DTS, EAPB e IPS, creará escenarios y procesos de desarrollo de capacidades dirigidos al talento humano en salud que brinda atención materno perinatal en las 4 líneas de tamizaje. El Ministerio en articulación con el INS y en el marco de la resolución, definirán procesos de desarrollo de capacidades y orientación técnica en relación con los procesos vinculados a la toma de muestra, transporte, almacenamiento, procesamiento, entrega de información y disposición de la misma.
3.2. Ampliación y progresividad del programa
Las intervenciones y atenciones definidas en los lineamientos técnicos y operativos del programa retoman lo establecido en la Resolución 3280 de 2018, en cuanto a las atenciones vinculadas al tamizaje neonatal en las cuatro líneas del programa y están garantizadas a la totalidad de la población. De acuerdo con esto, se entiende la progresividad, como la incorporación de nuevas patologías en el programa, así como la incorporación de las atenciones asociadas a las mismas en la Resolución que define procedimientos y tecnologías con cargo a la UPC; lo cual responde a criterios de sostenibilidad, revisión de criterios de inclusión y análisis de los aprendizajes de los programas de tamizaje a nivel mundial.
Este Ministerio será el responsable de liderar la gestión nacional correspondiente al programa, que permita avanzar en términos de integralidad y oportunidad de la atención, así como definir lo correspondiente a la progresividad de la misma; todo ello en articulación con el INS y, en los casos en que se requiera, con participación de las sociedades científicas y la academia.
En este sentido, este Ministerio convocará las mesas de expertos, para retroalimentar y/o validar las propuestas que permitan avanzar en la implementación y/o ampliación del Programa de Tamizaje Neonatal, para los casos en que sea necesario. Los expertos que la integran actuarán como instancia asesora para temas como la definición de patologías a ser incorporadas, tecnologías de tamizaje y diagnóstico, pautas de abordaje y de atención, entre otros. Las mesas de expertos serán convocadas según necesidad. El Ministerio, en articulación con el INS, realizará el seguimiento a los indicadores del programa, así como a su implementación.
Algunas tecnologías en salud pueden cambiar de acuerdo con los avances científicos y tecnológicos, entre ellas las pruebas de tamizaje y diagnósticas; la incorporación de estas se realizará mediante estudios técnicos y financieros que permitan la definición de la financiación y se formalizará mediante actos administrativos y de acuerdo con los servicios y tecnologías financiados por la UPC.
Para el grupo de tamizaje endocrino metabólico, salvo hipotiroidismo congénito, se tendrá en consideración lo expuesto en la Ley 1392 de 2010 que reconoce las enfermedades huérfanas como de especial interés y se adoptan normas tendientes a garantizar la protección por parte del estado colombiano.
3.3. Consentimiento sustituto informado
De conformidad con lo establecido en el artículo 12 de la Ley 1980 de 2019, que define la obligatoriedad del consentimiento informado escrito para el proceso de tamizaje neonatal; el consentimiento sustituto informado para tamizaje neonatal es el documento por medio del cual el representante o representantes legales del niño o niña, acepta de manera libre, voluntaria y consciente, la realización del proceso de tamizaje neonatal por medio de examen físico o tecnologías diagnósticas, tras haber recibido información sobre los beneficios, riesgos y alternativas existentes frente al tamizaje y al diagnóstico de las condiciones a identificar. Es una manifestación de la voluntad sustituta (del recién nacido) y, por lo tanto, frente a la negación de esta por parte de los padres, el profesional de salud debe invocar el interés superior del menor previsto en la convención sobre los derechos del niño y la niña, en el artículo 44 de la Constitución Política y la Ley 1098 de 2006.
Para el tamizaje neonatal el consentimiento podrá ser de tres tipos:
1. Consentimiento informado para tamizaje neonatal por medio de examen físico para el tamizaje visual o de cardiopatía congénita compleja.
2. Consentimiento informado para tamizaje neonatal endocrino-metabólico
a. Toma de muestra de sangre seca en papel filtro para tamizaje neonatal de hipotiroidismo congénito (y las patologías que sean incorporadas en el Programa de Tamizaje Neonatal en esta línea). En el caso de estas patologías, la toma de muestra de sangre de cordón umbilical debe ser realizada en todo caso, si el procedimiento así lo establece.
b. Toma de muestra de sangre periférica.
3. Consentimiento informado para tamizaje neonatal por medio de tecnologías diagnósticas diferentes a análisis de muestra de sangre.
El consentimiento sustituto informado implica en todo caso, un proceso de información adaptado a la autonomía progresiva y contextual de la persona mayor que brindará dicho consentimiento, independiente de la capacidad intelectual de la persona. Para el caso de personas menores de 14 años, el representante legal corresponde a la persona que asume dicho rol para los procedimientos de atención del parto.
El consentimiento sustituto informado se podrá realizar dentro de cualquiera de las siguientes atenciones: (i) última cita de control prenatal, (i¡) al ingreso de la hospitalización por atención del parto o cesárea, (iii) durante las primeras 24 horas de hospitalización post parto.
Para la realización de la toma de la muestra de sangre periférica o del procedimiento de evaluación por medio de tecnología diagnóstica diferente al análisis de muestra de sangre se podrá gestionar el consentimiento sustituto informado a los padres previo a la toma del tamizaje.
El proceso de información para la comprensión adecuada del consentimiento y su firma estará siempre a cargo del profesional de medicina, profesional de pediatría o profesional de neonatología que atiende al o a la recién nacido (a), que da la información a la madre, o al representante legal del niño o niña.
La historia clínica es un documento obligatorio y privado que debe ser garantizado desde el nacimiento de la persona como sujeto de derecho. Teniendo en cuenta esta consideración, se debe garantizar el registro en la historia clínica propia del o de la recién nacido (a), para consignar todos los datos correspondientes a la atención de este y hacer seguimiento a los resultados del tamizaje neonatal. En caso de que se realice en el contexto de la atención a la mujer gestante, se consignará en la historia clínica de la misma.
El consentimiento informado sustituto debe contener como mínimo la siguiente información: nombre completo e identificación de la madre del recién nacido, nombre del procedimiento y tecnología que se implementa para el tamizaje, patologías o línea de tamizaje asociada, ventajas para la detección del riesgo de morbilidad, discapacidad o muerte; posibles complicaciones que se pueden asociar al procedimiento en un lenguaje claro y sencillo[6], firma de uno de los padres o de la persona responsable del o de la recién nacido (a), donde afirma que entiende lo explicado y acepta el procedimiento, firma del profesional de salud que brinda la información del consentimiento informado.
En consideración de su carácter de consentimiento sustituto, en el caso que tras recibir la información de forma clara, objetiva y suficiente, y en comprensión de las implicaciones de la intervención de tamizaje, la persona representante o representantes legales del niño o niña, no acepte la realización del tamizaje, se actuará en garantía al interés superior del niño o niña y en reconocimiento de los límites del consentimiento sustituto; en consecuencia, el profesional de medicina realizará el tamizaje, tras dejar registro en la historia clínica del proceso de información brindado, la manifestación de disentimiento y, finalmente, la decisión de realización del tamizaje teniendo en cuenta el interés superior del niño o niña.
Es responsabilidad de las EAPB y de las IPS el desarrollo de escenarios y mecanismos de información continua durante la preconcepción, gestación, parto y puerperio, destinado a las familias. Como parte del proceso de información sobre el tamizaje neonatal y sus responsables, este Ministerio en articulación con otros actores dispondrá de información relacionada en su página web y a través de otros mecanismos.
- Consulta Básica de Orientación Familiar
En el marco de la Resolución 3280 de 2018, es importante identificar que además del recién nacido, la familia es reconocida como sujeto de atención, perspectiva que es estratégica en este momento en el que las familias vivencian un suceso vital que implica nuevas acomodaciones, que en algunos casos y de acuerdo con las condiciones y particularidades de cada una requiere orientaciones desde los servicios de salud. Los programas de tamízale neonatal deben garantizar el acceso equitativo y universal de todos los recién nacidos con la correcta información a los padres para la toma de decisiones.
Para ello, se cuenta con la consulta básica de orientación familiar, en el marco de lo indicado en la Resolución 3280 de 2018, desde la cual se comprende a la familia como sujeto y fin en sí misma de la atención en salud, resultando ser una acción estratégica para la garantía de la integralidad de la atención en la medida que se constituye en una ventana de oportunidad para fortalecerla como entorno protector, clave en el proceso del recién nacido. Si bien la atención en salud a las familias se brinda en todos los momentos del curso de vida, es importante para este proceso dado el suceso vital por el que atraviesa la familia, contar con la Atención Básica de Orientación Familiar realizada por medicina o medicina familiar, psicología, trabajo social o enfermería, como herramienta que logra profundizar en el reconocimiento de la dinámica familiar con incidencia en la salud.
Específicamente esta atención está definida para las familias con situaciones o condiciones de riesgo medio para la salud, identificadas en las intervenciones/atenciones en salud individuales (además de aquellas canalizadas por el Plan de Intervenciones Colectivas (PIC) y las que consulten de manera espontánea) Es importante de manera permanente promover acciones de educación para el fortalecimiento y promoción de la salud familiar, basado en el desarrollo de capacidades, como acción que brindará elementos para sostener la familia como red de cuidado principal del recién nacido.
Sin detrimento de la garantía de esta atención; debe mantenerse un acompañamiento a las familias de recién nacidos con tamizaje positivo e informar adecuadamente el significado de las pruebas de tamizaje y en caso de descartarse la patología, debe ser claro que el niño o niña no presentan alteración. En caso de confirmación, orientar las posibilidades terapéuticas, los riesgos, signos de alarma y las prácticas de cuidado.
3.4. Regulación de medicamentos y tecnologías en salud
El Ministerio de Salud y Protección Social, en conjunto con el Instituto Nacional de Salud y el Instituto Nacional de Vigilancia de Medicamentos y Alimentos (INVIMA), en el marco de las competencias de cada entidad, definirá los mecanismos que favorezcan el acceso equitativo a medicamentos y tecnologías en el marco del programa, especialmente en lo concerniente a las patologías del tamizaje endocrino metabólico, así como la financiación de estos.
3.5. Responsabilidad de los actores del SGSSS
En el marco de sus competencias y funciones, y para garantizar la implementación del Programa de Tamizaje Neonatal, son responsabilidades de los actores del SGSSS las siguientes:
- Superintendencia Nacional de Salud
La Superintendencia Nacional de Salud es la encargada de la inspección, vigilancia y control de los actores del SGSSS y en este marco de las atenciones establecidas con cargo a la UPC o con Presupuestos Máximos y de aquellas que se encuentren en progresividad, según la normativa vigente. Este proceso será articulado con las acciones de seguimiento desarrolladas por las entidades territoriales y se acompaña desde el Ministerio de Salud y Protección Social, en el marco de la gestión y seguimiento al Programa de Tamizaje Neonatal, en conjunto con el INS. Se articulará la opinión de los pacientes por medio de las mesas nacionales ya instauradas como son la Mesa Nacional de Enfermedades Huérfanas.
- Instituto Nacional de Salud
Orientar y avanzar en el seguimiento de los defectos congénitos, articulado con las acciones de gestión de los otros actores del SGSSS, de acuerdo con lo establecido en el Protocolo de Vigilancia en Salud Pública señalada por el INS.
Además, actuará como Centro Nacional Coordinador del Tamizaje Neonatal para lo que corresponde al Tamizaje Endocrino Metabólico, desarrollando los lineamientos o las directrices necesarias para su funcionamiento y garantía relacionado con las funciones de los laboratorios en el contexto de la Red Nacional de Laboratorios y en el marco de sus competencias, con asesoría de las mesas de expertos que sean convocadas para la implementación y ampliación del Programa de Tamizaje Neonatal.
- Entidades Territoriales
Los Departamentos y Distritos deben realizar los procesos de gestión en sus territorios los cuales incluyen hacer seguimiento a los resultados en salud en el marco de la implementación del Programa de Tamizaje Neonatal, promover los procesos de desarrollo de capacidades y fortalecer la vigilancia en salud pública. En articulación con las EAPB, deben hacer el seguimiento de las intervenciones individuales según normatividad vigente y en desarrollo de sus funciones de inspección y vigilancia en articulación con la Superintendencia Nacional de Salud.
Las entidades territoriales de orden departamental y municipal deben cumplir y hacer cumplir, de acuerdo con su jurisdicción, los lineamientos establecidos en el Sistema de Vigilancia en Salud Pública, de acuerdo con lo establecido por el INS.
- Entidades Administradoras de Planes de Beneficios
Garantizar con su red de prestación de servicios, la realización del tamizaje neonatal a todos los recién nacidos hijos de las madres afiliadas, así como atenciones definidas en el marco de la Ruta Integral de Atención en Salud Materno Perinatal y Ruta de Promoción y Mantenimiento de la Salud para la Primera Infancia (incluyendo las atenciones en progresividad).
Vigilar y hacer seguimiento a los casos probables y el ajuste de caso correspondiente (especialmente en los casos en los que la Unidades Primarias Generadoras de Datos no desarrollen la prueba diagnóstica); así como toda la gestión requerida en el marco del programa (lo cual implica gestionar la confirmación de los casos probables, ajustes de red, gestión expedita para casos probables, entre otras). En tanto sea detectado un riesgo deberá brindarse la atención según criterio del profesional y teniendo en cuenta las consideraciones señaladas en la presente resolución. Las EAPB que incorporen otras patologías en el marco de sus programas de tamizaje neonatal deberán garantizar la atención integral relacionada con las mismas.
Garantizar que se realice el rellamado o recitación de los recién nacidos considerados casos probables por tamizaje positivo y de aquellos casos en los que se considere se debe practicar retamizaje de manera inmediata, para lo cual debe tener un seguimiento de cohortes que permita ubicar desde la base de sus recién nacidos, aquellos que son notificados en el SIVIGILA y Repositorio de Tamizaje Neonatal como casos probables.
Gestionar la realización de la prueba diagnóstica, así como el reporte de su resultado, hacer seguimiento para garantizar el inicio temprano del tratamiento y, finalmente, gestionar el seguimiento pertinente. Para ello deberán activar los mecanismos que correspondan con su red de prestación de servicios (incluidos de manera especial los laboratorios e IPS que brindan las tecnologías de tamizaje y diagnóstico auditivo; así como las que garantizan tamizaje y diagnóstico endocrino metabólico) y fortalecer el reporte a las fuentes establecidas por normatividad.
Garantizar, a través de su red, la integralidad, disponibilidad, suficiencia y modalidad de prestación de servicios que se requiere para la calidad y especialmente la oportunidad de la atención en relación con el tamizaje neonatal. Es necesario, específicamente para los casos de tamizaje endocrino metabólico, se garantice la aplicación de las pruebas de tamizaje, pruebas diagnósticas o en caso de requerir tecnologías con baja disponibilidad en el área, se incorpore en la red lo necesario para gestionar de manera oportuna la realización de la prueba diagnóstica y su reporte; sin que medien barreras administrativas y en los casos que corresponda incorporando esto en los mecanismos de contratación con los laboratorios e IPS.
Realizar monitoreo y seguimiento del Programa de Tamizaje Neonatal y de los resultados de salud e indicadores, incorporar las orientaciones del programa en los procesos de desarrollo de capacidades al recurso humano en salud, en articulación con su red de prestación de servicios. Las EAPB deben cumplir con los lineamientos establecidos en el Sistema de Vigilancia en Salud Pública, de acuerdo con lo establecido por el INS.
- Instituciones Prestadoras de Servicios Salud
Garantizar a los usuarios el acceso efectivo y con calidad a los servicios y tecnologías en salud definidas en el Programa de Tamizaje Neonatal.
Cumplir las directrices y lineamientos vigentes para la atención de gestantes y recién nacidos, incluyendo la estancia hospitalaria de mínimo 24 horas posteriores al nacimiento, en el marco de lo establecido en Resolución 3280 de 2018, la Resolución 276 de 2019 y la norma que la modifique o sustituya.
Definir en el marco de la implementación del Programa de Tamizaje Neonatal, la planeación y ejecución de procesos de desarrollo de capacidades, verificación de la adherencia del talento humano a los lineamientos y calidad del dato, seguimiento a la oportunidad de las atenciones, valoración de percepción de los usuarios y barreras de acceso; así como la revisión de lo relacionado con dotación, equipamiento y capacidad instalada
En su función como Unidades Primarias Generadoras de Datos (UPGD) deben realizar la detección y notificación de casos probables, registrando la información en el Sistema de Vigilancia en Salud Pública - SIVIGILA y generar las alertas que correspondan al asegurador. Así mismo, la IPS deberá reportar en las fuentes de información que sean definidas, la aplicación del tamizaje, así como del resultado de este.
Las IPS deben cumplir con los lineamientos establecidos en el Sistema de Vigilancia en Salud Pública, de acuerdo con lo establecido por el INS.
- Laboratorios
Los laboratorios que realicen tamizaje neonatal endocrino metabólico deberán cumplir con los estándares de calidad en salud pública establecidos en la Resolución 1619 del 2015 o la norma vigente para tal fin, y con la inscripción en el Registro de Laboratorios (RELAB) establecido en la Resolución 561 de 2019 o el aplicativo que lo modifique o sustituya y con los procesos de habilitación como servicio de salud, según la normatividad vigente. Además, deberán participar en los procesos de evaluación del desempeño definidos por el INS y los relacionados con mejoramiento de procesos de calidad; que permitan avanzar hacia la acreditación de las pruebas de tamizaje por parte del Organismo Nacional de Acreditación de Colombia (ONAC) bajo la norma ISO/IEC 15189 o por un organismo de acreditación que sea signatario de los acuerdos de reconocimiento multilateral suscritos por ONAC, bajo el mismo alcance, deberán acreditar las pruebas empleadas para el tamizaje de la patología, en un plazo máximo de 2 años a partir del momento en el que sea incluida la patología y específicamente la tecnología de tamizaje en el Programa. El INS definirá, en articulación con la Dirección de Epidemiología y Demografía de este Ministerio y en el marco del programa, el acompañamiento y seguimiento a este proceso.
Todo laboratorio que realice pruebas de tamizaje neonatal o pruebas confirmatorias debe ingresar los resultados de las pruebas de manera simultánea a la emisión de los mismos, al Repositorio de Tamizaje Neonatal del Instituto Nacional de Salud, garantizando que dicho reporte cumpla todos los criterios de calidad de la información; así como realizar el reporte que corresponda según la normatividad vigente que tenga relación con el Programa de Tamizaje Neonatal.
3.6. Monitoreo y seguimiento a los resultados en salud
Los obligados al cumplimiento de esta resolución realizarán, en el marco de sus competencias, el monitoreo de las intervenciones de las rutas a que alude el presente acto administrativo y la evaluación de los resultados en salud y reducción de las inequidades en salud en las personas, familias y comunidades, derivadas de su implementación.
El seguimiento y monitoreo del Programa de Tamizaje Neonatal se realizará a partir de fuentes de información disponibles y oficiales.
- SIVIGILA.
- Resolución 202 de 2021.
- Registros Individuales de Prestación de Servicios de Salud (RIPS).
- Registro de enfermedades huérfanas (en tanto sean incluidas patologías que estén incluidas en el listado actualizado de enfermedades huérfanas).
- Información de prestaciones de servicios de salud en el marco del cálculo de la Unidad de Pago por Capitación (UPC) y mecanismos de ajuste de riesgo.
- Programas de Evaluación del Desempeño (INS).
- Repositorio de Tamizaje Neonatal (INS).
- Las que sean definidas según normatividad.
3.6.1 Indicadores Programa de Tamizaje Neonatal
El Programa de Tamizaje Neonatal, define los siguientes indicadores como parte del seguimiento y monitoreo:
Tabla 1. Resultados e Indicadores del Programa de Tamizaje Neonatal
| Línea de tamizaje neonatal | Indicadores Tamizaje |
| Tamizaje Endocrino metabólico | - Cobertura de tamizaje de hipotiroidismo congénito.- Oportunidad del tamizaje para hipotiroidismo congénito.- Proporción de niñas y niños con probable hipotiroidismo congénito por TSH.- Proporción de niñas y niños con diagnóstico de hipotiroidismo congénito.- Cobertura de tamizaje de fenilcetonuria.- Oportunidad del tamizaje para fenilcetonuria.- Proporción de niñas v niños con probable fenilcetonuria.- Proporción de niñas v niños con fenilcetonuria- Cobertura de tamizaje de galactosemia.- Oportunidad del tamizaje para galactosemia.- Proporción de niñas v niños con probable galactosemia.- Proporción de niñas v niños con diagnóstico de galactosemia.- Cobertura de tamizaje de fibrosis quística.- Oportunidad del tamizaje para fibrosis quística.- Proporción de niñas y niños con probable fibrosis quística.- Proporción de niñas y niños con diagnóstico de fibrosis quística.- Cobertura de tamizaje de déficit de biotinidasa.- Oportunidad del tamizaje para déficit de biotinidasa- Proporción de niñas y niños con probable déficit de biotinidasa.- Proporción de niñas v niños con diagnóstico de déficit de biotinidasa.- Cobertura de tamizaje de hiperplasia suprarrenal congénita.- Oportunidad del tamizaje para hiperplasia suprarrenal congénita.- Proporción de niñas y niños con probable hiperplasia suprarrenal congénita.- Proporción de niñas y niños con diagnóstico de hiperplasia suprarrenal congénita.- Cobertura de tamizaje para defectos de hemoglobina.- Oportunidad del tamizaje para defectos de hemoglobina.- Proporción de niñas y niños con probables defectos de hemoglobina.- Proporción de niñas v niños con diagnóstico de defectos de hemoglobina. |
| Tamizaje Auditivo | - Cobertura de tamizaje auditivo.- Oportunidad del tamizaje auditivo.- Proporción de niñas y niños con probable alteración auditiva congénita.- Oportunidad en el diagnóstico de hipoacusia o sordera congénita.- Cobertura de niñas y niños con hipoacusia o sordera congénita atendidos por especialista. |
| Tamizaje Visual | - Cobertura de tamizaje visual.- Proporción de niñas y niños con probable alteración visual congénita.- Cobertura de niñas y niños con probable alteración visual congénita atendidos por especialista. |
| Tamizaje de Cardiopatía Congénita Compleja | - Cobertura de tamizaje de cardiopatía congénita compleja.- Proporción de niñas y niños con probable cardiopatía congénita compleja.- Cobertura de niñas y niños probable cardiopatía congénita compleja atendidos por especialista.- Oportunidad de atención por especialista en los casos de probable cardiopatía congénita compleja. |
Las fichas técnicas de los indicadores estarán disponibles en la página web del Ministerio de Salud y Protección Social.
4. Líneas de tamizaje
Líneas del Programa de Tamizaje Neonatal.
Partiendo de distintas consideraciones éticas, clínicas, epidemiológicas y económicas, en el marco del programa se reconocen las siguientes líneas de tamizaje: Endocrino Metabólico (incluye el tamizaje básico y ampliado), Visual, Auditivo y Cardiopatía Congénita Compleja.

Definiciones
- Tamizaje neonatal. Atención en salud dirigida a la detección temprana de recién nacidos con enfermedades que pueden producir mortalidad evitable, discapacidad, morbilidad significativa o grave afectación de la calidad de vida, susceptibles de ser identificadas a través de tecnologías de alta sensibilidad durante las primeras horas o días de nacimiento, con el objeto de ser confirmadas, brindarles tratamiento de manera oportuna y el seguimiento necesario para mejorar sus resultados en salud y desarrollo.
- Tamizaje neonatal básico. Incluye pruebas para hipotiroidismo congénito, fenilcetonuria, galactosemia, fibrosis quística, hiperplasia suprarrenal congénita, déficit de biotinidasa o defectos de la hemoglobina.
- Tamizaje ampliado. Incluye las anteriores pruebas más las pruebas para desórdenes de los aminoácidos, desórdenes de los ácidos orgánicos y desórdenes de la oxidación de los ácidos grasos.
- Tamizaje endocrino metabólico. Se define como la detección de casos probables de patologías endocrino-metabólicas que se detectan por pruebas en sangre, con las consideraciones de tiempo, muestra y tecnología de tamizaje correspondiente.
- Tamizaje neonatal auditivo. Corresponde a la detección de recién nacidos con alteraciones auditivas que pueden llevar a hipoacusia, afectar su capacidad auditiva y de esta forma, amenazar el desarrollo integral del niño o la niña en el curso de la vida.
- Tamizaje neonatal visual. Corresponde a la detección de recién nacidos con alteraciones al examen físico que permitan detectar posibles patologías oculares o visuales que pueden llevar a ceguera, afectar la capacidad visual y de esta forma, amenazar el desarrollo integral del niño o la niña en el curso de la vida.
- Tamizaje de cardiopatía congénita. Corresponde a la detección de cardiopatía congénita compleja asociada a altas tasas de mortalidad, por medio de la saturación de oxígeno (pulsooximetría) pre y postductal.
4.1 Tamizaje endocrino metabólico básico
Esta línea de tamizaje incluye las condiciones endocrino-metabólicas: hipotiroidismo congénito, fenilcetonuria, galactosemia, fibrosis quística, hiperplasia suprarrenal congénita, déficit de biotinidasa o defectos de la hemoglobina, así como las enfermedades de los aminoácidos, de los ácidos orgánicos o los desórdenes de la beta oxidación de los ácidos grasos. Incorpora el tamizaje básico como el ampliado, siguiendo lo indicado por la Ley 1980 de 2019, en términos de la progresividad y de acuerdo a la disponibilidad de recursos el Gobierno Nacional definirá las pruebas a incluirse en el Programa de Tamizaje Neonatal, el cual como mínimo garantizará como punto de partida las correspondiente al tamizaje neonatal básico, hasta lograr el tamizaje ampliado.
Si bien la Resolución 3280 de 2018 menciona la técnica a utilizar para la toma de la muestra de sangre del cordón o periférico, las consideraciones de acuerdo a los factores de riesgo materno, perinatales o neonatales y a los tiempos ideales de toma; era necesario ahondar mucho más en cada una de las líneas expuestas. La citada Resolución 3280 expone como nota lo siguiente: "En el momento en que se formule el programa de tamizaje neonatal o se den directrices sobre la atención integral en salud para la identificación de riesgo metabólico, cardiovascular, auditivo y visual en el recién nacido (que incluye tamizaje de errores innatos del metabolismo), se realizarán consideraciones respecto a la toma de la muestra para tamizaje de hipotiroidismo congénito y las demás pruebas de tamizaje en sangre".
Por las características de las patologías de la línea endocrino metabólico básico, se tuvieron en cuenta las siguientes consideraciones de acuerdo con mesas de trabajo con expertos, protocolos y guías de manejo internacionales relacionadas con el tamizaje básico:
- Tecnologías requeridas para el tamizaje y la confirmación diagnóstica.
- Inclusión de un componente preanalítico, analítico y postanalítico donde se definen los puntos de corte para las siete patologías de la línea endocrino metabólico básico: hipotiroidismo congénito, fenilcetonuria, galactosemia, fibrosis quística, hiperplasia suprarrenal congénita, déficit de biotinidasa y defectos de la hemoglobina.
- Definición de tiempos ideales y máximos para la toma de muestra de talón.
- Situaciones en las que se requiere un retamizaje.
- Perfiles y atenciones definidas para establecer el plan de cuidado y garantizar el tratamiento oportuno.
A continuación, se describe ampliamente cada uno de los elementos de los componentes preanalítico, analítico y postanalítico, y se especificarán en los apartados de cada patología del tamizaje neonatal básico.
Componente preanalítico
- Enfoque antenatal de riesgo y realización de la historia clínica
Exige la realización de una historia clínica dirigida a la identificación de factores de riesgo prenatales, perinatales y neonatales, según lo relacionado en la Ruta Integral de Atención en Salud para la población materno perinatal. En este caso se deberá indagar por el antecedente familiar de cada una de las patologías que se tamizan en el país, pero también por cualquier antecedente de patología congénita que exista en la familia. Como menciona la Resolución 3280 del 2018, la historia clínica perinatal debe empezar a realizarse desde antes del nacimiento, con el fin de preparar el equipo y los insumos necesarios para la atención adecuada en sala de partos/nacimientos y programar las actividades a realizar en las horas posteriores al nacimiento.
Es necesario reiterar en todo caso, que el tamizaje es una medida universal y todos los recién nacidos deben recibir esta atención.
- Información y comunicación sobre tamizaje neonatal
Se deben desarrollar diferentes estrategias de información y comunicación para promover el programa y la práctica del tamizaje neonatal en el país y deben ser dirigidos a todos los actores con responsabilidades en el programa, incluyendo madres, padres, familias y comunidad en general. Se deben brindar teniendo en cuenta las intervenciones poblacionales, colectivas e individuales que han sido contempladas y que se desarrollan a partir de lo dispuesto en la Resolución 3280 de 2018 o la norma que la modifique o la sustituya. Esto quiere decir que se pueden desarrollar piezas comunicativas o audiovisuales sobre la práctica y el Programa de Tamizaje Neonatal; implica reconocer la importancia del tamizaje neonatal, el reconocimiento de los resultados del tamizaje neonatal durante la consulta de seguimiento del recién nacido y las consultas de valoración integral en salud de la primera infancia, la importancia del tratamiento oportuno y el seguimiento integral. Así mismo, es fundamental promover y brindar educación sobre el tamízale neonatal durante la atención para el cuidado prenatal y la atención del parto.
- Consentimiento sustituto informado
De conformidad con lo establecido en la Ley 1980 de 2019, se establece la obligatoriedad del consentimiento sustituto informado para tamizaje neonatal posterior a recibir información sobre los beneficios, riesgos y alternativas existentes frente al tamizaje y diagnóstico de las patologías.
Se debe realizar el abordaje familiar, explicando en que consiste la toma del tamizaje neonatal básico, porqué la toma de este examen debe ser universal y obligatoria para todos los recién nacido en el país, qué es el Programa de Tamizaje Neonatal y de los pasos de cada una de las etapas contempladas para el rellamado y la entrega de resultados.
En marco de la Resolución 207 de 2024, el consentimiento sustituto informado para tamizaje neonatal endocrino metabólico involucra la toma de muestra de sangre de talón en papel filtro, y la toma de muestras de sangre periférica para la confirmación diagnóstica de las patologías objeto de esta resolución. El proceso de información brindado a la familia debe ser registrado en la historia clínica, así como la decisión de realización del tamizaje.
El consentimiento informado debe ser adecuadamente explicado a los padres o cuidadores antes de tomar la muestra. Debe explicar a detalle en que consiste el tamizaje neonatal básico, en términos sencillos, cuáles y el tipo de enfermedades, para que la familia tenga claro el alcance de la prueba.
El talento humano en salud debe hacer la descripción del procedimiento de la toma de la muestra en sangre de talón del recién nacido, dar a conocer el manejo que se le va a dar a la muestra y los posibles resultados, con las implicaciones de acuerdo a un resultado positivo o negativo. Se debe indicar el proceso de atención en salud integral a seguir y el compromiso en el acompañamiento en caso de que sea un resultado positivo, así como el impacto en el beneficio al recién nacido de una detección e inicio de tratamiento oportuno. Reconociendo que es un procedimiento seguro, mínimamente invasivo y con bajo riesgo de complicación.
La información en salud brindada a la familia respecto al tamizaje hace parte de la atención en el marco del programa y debe ser registrada (puede ser directamente en la historia clínica) y debe incluir la importancia del tamizaje reconociendo que es una práctica segura, mínimamente invasiva, con bajo riesgo de complicaciones que genera un dolor mínimo y de corta duración cuando se realiza con la técnica correcta; así mismo, debe lograrse que la familia comprenda la importancia de regresar en los tiempos establecidos a verificar los resultados lo que garantice que se descarte la patología o se pueda dar el inicio de tratamiento, retamizaje o pruebas confirmatorias requeridas de manera temprana, explicando que esto mejorará de manera significativa la evolución de la enfermedad, disminuyendo el riesgo de secuelas a corto y largo plazo; la información debe ser clara, suficiente y comprensible para lo cual debe realizarse la adecuación sociocultural necesaria.
- Toma de muestra de sangre mediante punción capilar de talón y recolección en papel filtro
- Las recomendaciones para la toma de muestra de sangre de cordón umbilical, quedan referenciadas en el apartado de hipotiroidismo congénito.
La toma de la muestra de tamizaje neonatal endocrino metabólico básico debe realizarse mediante punción capilar de talón idealmente entre las 48 y 72 horas de vida (una muestra en papel filtro para procesar las pruebas de las 7 patologías), intervalo que permite un equilibrio entre la maduración metabólica del recién nacido y la posibilidad de detectar oportunamente enfermedades graves y tratables.
En el caso de los recién nacidos que nacen por parto vía vaginal, a los cuales no se les pueda garantizar la toma de la muestra entre las 48 a 72 horas o en el marco de la consulta de seguimiento del recién nacido, se podrá tomar la muestra de sangre de talón si se cumplen las siguientes condiciones: mínimo 24 horas del nacimiento y tres tomas completas de alimentación; considerando en todo caso, que se pueden presentar un mayor porcentaje de falsos positivos o falsos negativos en los resultados del tamizaje de acuerdo a cada patología. Podrán gestionarse mecanismos de albergue o transporte que permitan garantizar la toma de la muestra en los tiempos adecuados y a su vez las consultas de seguimiento al recién nacido y de la mujer en el puerperio. En los casos en los que se tome antes de las 48 horas, deberá registrarse en la historia clínica, las razones por las cuales no se garantiza la toma de muestra en los tiempos definidos.
Garantizar la toma de la muestra entre las 48 y 72 horas de vida tiene un alto impacto en los recién nacidos y sus familias, así como en costos y atenciones asociadas al Programa de Tamizaje Neonatal. Se establece como límite superior admisible las 120 horas (5 días) para la toma y procesamiento de la muestra de sangre de talón.
Es imprescindible que, antes de la toma de la muestra en talón, el recién nacido haya recibido al menos tres tomas completas, idealmente con leche materna, fórmulas que contengan proteínas intactas y lactosa, ya que una o dos alimentaciones pueden ser insuficientes para permitir la acumulación detectable de metabolitos como la fenilalanina o la galactosa, lo que conlleva riesgo de falsos negativos. Este criterio está respaldado por el Newborn Blood Spot Screening Handbook del Reino Unido (8), y por el New South Wales Newborn Screening Program de Australia (9), que considera inadecuada cualquier muestra tomada antes de tres tomas alimentarías. Aunque no todas las guías norman esta cifra con precisión, su adopción como estándar clínico operativo permite mejorar la calidad del programa, asegurar una interpretación más confiable v justificar, si es necesario, la repetición de la muestra en contextos de alimentación limitada, ayuno, fórmulas especiales o nutrición parenteral. Se reseñan a continuación, los tiempos recomendados para la toma de la muestra para cada patología, sin detrimento de la indicación ya reseñada.
Tabla 2. Tiempos recomendados para la toma de muestra de sangre de talón por cada patología de manera específica.
| Patología | Tiempo ideal |
| Hipotiroidismo congénito | 48 a 72 horas |
| Fenilcetonuria | 24 a 72 horas |
| Galactosemia | 48 a 72 horas |
| Fibrosis quística | 48 a 72 horas |
| Déficit de biotinidasa | 24 a 72 horas |
| Hiperplasia suprarrenal congénita | 48 a 72 horas |
| Defectos de la hemoglobina | 36 a 72 horas |
Fuente: Elaboración propia basados en la literatura referenciada. (8)
Además del número de tomas, se ha identificado como buena práctica en tamizaje neonatal que la muestra de sangre seca no se tome de manera inmediata tras la alimentación, sino que se permita un intervalo mínimo entre la última toma y la recolección. Tomar la muestra de forma inmediata tras la toma puede además generar variabilidad analítica por efecto de cambios hemodinámicos o interferencias en la composición del suero. Por tanto, se sugiere que, siempre que sea posible, se respete un intervalo mínimo de 1.5 a 3 horas después de la última alimentación para realizar la punción del talón para la toma de muestra de tamizaje
En casos en los que el neonato reciba fórmulas especiales como leches sin lactosa, fórmulas hidrolizadas, aminoacídicas o nutrición parenteral, es necesario documentar este hecho en el formulario del tamizaje y considerar si se requiere una segunda muestra posterior a la introducción de alimentación convencional, ya que la ausencia de galactosa o fenilalanina en la dieta puede ocultar errores metabólicos como galactosemia o fenilcetonuria.
Tabla 3. Recomendaciones con relación al tamizaje neonatal endocrino metabólico básico de acuerdo al tipo de alimentación del recién nacido (10)
| Tipo de alimentación al momento del tamizaje | Posible impacto en resultados | Recomendación |
| Leche materna exclusiva. | Adecuada para acumulación de metabolitos. | Proceder con toma de muestra. |
| Fórmula estándar con lactosa. | Adecuada para acumulación de metabolitos. | Proceder con toma de muestra. |
| Fórmula sin lactosa / fórmula de soya. | Puede reducir galactosa en sangre - riesgo de falso negativo en galactosemia. | Tomar muestra y repetir después de introducir fórmula estándar o leche materna. |
| Fórmula extensamente hidrolizada o aminoacídica. | Puede reducir fenilalanina v galactosa - riesgo de falsos negativos en PKU v galactosemia. | Tomar muestra y repetir una vez iniciada alimentación con proteínas intactas v lactosa. |
| Nutrición parenteral total (NPT). | No permite acumulación de metabolitos - riesgo de falsos | Tomar muestra inicial v repetir cuando se introduzca alimentación enteral. |
| Ayuno o alimentación insuficiente (< 3 tomas). | Metabolitos bajos, riesgo de falsos negativos, especialmente en PKU y galactosemia. | Registrar claramente v repetir muestra tras alimentación adecuada. |
Es importante verificar en la tarjeta del papel filtro los datos generales en relación con el nombre del paciente, acudiente, teléfonos de contacto, correo electrónico y dirección del domicilio para gestionar la entrega de resultados o rellamado inmediato, así como la asistencia a la consulta de seguimiento del tercer al quinto día por parte de la entidad responsable (articulación entre laboratorio que procesa la muestra, IPS donde se toma la prueba y EAPB o quien haga sus veces).
A nivel de cada IPS, el prestador mismo y los laboratorios donde se procesen las muestras de tamizaje o pruebas confirmatorias, son los encargados de garantizar y hacer seguimiento al desarrollo de capacidades de los profesionales de la salud que toman la muestra de sangre para el tamizaje neonatal y de la calidad de la muestra (cumpliendo lo establecido) que se dispondrá para el procesamiento analítico. Es decir, debe capacitarse y hacerse seguimiento a la calidad de la muestra desde la sala de nacimientos, alojamiento conjunto y de las demás unidades donde se atiendan recién nacidos, en la toma, manejo, almacenamiento y entrega de la muestra.
Así mismo, se debe programar la realización de reentrenamientos para el personal antiguo que está teniendo dificultades en estos procesos, así como garantizar el entrenamiento del personal nuevo de la institución (como parte de los procesos de inducción).
Se deben disponer los mecanismos para registro de la información relacionada con el tamizaje neonatal en sala de nacimientos o en sala de alojamiento conjunto, incluyendo la toma de la muestra, los datos de la tarjeta del papel filtro con los datos de cada paciente, laboratorio que procesa la muestra y fecha de entrega de esta a dicho laboratorio, lo cual será fundamental para la trazabilidad en el Programa de Tamizaje Neonatal.
Se deben tener en cuenta las recomendaciones emitidas por el Instituto Nacional de Salud, para garantizar la calidad en la muestra recolectada en todo el proceso de toma, manejo, almacenamiento y transporte de esta.
- Manejo, almacenamiento y transporte de la muestra
La muestra de sangre debe disponerse en la tarjeta de papel filtro y permitirse su secado completo a temperatura ambiente por un tiempo aproximado de 3 horas. Estas tarjetas de papel filtro deben cumplir con los requerimientos de material, densidad, peso, pH, cenizas, resistencia y absorbancia, tal y como se define en los lineamientos emitidos por el INS.[7] Las tarjetas de papel filtro deben ubicarse en soportes para su secado y almacenamiento, impidiendo el contacto y la mezcla de sangre no seca de diferentes tarjetas de papel filtro. Las tarjetas deben estar completa y adecuadamente diligenciadas, y se deben cuidar las variables de temperatura ambiental, control de humedad y tiempo de secado para garantizar la calidad del proceso. El funcionamiento de estos elementos preanalíticos (verificación de la identificación de factores de riesgo, información registrada por escrito que ha sido brindada a los padres, calidad de la toma de la muestra: así como manejo, embalaje y entrega, y finalmente el registro de la información) es responsabilidad y será liderado por la IPS en articulación con su laboratorio o el laboratorio que realice el procesamiento de las muestras. Las muestras deben ser transportadas por empresas certificadas para transporte de muestras biológicas.
Componente analítico
- Procesamiento analítico de la muestra
El procesamiento analítico de las patologías objeto de esta resolución se realizan generalmente mediante técnicas de ELISA, micro-ELISA, o radio enzimoinmunoensayo, fluorometría, entre otras técnicas disponibles. Se debe realizar el proceso analítico de acuerdo con las especificaciones dadas por las casas productoras de los equipos de análisis y de los kits de las pruebas, cuidando todos y cada uno de los pasos hasta obtener el resultado final.
Se deben atender todas las indicaciones dadas por el INS y por este Ministerio para garantizar la calidad y la oportunidad de los resultados de tamizaje neonatal. Cuando la muestra que ha sido recibida en el laboratorio de análisis es de mala calidad, se debe procesar de todas maneras para evitar el riesgo de dejar pasar un caso positivo, pero se debe informar al laboratorio de la IPS y avisar a la EAPB o quién haga sus veces, para repetir la toma de la muestra. En caso de que se haya dado egreso hospitalario, se debe informar también al referente o líder de tamizaje neonatal de la EAPB del recién nacido (o de la Secretaría de Salud, en el caso de que se trate de un niño sin aseguramiento), y se debe llamar a los números de contacto anotados en la tarjeta de papel filtro.
- Calidad del análisis de la muestra
De acuerdo con el artículo 7o de la Ley 1980 de 2019, los laboratorios que procesen muestras de tamizaje neonatal deben acreditar las pruebas de tamizaje neonatal bajo la norma ISO 15189 ante el Organismo Nacional de Acreditación en Colombia (ONAC).
Los laboratorios deben cumplir todos aquellos requerimientos dirigidos a garantizar la calidad de sus procesos. Por este motivo, debe cumplirse con la normatividad vigente en materia de habilitación, control de calidad en el marco del programa de evaluación de desempeño interno y externo, cumplimiento de estándares de calidad en salud pública y de acreditación, en los términos establecidos en este lineamiento, en la resolución de reglamentación, en la normatividad subsecuente, y deben participar en los programas de evaluación de desempeño coordinados por el INS. Al igual que con todos los procesos relacionados con la toma, manejo, almacenamiento, procesamiento y reporte y notificación de resultados, se debe cumplir con las directrices y lineamientos emitidos desde el INS.
- Registro y notificación de los resultados - flujo de información
La fecha de realización, la tecnología, resultado de tamizaje y pruebas confirmatorias deben ser reportados para el 100% de los recién nacidos conforme lo establecido en la Resolución 202 de 2021, SIVIGILA y Repositorio de Tamizaje Neonatal, y las definiciones normativas vigentes y de acuerdo con los protocolos y lineamientos nacionales emitidos por el Instituto Nacional de Salud.
De igual forma, se debe garantizar la protección de la confidencialidad, la correcta toma de las muestras en el tiempo ideal, la entrega de resultados (tanto casos positivos como negativos), el reporte inmediato a la EPS y a la IPS de referencia en los casos que se encuentren hallazgos en el tamizaje o en el diagnóstico, el registro de resultados (la emisión de resultados debe optimizarse para garantizar la gestión del riesgo oportuna), la gestión oportuna para garantizar la toma de muestra para confirmación de casos positivos en pruebas de tamizaje a través del rellamado inmediato, la disponibilidad de las pruebas confirmatorias, la entrega adecuada de la información y acompañamiento a las familias de los recién nacidos en todo el proceso, así como la gestión para garantizar el inicio del tratamiento y el establecimiento de un plan integral de cuidado para incidir en los resultados en salud de esta población. Es importante la continuidad e integralidad de la atención de los niños y niñas, como requisitos fundamentales para el cumplimiento eficaz de los objetivos del programa.
El objetivo del tamizaje neonatal se cumple, solo si se gestiona de manera inmediata la confirmación o descarte de la patología en cualquier recién nacido con pruebas de tamizaje alteradas.
Se debe indicar a los padres o familiares que deben llevar este resultado a la consulta de seguimiento del recién nacido, realizar el registro de toda la información correspondiente en el carné de salud infantil para que se tenga en consideración en los escenarios de valoración integral definidos en la RPMS.
Componente postanalítico
- Rellamado de los pacientes y confirmación diagnóstica
Cada IPS, laboratorios de procesamiento analítico y EAPB o quien haga sus veces, deben contar con un protocolo por escrito sobre cómo proceder ante casos de tamizaje o retamizaje positivo, en donde se establezca el actuar articulado e inmediato ante el reporte de los resultados de tamizaje neonatal básico. Este protocolo debe incluir los datos de contacto (nombre, teléfono, correo electrónico y dirección) de los líderes, referentes o responsables del tamizaje neonatal o en caso dado de la atención neonatal o materno infantil de las IPS de las que reciben y procesan muestras para tamizaje, de las EAPB a las que están afiliados los pacientes y de los laboratorios que realizan el procesamiento analítico (tanto de tamizaje como de confirmación diagnóstica). Esta información debe ser de conocimiento para la entidad territorial, para favorecer el seguimiento y gestión de los procesos en el marco de la atención materno infantil.
Si el resultado es negativo, se le debe informar claramente a los padres que la prueba permite descartar que el niño tenga dicha patología y el recién nacido continúa en la Ruta Integral de Atención para la Promoción y Mantenimiento de la Salud, garantizándole todas las atenciones contenidas en la misma.
Si los resultados son positivos, los laboratorios que procesan muestras para tamizaje neonatal básico deben garantizar también la toma y el procesamiento de las muestras para la confirmación diagnóstica. En caso de que esto no sea así, los laboratorios, las IPS que atendieron o están atendiendo a los recién nacidos, y las EAPB o quien haga sus veces, deben definir de común acuerdo (y hacerlo constar por escrito) cómo van a garantizar la confirmación diagnóstica dentro de las 24 horas siguientes a la obtención del resultado positivo del tamizaje (o del retamizaje), así como la consulta por profesional de pediatría, neonatología o genetista (según disponibilidad en el territorio) para la lectura e interpretación de los resultados de las pruebas diagnósticas dentro de las 24 horas siguientes al reporte de resultados de las pruebas de diagnóstico. En todo caso, siempre que un tamizaje o retamizaje resulte positivo, se debe llamar de manera inmediata al paciente para la confirmación diagnóstica ("rellamado'' o "recitación"). Este llamado debe ser realizado vía telefónica o un medio eficaz a los datos de contacto de los padres (padre, madre u otro familiar) que están descritos en la tarjeta de papel filtro. Se debe programar la toma de muestra de sangre periférica máximo al día siguiente del resultado positivo del tamizaje (o del retamizaje), para la confirmación diagnóstica.
La información brindada a los padres antes de la realización del tamizaje y de manera especial, el momento del rellamado es esencial, en tanto debe garantizar la sensibilización y adecuada comprensión respecto a la oportunidad que implica realizar un diagnóstico oportuno. Así mismo, el laboratorio debe informar telefónicamente o por un medio eficaz a la IPS de la que procede la muestra del resultado positivo del tamizaje o retamizaje (comunicarse directamente con el responsable de tamizaje neonatal o la persona del área asistencial), para que en caso de que el niño o niña se encuentre allí todavía, pueda tomarse la muestra de sangre para la confirmación diagnóstica; y también para que se registre esta información en el mecanismo establecido para el programa (libro, base de datos u otro). Adicionalmente, el laboratorio debe reportar por vía telefónica, por email o un medio eficaz al líder o referente de tamizaje neonatal de la EAPB del paciente.
En todo caso, la contratación, debe garantizar que el mismo laboratorio o un laboratorio preestablecido desarrolle este procedimiento diagnóstico. La EAPB, en articulación con su red, dispondrá la información respecto a los laboratorios donde se tome la muestra para la prueba diagnóstica, e informará directamente a los padres del recién nacido el lugar para la atención por el profesional en pediatría o profesional en medicina general (solamente en los casos en los que no exista profesional en pediatra) para la lectura e interpretación de los resultados de las pruebas confirmatorias, así como para el inicio del tratamiento de forma oportuna en caso de tratarse de un diagnóstico confirmado.
En caso de tratarse de un niño o niña perteneciente a una familia sin aseguramiento, se debe notificar al encargado o responsable del tema de tamizaje neonatal, atención neonatal o materno infantil en la entidad territorial de salud correspondiente, para gestionar su afiliación al SGSSS y de esta forma garantizar la atención integral de estos niños y niñas.
- Inicio del tratamiento
El inicio del tratamiento debe ser inmediato a la confirmación diagnóstica, las atenciones objeto de las patologías incluidas en el tamizaje neonatal básico deben ser consideradas una urgencia médica.
Se debe considerar el inicio del tratamiento con una prueba de tamizaje positiva en los casos de hipotiroidismo congénito, fenilcetonuria y galactosemia, se debe iniciar tratamiento considerando el balance riesgo beneficio.
Las indicaciones que se dan en la presente resolución aplican para garantizar el tratamiento inicial de los niños y las niñas en quienes se diagnostican las patologías a partir de un resultado positivo en las pruebas de tamizaje.
Nota: Debe tenerse en cuenta que todas estas definiciones serán empleadas en la evaluación y el seguimiento del Programa de Tamizaje Neonatal, en la línea específica de tamizaje metabólico básico, y no sustituyen las definiciones propias del Sistema de Vigilancia Epidemiológica Nacional (SIVIGILA). Sin embargo, deben mantenerse alineadas con dicho sistema en los casos que correspondan a eventos de notificación obligatoria.
La información derivada del tamizaje que resulte en diagnóstico confirmado deberá ser reportada formalmente, según los lineamientos del Instituto Nacional de Salud, utilizando las fichas correspondientes (INS 215 para defectos congénitos y/o INS 342 para enfermedades huérfanas, según aplique). Esta articulación garantiza que el programa de tamizaje no solo contribuya al cuidado individual, sino también a la vigilancia poblacional y a la planeación en salud pública.
4.1.1 Tamizaje de hipotiroidismo congénito
Se define como hipotiroidismo congénito la producción insuficiente de las hormonas tiroideas en los primeros tres años de vida, detectada por la elevación del valor de la Hormona Estimulante de la Tiroides (TSH, por sus siglas en inglés) asociado o no con valores bajos de hormonas tiroideas (hipotiroidismo primario); o a la disminución de los valores normales para la edad de las hormonas tiroideas no asociados con la elevación de la TSH (hipotiroidismo central). Las hormonas tiroideas tienen un papel predominante en el neurodesarrollo durante la primera infancia; por este motivo, el hipotiroidismo congénito representa la principal causa de discapacidad intelectual prevenible (INS, 2019) y se presenta con una incidencia aproximada de entre 1:2.500 – 1:4.500 casos para hipotiroidismo primario (donde la causa es propia del tejido tiroideo), y de 1:100.000 para el hipotiroidismo central (de causa hipofisiaria o hipotalámica). (1)
Teniendo en cuenta que los recién nacidos generalmente no presentan manifestaciones clínicas de hipotiroidismo congénito, así como la alta frecuencia de la patología, y el grave impacto de no detectarla e iniciar tratamiento oportunamente; el hipotiroidismo congénito se incluyó como una patología de tamizaje neonatal y, de hecho, representa la primera patología no metabólica en ser incluida en un panel de tamizaje neonatal.
A nivel internacional, se han dado distintas pautas para el tamizaje de hipotiroidismo congénito. De esta forma, en algunos países se utiliza la medición de la TSH en sangre de cordón umbilical o en sangre de talón, en otros se evalúan los niveles de T4 Libre (T4L) y en otros se utiliza tanto la TSH como la T4L de forma combinada. Incluso, en EEUU existen diferencias en la estrategia de tamizaje de hipotiroidismo congénito entre sus estados (AAP).
Según el INS, la cobertura del tamizaje neonatal de hipotiroidismo congénito en el año 2024 es de aproximadamente 72% (Repositorio de Tamizaje Neonatal INS, 2025) (7). Sin embargo, por distintas dificultades, el llamado para la confirmación diagnóstica se realiza solamente en alrededor del 50% de los niños con resultado de tamizaje alterado ("rellamado" o "recitación"). No se cuenta con información sobre la oportunidad del inicio del tratamiento, la adherencia al tratamiento, el seguimiento de niños y niñas con diagnóstico confirmado, ni otros aspectos importantes como el desenlace desde el punto de vista neurológico.
De esta forma, uno de los objetivos principales de la formulación de estos lineamientos, es brindar las directrices para la estructuración de un programa de tamizaje en el que sea posible contar con la información necesaria para comprender las coberturas de tamizaje y el cumplimiento de las metas de confirmación diagnóstica, inicio de tratamiento y adherencia al seguimiento de los niños y las niñas diagnosticadas, para mejorar así los resultados en salud y en el desarrollo de los niños o niñas con hipotiroidismo congénito.
En el contexto del programa de tamizaje de hipotiroidismo congénito, el resultado del tamizaje puede ser positivo o negativo. Los niños y las niñas con tamizaje positivo deben ser evaluados para la confirmación diagnóstica con un criterio de URGENCIA MÉDICA, puesto que no iniciar el tratamiento tan pronto como se confirme el diagnóstico no solo incumple el objetivo de la Ley y del Programa, sino que se asocia con mayor riesgo de afectación y de discapacidad por causa del hipotiroidismo congénito[8]. En tamizaje neonatal, cada hora y cada día cuentan para lograr los resultados en salud y evitar efectos a largo plazo en el desarrollo integral de los sujetos.
Objetivos de la línea de tamizaje de hipotiroidismo congénito
- Identificar niños y niñas recién nacidos vivos con probable hipotiroidismo congénito primario por medio de la medición de los niveles de TSH.
- Enunciar las situaciones en las que se requiere el retamizaje como parte del proceso de tamizaje de hipotiroidismo congénito primario.
- Definir los aspectos necesarios para el adecuado funcionamiento de los componentes preanalítico, analítico y pos analítico del tamizaje de hipotiroidismo congénito primario.
- Establecer los elementos mínimos de oportunidad y características del diagnóstico de hipotiroidismo congénito primario y del inicio del tratamiento en el marco del plan de cuidado de recién nacidos afectados y de aquellos con condiciones particulares de riesgo.
Definiciones de la línea de tamizaje de hipotiroidismo congénito:
En el contexto del Programa de Tamizaje Neonatal, frente a hipotiroidismo congénito se precisan las siguientes definiciones:
Recién nacido vivo: teniendo en cuenta lo establecido en el artículo 90 del Código Civil, se define como recién nacido vivo al niño o niña que sobrevive siquiera un momento a la separación completa de la madre, esto es, que respira por su cuenta al menos una vez luego de su alumbramiento y del pinzamiento y corte del cordón umbilical. Esta definición no se relaciona con el peso al nacer ni con la edad gestacional.
Recién nacido prematuro: niño o niña que nace antes de la semana 37 de gestación.
Recién nacido prematuro extremo: niño o niña que nace antes de la semana 28 de gestación.
Tamizaje de hipotiroidismo congénito: evaluación de los niveles de TSH en muestra de sangre seca dispuesta en papel filtro, obtenida de fragmento del cordón umbilical en su lado neonatal (técnica de asa) o del talón del niño o niña recién nacido vivo para la detección de casos probables de hipotiroidismo congénito primario.
Retamizaje de hipotiroidismo congénito: evaluación de los niveles de TSH en muestra de sangre seca dispuesta en papel filtro, obtenida del talón del niño o niña. Se comporta como un segundo paso o componente del tamizaje, no es una repetición del tamizaje, no es una medida universal y se indica exclusivamente en los casos en los que por inmadurez del eje hipotálamo- hipofisiario tiroideo (como en la prematuridad) o por riesgo de mezcla de sangres de forma antenatal o perinatal (como en los gemelos monocoriónicos), no es suficiente realizar el tamizaje como se hace en los demás casos, puesto que puede tener una mayor cantidad de falsos negativos.
Diagnóstico de hipotiroidismo congénito: evaluación de los niveles de TSH y de T4L en muestra de suero (de sangre venosa o arterial).
Niño o niña perdido (a) del Programa de Tamizaje Neonatal: recién nacido vivo en quien no se realiza el tamizaje neonatal, no se realiza el retamizaje a pesar de estar indicado, o no se realizan las pruebas de confirmación diagnóstica a pesar de haber tenido un tamizaje o un retamizaje positivo. Debe tenerse en cuenta en qué punto se pierden los niños o las niñas con el objeto de tomar las medidas necesarias para evitar esta situación.
Niño o niña excluido (a) del Programa de Tamizaje Neonatal: recién nacido vivo a quien se realizó el tamizaje pero que fallece antes del retamizaje o del diagnóstico, en este último caso, habiendo tenido un tamizaje o retamizaje positivo. Se incluye también al recién nacido prematuro extremo que fallece antes de la realización del tamizaje en los términos indicados en el presente lineamiento (en el talón, después de 72 horas de nacido).
Respecto al resultado obtenido, el tamizaje puede definirse como:
- Tamizaje positivo de hipotiroidismo congénito: recién nacido con niveles de TSH por encima del punto de corte establecido (![]() 15
15 ![]() UI/ml en muestra de sangre de cordón umbilical, o
UI/ml en muestra de sangre de cordón umbilical, o ![]() 6
6 ![]() UI/ml en muestra de sangre de talón en RN prematuros y
UI/ml en muestra de sangre de talón en RN prematuros y ![]() 10
10 ![]() UI/ml en muestra de sangre de talón en RN a término), los cuales son considerados casos probables de hipotiroidismo congénito.[9]
UI/ml en muestra de sangre de talón en RN a término), los cuales son considerados casos probables de hipotiroidismo congénito.[9]
- Tamizaje negativo de hipotiroidismo congénito: recién nacido con niveles de TSH por debajo del punto de corte establecido.
El tamizaje de hipotiroidismo congénito será interpretado por un profesional en neonatologia, profesional en pediatría o profesional en medicina general entrenado en la interpretación de los resultados del tamizaje de hipotiroidismo congénito. En el caso del retamizaje, al ser considerado como un segundo paso del tamizaje en un grupo de niños y niñas, se aplican las mismas definiciones de los resultados del tamizaje, teniendo en cuenta que el punto de corte es el de la muestra de sangre que procede del talón.
Respecto a la realización del diagnóstico de hipotiroidismo congénito, se tendrán en cuenta las siguientes definiciones:
- Rellamado: procedimiento de llamado o citación activa de los pacientes y su familia ante un resultado de tamizaje metabólico positivo, con el fin de realizar pruebas confirmatorias y definir la conducta diagnóstica y terapéutica.
- Diagnóstico confirmado de hipotiroidismo congénito: recién nacido con tamizaje (o retamizaje) positivo con niveles de TSH por encima del valor de referencia del kit de ensayo y/o con niveles de T4L por debajo del valor de referencia del kit de ensayo de las pruebas de diagnóstico. Por consenso de expertos se considera también diagnóstico confirmado cuando el THS sea ![]() 20 mU/L sin importar niveles de T4 libre, o niveles bajos de T4 libre sin importar TSH.
20 mU/L sin importar niveles de T4 libre, o niveles bajos de T4 libre sin importar TSH.
- Diagnóstico descartado de hipotiroidismo congénito: recién nacido con tamizaje (o retamizaje) positivo con niveles de TSH y de T4L dentro del rango de referencia del kit de ensayo de las pruebas de diagnóstico.
En relación con el tratamiento, se especifican las siguientes definiciones:
- Niño o niña con tratamiento: niño o niña con diagnóstico confirmado de hipotiroidismo congénito quien se encuentra en tratamiento con levotiroxina de forma continua o regular.
- Niño o niña sin tratamiento: niño o niña con diagnóstico confirmado de hipotiroidismo congénito quien se encuentra sin tratamiento con levotiroxina de forma continua o regular.
- Niño o niña sin información de tratamiento: niño o niña con diagnóstico confirmado de hipotiroidismo congénito en quien no se cuenta con información sobre el inicio y la continuidad del tratamiento con levotiroxina.
- Niño o niña con seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de hipotiroidismo congénito quien tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de pediatría con abordaje de su condición de mayor riesgo según lo señalado en la RPMS.
- Niño o niña sin seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de hipotiroidismo congénito quien no tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de pediatría con abordaje de su condición de mayor riesgo según lo señalado en la RPMS.
NOTA: Debe tenerse en cuenta que un niño o una niña puede tener hipotiroidismo congénito y manifestarlo posterior a haber tenido un tamizaje y/o un retamizaje negativo, o incluso, a pesar de haber tenido un tamizaje o un retamizaje positivo, pero con un resultado posterior de diagnóstico descartado. En este caso, puede tratarse de un hipotiroidismo congénito de inicio "tardío" (que no es captado en el Programa de Tamizaje Neonatal) o de un caso no identificado en el Programa de Tamizaje Neonatal (falso negativo en el tamizaje, el retamizaje o el diagnóstico). En todo caso, los niños y las niñas con probable hipotiroidismo congénito siempre deben ser reportados al SIVIGILA y debe gestionarse el cierre de caso para reportar el resultado del diagnóstico.
Tecnología del tamizaje de hipotiroidismo congénito
Como se indicó previamente, en Colombia, el tamizaje de hipotiroidismo congénito se debe realizar a través de la medición de los niveles de TSH en muestra de sangre seca depositada en papel filtro. Esta muestra de sangre puede obtenerse de fragmento del cordón umbilical del lado neonatal según la "técnica del asa" o por medio de la punción del talón del niño o niña.
Teniendo en cuenta que posterior al nacimiento se presenta un "estallido" fisiológico de liberación de la Hormona Estimulante de la Tirotropina desde el hipotálamo (TRH, por sus siglas en inglés), de la TSH desde la adenohipófisis y de las hormonas tiroideas desde la tiroides.
En Colombia, se ha permitido la práctica del tamizaje de hipotiroidismo congénito con la toma de la muestra del cordón umbilical como una forma de garantizar la realización del procedimiento para que se realice en el tiempo de estancia hospitalaria del recién nacido. La Resolución 3280 de 2018 establece el criterio de tiempo de estancia hospitalaria para el recién nacido y la madre: "El alta hospitalaria se debe dar a las 24 horas de un parto vaginal y de 48 después de una cesárea como mínimo.'', así como reitera la obligatoriedad del tamizaje neonatal.
En procura de avanzar hacia el tamizaje de hipotiroidismo congénito y de otras patologías con muestra de sangre proveniente de manera exclusiva del talón del niño o niña, cada IPS y EAPB (o quién haga sus veces) del país, que atiende recién nacidos debe trazar un plan para garantizar la toma de muestra de sangre del talón, con el objeto de que, se realice el cambio progresivo del origen de la muestra de sangre del cordón umbilical al talón.
Cuando se tome la muestra de sangre del cordón umbilical, debe hacerse en un tiempo no mayor a 20 minutos posterior al nacimiento del niño o niña y por ningún motivo se debe tomar del lado placentario del cordón umbilical, mucho menos si no se ha producido el alumbramiento de la placenta. Cuando se tome la muestra de sangre del talón del niño o niña, se recomienda tomar entre las 48 y 72 horas de vida, sin embargo, se puede considerar la posibilidad de tomar durante las primeras 24 horas de vida (solamente en los casos que haya riesgo de no garantizarse la toma en los tiempos definidos previamente), antes del egreso hospitalario del recién nacido, considerando un mayor riesgo de falsos resultados. Debe realizarse con la lanceta adecuada, para garantizar la sangría necesaria para que no se afecte la disposición de la sangre en el papel filtro. Para el caso de hipotiroidismo congénito, debe garantizarse el procesamiento de la muestra de cordón y también el procesamiento de la muestra de sangre en talón.
Si bien los niveles de TSH son distintos a lo largo de los primeros días de vida, en Colombia se definió un punto de corte especifico. Se decide continuar con este mismo punto de corte para la muestra obtenida (Cordón ![]() 15
15![]() UI/ml; Talón
UI/ml; Talón ![]() 6
6 ![]() UI/ml en RN pretérmino y
UI/ml en RN pretérmino y ![]() 10
10 ![]() Ul/ml en RN a término).[10]
Ul/ml en RN a término).[10]
En el caso de los recién nacidos prematuros extremos (nacidos antes de la semana 28 de gestación), no se recomienda el tamizaje por muestra de sangre del cordón umbilical, y debe realizarse a las 72 horas del nacimiento en muestra de sangre proveniente del talón del niño o niña. En este contexto particular, el punto de corte del tamizaje es ![]() 6
6 ![]() Ul/ml para prematuros, por lo que se considera positivo un tamizaje con un nivel de TSH mayor a este punto de corte.
Ul/ml para prematuros, por lo que se considera positivo un tamizaje con un nivel de TSH mayor a este punto de corte.
En el caso del retamizaje, el cual realmente se trata del segundo paso del tamizaje para dos grupos específicos de recién nacidos (prematuros y gemelos monocoriónicos), se realizará al igual que el tamizaje, con la medición de los niveles de TSH en muestra de sangre seca proveniente del talón del niño o niña y depositada en papel filtro. En el caso de los recién nacidos prematuros (nacidos antes de la semana 37 de gestación), se indica el retamizaje con TSH a las 2 semanas del nacimiento. Para los recién nacidos gemelos monocoriónicos a término, el retamizaje se indica a los 5 días de nacimiento. En ambos casos, el punto de corte es el mismo del tamizaje por muestra proveniente de sangre del talón ![]() 10
10 ![]() Ul/ml).
Ul/ml).
Componentes del tamizaje de hipotiroidismo congénito
Por las características del tamizaje de hipotiroidismo congénito, al igual que el de otras patologías endocrino-metabólicas en las que se cuenta con la participación del laboratorio de tamizaje, se han definido elementos preanalíticos específicos para esta patología. Si bien es cierto que la detección y el tratamiento oportuno del hipotiroidismo congénito que se realiza por medio de los programas de tamizaje ha eliminado casi por completo el retraso mental asociado, el éxito se enfoca también, en el seguimiento mediante la monitorización oportuna y continua para ajustar el tratamiento según se requiera. Por lo tanto, este Ministerio dispondrá de las orientaciones para favorecer el seguimiento adecuado de los niños y niñas con diagnóstico confirmado de hipotiroidismo congénito.
El laboratorio de cada IPS tiene importantes responsabilidades para el funcionamiento de la línea endocrino-metabólica para el tamizaje neonatal.
Componente preanalítico
- Enfoque antenatal de riesgo y realización de la historia clínica: en relación con la línea de tamizaje de hipotiroidismo congénito, los siguientes son los riesgos y factores prenatales (antecedentes maternos de enfermedad tiroidea, antecedente de hipotiroidismo congénito en hermano), perinatales (prematuridad, enfermedad neonatal grave y posibilidad de sobreexposición a yodo por múltiples procedimientos quirúrgicos); así como postnatales (Síndromes Genéticos - sospecha o diagnóstico Anomalías Congénitas - especialmente de línea media detección de bocio o de quiste sublingual - por ecografía prenatal o al examen físico) los cuales deben ser tenidos en cuenta en la atención del neonato, el tamizaje neonatal y el seguimiento posterior. En el caso de una mujer gestante con antecedente de hipotiroidismo, se debe verificar si se realizó ajuste a la dosis de la levotiroxina durante la gestación y si tuvo valoración o seguimiento por endocrinología. En todo caso, estos aspectos refuerzan la necesidad de seguimiento de su función tiroidea; pero debe reiterarse que el tamizaje es una medida universal y todos los recién nacidos deben recibir esta atención.
- Toma de la muestra de sangre: A nivel de cada IPS, el prestador mismo y el laboratorio son los encargados de garantizar y hacer seguimiento al desarrollo de capacidades de los profesionales de la salud que toman la muestra de sangre para el tamizaje neonatal[11] y de la calidad de la muestra (cumpliendo lo establecido) que se dispondrá para el procesamiento analítico. Es decir, debe capacitarse y hacerse seguimiento a la calidad de la muestra desde la sala de nacimientos, alojamiento conjunto y de las demás unidades donde se atiendan recién nacidos, en la toma, manejo, almacenamiento y entrega de la muestra
Componente analítico
- Registro y notificación de los resultados. Se debe garantizar la entrega de los resultados de la prueba de tamizaje (incluso en los casos negativos) y se debe indicar a los padres familiares que deben llevar este resultado a la consulta de seguimiento del recién nacido, realizar el registro de toda la información correspondiente en el carné de salud infantil para que se tenga en consideración en los escenarios de valoración integral definidos en la Ruta Integral de Atención para la Promoción y Mantenimiento de la Salud (RIAPMS).
Componente post analítico
Confirmación diagnóstica: se realiza mediante la medición de los niveles de TSH y de T4L en sangre periférica. El hipotiroidismo congénito se diagnostica cuando el nivel de la TSH se encuentra por encima o igual a 20 mll/L sin importar los niveles de T4 libre y/o cuando el nivel de la T4L se encuentra por debajo del rango de referencia para la técnica de análisis, sin importar los niveles de TSH. El laboratorio debe reportar el nivel de la TSH en pUl/ml o mU/L, y el de la T4L en ng/dL, así como el valor del rango de referencia para cada una de las pruebas. Teniendo en cuenta que el diagnóstico y el inicio del tratamiento en hipotiroidismo congénito se considera una urgencia médica, los laboratorios en los que se realiza el procesamiento analítico de las muestras de sangre para la confirmación diagnóstica deben funcionar las 24 horas del día, todos los días del año.
- Igualmente, será de obligatorio cumplimiento el reporte inmediato del resultado positivo y negativo de la prueba confirmatoria al Repositorio de Tamizaje Neonatal, administrado por el INS.
Inicio del tratamiento: teniendo en cuenta la importancia de las hormonas tiroideas para el neurodesarrollo y la elevada tasa de formación de conexiones neuronales (sinaptogénesis) durante las primeras semanas de vida, el diagnóstico y el inicio del tratamiento del hipotiroidismo congénito debe ser considerado una URGENCIA MÉDICA. En hipotiroidismo congénito, el tiempo es determinante, por este motivo, el inicio del tratamiento debe ser inmediato a la confirmación diagnóstica, máximo a la mañana siguiente de esta. Así mismo, podrá ser iniciado cuando el resultado del tamizaje (o del retamizaje) sea ![]() 40
40 ![]() Ul/ml con previa toma de muestra de sangre para la confirmación diagnóstica, momento en el cual se ajustará el abordaje de acuerdo con la prueba diagnóstica. Para efectos del Programa de Tamizaje Neonatal, no se considerará el término de hipotiroidismo subclínico (TSH elevada con T4L en rango normal), puesto que ante la elevación del nivel de TSH es impredecible saber en qué momento se pueden reducir los niveles de T4 Libre. Entonces, ante el riesgo de no garantizar oportunamente el tratamiento a un niño o niña con hipotiroidismo subclínico en proceso de descompensación, es preferible iniciar el tratamiento con la elevación aislada de los niveles de TSH. De otro lado, en el contexto del Programa de Tamizaje Neonatal tampoco se debe emplear el término de hipotiroidismo congénito transitorio, puesto que es dominio del especialista en endocrinología pediátrica establecer la transitoriedad o la permanencia del hipotiroidismo congénito, y las indicaciones que aquí se dan aplican para garantizar el tratamiento de los niños y las niñas en quienes se diagnostica hipotiroidismo congénito a partir de un resultado positivo en una prueba de tamizaje.
Ul/ml con previa toma de muestra de sangre para la confirmación diagnóstica, momento en el cual se ajustará el abordaje de acuerdo con la prueba diagnóstica. Para efectos del Programa de Tamizaje Neonatal, no se considerará el término de hipotiroidismo subclínico (TSH elevada con T4L en rango normal), puesto que ante la elevación del nivel de TSH es impredecible saber en qué momento se pueden reducir los niveles de T4 Libre. Entonces, ante el riesgo de no garantizar oportunamente el tratamiento a un niño o niña con hipotiroidismo subclínico en proceso de descompensación, es preferible iniciar el tratamiento con la elevación aislada de los niveles de TSH. De otro lado, en el contexto del Programa de Tamizaje Neonatal tampoco se debe emplear el término de hipotiroidismo congénito transitorio, puesto que es dominio del especialista en endocrinología pediátrica establecer la transitoriedad o la permanencia del hipotiroidismo congénito, y las indicaciones que aquí se dan aplican para garantizar el tratamiento de los niños y las niñas en quienes se diagnostica hipotiroidismo congénito a partir de un resultado positivo en una prueba de tamizaje.
El tratamiento se debe iniciar con levotiroxina 10 a 15 microgramos/kg/día. Para esto, se debe triturar la tableta del medicamento y administrarse en máximo dos centímetros de agua o leche materna en las mañanas. El medicamento no debe ser administrado en otro liquido diferente (por ejemplo, jugos) y debe ser administrado todos los días en el mismo horario. Es recomendable que en las piezas comunicativas que se usen para promover el programa y la práctica del tamizaje neonatal, se deje explícito que el tratamiento es gratuito y debe ser continuo y regular. En ningún caso, la realización de una imagen diagnóstica, la evaluación de transitoriedad o la búsqueda de etiología se considerarán factores indispensables para el inicio del tratamiento y por lo tanto no debe retrasarse por ningún motivo.
Todas las niñas y niños con diagnóstico de hipotiroidismo congénito deben recibir la consulta médica por profesional de pediatría en los primeros 15 días o endocrinología pediátrica (según disponibilidad en territorio) en el primer mes posterior al diagnóstico, para la cual debe contarse con resultado de TSH y T4 L en sangre periférica tomada entre las 2 a 4 semanas de haber iniciado el medicamento.
Figura 1. Esquema de tamizaje neonatal de hipotiroidismo congénito.
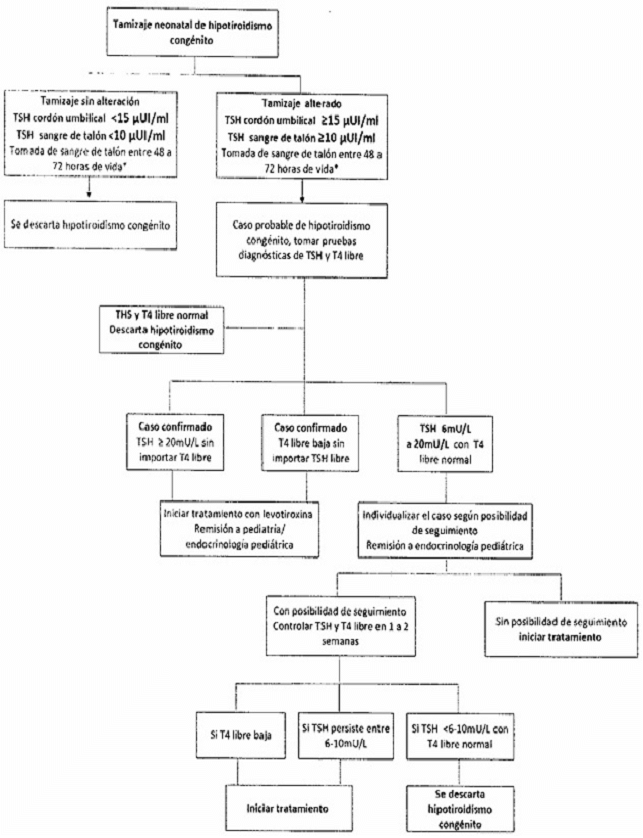
Consideraciones descritas en el apartado 4.1. - componente preanalítico. Fuente: Elaboración propia a partir de literatura referenciada.
Se establecen los puntos de corte de acuerdo con los lineamientos establecidos por el Instituto Nacional de Salud, los cuales están sujetos de actualización. (11)
A continuación, se presenta la síntesis de las directrices frente al tamizaje y diagnóstico de hípotiroidismo congénito, incorporando algunas observaciones a tenerse en cuenta. En la tabla 4 se indican los aspectos para tener en cuenta para el seguimiento de grupos de niños con condiciones particulares, en el contexto del Programa de Tamizaje Neonatal.
Tabla 4. Directrices de tamizaje y diagnóstico del hipotiroidismo congénito en el contexto del Programa de Tamizaje Neonatal.
| Grupo Poblacional | Tamizaje | Retamizaje | Diagnóstico | Observaciones |
| Recién nacido (RN) a término | Punto de corte cordón: 15 | NO | Nivel de TSH mayor al punto de corte de la referencia cada de laboratorio, especificado para la técnica de análisis y según la edad del paciente. Debe ser expresado en | Se debe disponer y comunicar el resultado del tamizaje durante la primera semana de vida como máximo.Si el tamizaje resulta positivo, se debe garantizar la toma de TSH y T4L máximo al día siguiente de tener el resultado de la TSH. Se debe manejar y procesar en laboratorio como una urgencia médica. Si se confirma el diagnóstico, se debe iniciar el tratamiento inmediatamente, máximo al día siguiente en el que se confirma el diagnóstico.Desde una perspectiva poblacional, el tratamiento debe haberse iniciado en la primera semana o máximo durante la segunda semana de nacimiento. |
| RN prematuro | En menores de 32 semanas debe realizarse a las 72 horas con muestra de sangre procedente del talón y su punto corte es: <6 | A los 15 días del nacimiento, con muestra de talón con punto de corte: 10 | Igual que lo descrito para el RN a término. | Igual que lo descrito para el RN a término. |
| Gemelos mono coriónico. | Igual que para el RN a término o el RN prematuro, según el caso. | En RN a término, se retamizarán a los días del nacimiento con muestra de talón y Punto de corte: 10 | Igual que lo descrito para el RN a término. | Igual que lo descrito para el RN a término |
Tabla 5. Directrices de tamizaje de hipotiroidismo congénito y seguimiento en niños con condiciones particulares
| Grupo Poblacional | Tamizaje | Retamizaje | Diagnóstico | Observaciones |
| Niño o niña con bajo peso al nacer, restricción de crecimiento intrauterino o Pequeño para la Edad gestacional. | Igual que para el RN a término, excepto si es prematuro, caso en el que se procede según lo indicado en esta situación. | NO. Excepto si es prematuro o gemelo mono coriónico. | Igual que lo descrito para el RN a término. | Realizar seguimiento por datos de historia clínica y examen físico. No indicación de retamizaje. Se debe atender |
| Niño o niña a término críticamente enfermo y/o con sospecha o riesgo de lesión neurológica aguda. | Igual que para el RN a término, excepto si es prematuro, caso en el que se procede según lo indicado en esta situación. | NO. Excepto si es prematuro o gemelo mono coriónico. | Igual que lo descrito para el RN a término | Seguimiento por datos de historia clínica y examen físico. Indicación de evaluación con TSH y T4L dentro de los procedimientos de atención integral de su patología.___ |
| Niño o niña hijo o hija de madre con hipotiroidismo. | Igual que para el RN a término, excepto si es prematuro, caso en el que se procede según lo indicado en esta situación. | NO. Excepto si es prematuro o gemelo mono coriónico. | Igual que lo descrito para el RN a término. | No se debe realizar retamizaje o de seguimiento especial de laboratorios de función tiroidea. |
| Niño o niña hijo de madre con hipertiroidismo tiroidectomizada o con tratamiento farmacológico. | Igual que para el RN a término, excepto si es prematuro, caso en el que se procede según lo indicado en esta situación. Requiere hospitalización en unidad neonatal. | NO. Excepto si es prematuro o gemelo mono coriónico. | Igual que lo descrito para el RN a término. | Remisión para nacimiento en institución de mayor complejidad que cuente con endocrinología pediátrica. Se recomienda hospitaliazación para atención en unidad neonatal. Tine indicación para la toma de anticuerpos contra el receptor de TSH en sangre de cordón umbilical. Debe ser valorado por endocrinología pediátrica. |
| Niño o niña con antecedente de hipotiroidismo congénito en hermano. | Igual que para el RN a término, excepto si es prematuro, caso en el que se procede según lo indicado en esta situación. | NO. Excepto si es prematuro o gemelo mono coriónico. | Igual que lo descrito para el RN a término | No realizar retamizaje o de seguimiento especial de laboratorios de función tiroidea. Se debe remitir a genética |
| Niño o niña con Síndrome de Down. | Igual que para el RN a término, excepto si es prematuro, caso en el que se procede según lo indicado en esta situación. | NO. Excepto si es prematuro c gemelo mono coriónico. | Igual Que lo descrito para el RN a término. | No se realiza retamizaje, pero se debe remitir a endocrinología pediátrica incluso Si tamizaje neonatal de TSH es normal y no tiene clínica de hipotiroidismo congénito. Se debe remitir a genética. |
| Niño o niña con defectos de línea media u otros defectos congénitos. | Igual que para el RN a término, excepto si es prematuro, caso en el que se procede según lo indicado en esta situación | NO. Excepto si es prematuro o gemelo mono coriónico. | Igual que lo descrito para el RN a término. | Seguimiento por datos de historia clínica y examen físico. No realizar retamizaje, pero con remitir a genética y seguimiento interdisciplinario. |
| Niño o niña con sobreexposición a yodo (3 o más procedimientos con preparación extensa con yodopovidona o alcohol yodado). | Igual que para el RN a término, excepto si es prematuro, caso en el que se procede según lo indicado en esta situación. | NO. Excepto si es prematuro o gemelo mono coriónico. | Igual que lo descrito para el RN a término. | Seguimiento por datos de historia clínica y examen físico. No se retamizaje, pero con seguimiento de función tiroidea con TSH y T4 dentro de la atención integral en salud que requiera. |
| Niño o niña con bocio (detección antenatal por ecografía o postnatal por examen físico). | Igual que para el RN a término, excepto si es prematuro, caso en el que se procede según lo indicado en esta situación. | NO. Excepto si es prematuro o gemelo mono coriónico. | Igual que lo descrito para el RN a término. | No realizar retamizaje, pero con se debe remitir para seguimiento por endocrinología pediátrica incluso si tamizaje neonatal de TSH es normal. Debe tenerse prestarse atención al riesgo de obstrucción de vía aérea |
(1)
4.1.2 Tamizaje de fenilcetonuria
Número de identificación de la enfermedad huérfana rara: 920
La fenilcetonuria (PKU) es un error innato del metabolismo con patrón de herencia autosómico recesivo, causado por la deficiencia de la enzima fenilalanina hidroxilasa (PHA), responsable de la conversión de fenilalanina en tirosina.
Figura 2. Metabolismo de fenilalanina
Adaptado de: HubPages»Education and SciencewLife Sciences»Genetics. Genetic Disorders - Phenylketonuria (2025)
La acumulación de fenilalanina y sus metabolitos neurotóxicos en sangre y tejidos, en ausencia de tratamiento oportuno, puede producir trastornos severos del neurodesarrollo, discapacidad intelectual irreversible, convulsiones, síntomas conductuales y psiquiátricos. Así como microcefalia en hijos de madres con fenilcetonuria no tratada. Los recién nacidos afectados son asintomáticos al nacer, por lo que el tamizaje neonatal constituye la única herramienta efectiva para identificar precozmente los casos y prevenir el daño neurológico.
El objetivo principal del tamizaje es reducir la carga de discapacidad por PKU en el país mediante la identificación temprana, confirmación diagnóstica y tratamiento oportuno de los lactantes afectados.
Si bien existen estimaciones globales de prevalencia, con cifras de 1 en 10.000 en poblaciones caucásicas y menor frecuencia en otras etnias, en Colombia no se dispone de datos poblacionales robustos ni estudios epidemiológicos actualizados que sustenten con certeza las cifras proyectadas. Por tanto, resulta prioritario fortalecer el sistema de registro, vigilancia y notificación, garantizando que las decisiones de política pública se basen en evidencia nacional confiable y actualizada. De acuerdo con el Registro Nacional de Personas con Enfermedad Huérfana desde el año 1960 se han reportado 29 casos, la mayoría del género masculino con un total de 17 casos en comparación con el género femenino con 12 casos.
| Prevalencia | 1:10.000 |
| Edad promedio diagnóstico (Meses) | 1 a 2 meses |
| Resultado en Salud a incidir con el tamizaje | Discapacidad cognitiva |
Los recién nacidos son asintomáticos antes del inicio de los alimentos que contienen fenilalanina (leche materna o fórmula infantil estándar). Si no se detecta durante el período neonatal, el inicio de la fenilcetonuria es insidioso y puede no causar síntomas hasta la primera infancia. La elevación de la fenilalanina en rangos fuera de lo normal condiciona daño neurológico y déficit cognitivo. Durante los primeros meses de vida, los niños nacidos con PKU parecen sanos, pero si no reciben diagnóstico oportuno e inicio de tratamiento dentro de los primeros 20 días de vida, empiezan a presentar manifestaciones clínicas alrededor de los seis meses de vida y pueden tardar en aprender a sentarse, gatear o caminar. El deterioro cognitivo empeora durante la mielinización en la primera infancia con el aumento de la exposición dietética a la fenilalanina, si no es tratada luego de un año, produce daño irreversible.
En su mayoría, en la PKU clásica los pacientes diagnosticados tardíamente presentan un retraso progresivo del desarrollo, asociado a signos graves que incluyen retraso del crecimiento, microcefalia, crisis, temblores, eccema, vómitos, olor peculiar a humedad y, posteriormente, trastornos de conducta (hiperactividad) y motores. Los pacientes no tratados experimentan una afectación intelectual profunda y permanente, así como del rendimiento cognitivo y de las habilidades motoras. En pacientes que no siguen las restricciones nutricionales en la edad adulta, se ha descrito desmielinización y disminución de la producción de dopamina, norepinefrina y serotonina Las complicaciones posteriores son exaltación de los reflejos tendinosos profundos, temblores y paraparesia o hemiplejía. En pacientes tratados, los signos clínicos varían según el tratamiento y la adherencia a la dieta, y pueden incluir trastornos psiquiátricos como el trastorno por déficit de atención e hiperactividad y depresión. (12) (10) (13)
Objetivos de la línea de tamizaje de fenilcetonuria
- Detectar de forma temprana niños y niñas recién nacidos vivos con concentraciones elevadas de fenilalanina en muestra de talón, sugestivas de fenilcetonuria o hiperfenilalaninemia.
- Establecer lineamientos técnicos claros para el seguimiento de casos sospechosos y confirmados, incluyendo la articulación con genética médica, nutrición especializada y pediatría.
- Identificar condiciones clínicas o factores de riesgo que puedan requerir un abordaje diferenciado o intensificado del seguimiento.
- Establecer los elementos mínimos de oportunidad y características del diagnóstico de fenilcetonuria y del inicio del tratamiento en el marco del plan de cuidado de recién nacidos afectados y de aquellos con condiciones particulares de riesgo.
- Iniciar precozmente el tratamiento dietético en los casos confirmados, minimizando el riesgo de daño neurológico irreversible y mejorando el pronóstico a largo plazo.
Definiciones de la línea de tamizaje de fenilcetonuria
Respecto al resultado obtenido, el tamizaje puede definirse como:
- Tamizaje positivo para fenilcetonuria: recién nacido con niveles de PHE por encima del punto de corte establecido ( ![]() 2mg/dL (
2mg/dL ( ![]() 120pmol/L) en muestra de sangre de talón), los cuales son considerados casos probables de fenilcetonuria o hiperfenilalaninemia leve, moderada o severa.
120pmol/L) en muestra de sangre de talón), los cuales son considerados casos probables de fenilcetonuria o hiperfenilalaninemia leve, moderada o severa.
- Tamizaje negativo de fenilcetonuria: recién nacido con niveles de PHE menores al punto de corte Este resultado no requiere seguimiento adicional, salvo que existan condiciones clínicas especiales o antecedentes familiares relevantes.
Para efectos de la evaluación y tratamiento del Programa de Tamizaje Neonatal, se emplearán las siguientes definiciones en relación con la confirmación diagnóstica para fenilcetonuria:
- Rellamado: procedimiento de llamado o citación activa de los pacientes y su familia ante un resultado de tamizaje metabólico positivo o en zona gris, con el fin de realizar pruebas confirmatorias y definir la conducta diagnóstica y terapéutica.
- Diagnóstico confirmado de fenilcetonuria: condición establecida cuando un recién nacido con tamizaje positivo presenta elevación confirmada en la prueba de aminoácidos plasmáticos cuantitativos, y se excluyen otras causas de hiperfenilalaninemia.
- Diagnóstico descartado de fenilcetonuria: condición en la cual, tras el resultado de tamizaje positivo o en zona gris, las pruebas confirmatorias (aminoácidos plasmáticos cuantitativos) son normales, sin evidencia de hiperfenilalaninemia clínicamente significativa.
Se especifican las siguientes definiciones relacionadas con la atención terapéutica del paciente con diagnóstico confirmado:
- Niño o niña con tratamiento: niño o niña con diagnóstico confirmado de fenilcetonuria que ha iniciado manejo con fórmula láctea especial libre de fenilalanina, según lo indicado por el equipo médico tratante.
- Niño o niña sin tratamiento: niño o niña con diagnóstico confirmado de fenilcetonuria que no ha recibido fórmula especial ni ninguna intervención terapéutica orientada al control de los niveles de fenilalanina.
- Niño o niña sin información de tratamiento: niño o niña con diagnóstico confirmado de fenilcetonuria del que no se dispone de datos verificables sobre el inicio, tipo o continuidad del tratamiento.
Respecto a la continuidad del cuidado, se establecen los siguientes conceptos:
- Niño o niña con seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de fenilcetonuria quien tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de especialista con abordaje de su condición de mayor riesgo, según lo señalado en la RPMS.
- Niño o niña sin seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de fenilcetonuria quien no tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de especialista con abordaje de su condición de mayor riesgo según lo señalado en la RPMS.
Tecnología del tamizaje neonatal de fenilcetonuria
El tamizaje neonatal para fenilcetonuria debe realizarse mediante la punción de talón, recolectando sangre en papel filtro. La prueba para tamizaje que se consideró es la cuantificación de fenilalanina (Descripción CUPS: Fenilalanina cuantitativa), el punto de corte para tamizaje positivo es ![]() 2mg/dL (equivalente a
2mg/dL (equivalente a ![]() 120
120![]() mol/L).
mol/L).
Si bien se recomienda que la toma de la muestra para fenilcetonuria se realice entre las 24 y 72 horas de vida, asegurando que el recién nacido haya recibido alimentación previa (mínimo tres tomas), lo cual es indispensable para evitar falsos negativos; en el caso de Colombia está indicada una sola toma de muestra para las 7 patologías, la cual debe desarrollarse entre las 48 y 72 horas con las consideraciones descritas en el apartado 4.1. - componente preanalítico.
El tiempo máximo para la toma de la muestra debe ser de 5 días de vida, dado que el acúmulo de fenilalanina por deficiencia enzimática puede generar daño neurológico irreversible desde etapas muy tempranas.
El tamizaje de fenilcetonuria será interpretado por un profesional en pediatría, neonatología o profesional en medicina general entrenado en la interpretación de los resultados del tamizaje metabólico básico.
Clasificación de resultados del tamizaje para fenilcetonuria
Los resultados del tamizaje neonatal para fenilcetonuria deben clasificarse en tres categorías claramente definidas para facilitar una interpretación estandarizada y acciones clínicas oportunas:
1. Resultado negativo: valores de fenilalanina <2 mg/dL (<120 ![]() mol/L). Estos resultados no requieren seguimiento adicional, salvo que existan condiciones clínicas especiales o antecedentes familiares relevantes.
mol/L). Estos resultados no requieren seguimiento adicional, salvo que existan condiciones clínicas especiales o antecedentes familiares relevantes.
2. Resultado en rango intermedio (zona de indeterminación o "zona gris"): valores entre 2 mg/dL y 6 mg/dL (120 ![]() mol/L y 360
mol/L y 360 ![]() mol/L). En este rango no puede descartarse una hiperfenilalanínemia leve o una variante no clásica de fenilcetonuria. Se recomienda realizar confirmación diagnóstica mediante aminoácidos cuantitativos en plasma y seguimiento clínico, sin iniciar tratamiento de manera inmediata salvo indicación específica. Se recomienda seguir una ruta diagnóstica específica: Seguimiento clínico, nutricional y bioquímico, así como la cuantificación repetida de aminoácidos en plasma cada 5 a 7 días durante las primeras 3 a 4 semanas de vida, o con mayor frecuencia si hay cambios en la alimentación o síntomas clínicos. En este escenario, los cambios en la alimentación son una variable critica al interpretar los niveles de fenilalanina. Por eso, cualquier modificación dietética debe ser cuidadosamente documentada y considerada en el análisis clínico y bioquímico, y preferiblemente supervisada por expertos en errores innatos del metabolismo o nutrición clínica pediátrica. Leche materna contiene una cantidad moderada de fenilalanina (aprox. 46 mg por 100 mi). Su digestión puede ser más lenta y el contenido proteico más bajo comparado con algunas fórmulas, por lo que los niveles de fenilalanina pueden subir más lentamente. Algunas fórmulas estándar contienen más proteínas, y por tanto, más fenilalanina. En bebés que reciben fórmula artificial exclusivamente, los niveles de Phe pueden elevarse más rápidamente.
mol/L). En este rango no puede descartarse una hiperfenilalanínemia leve o una variante no clásica de fenilcetonuria. Se recomienda realizar confirmación diagnóstica mediante aminoácidos cuantitativos en plasma y seguimiento clínico, sin iniciar tratamiento de manera inmediata salvo indicación específica. Se recomienda seguir una ruta diagnóstica específica: Seguimiento clínico, nutricional y bioquímico, así como la cuantificación repetida de aminoácidos en plasma cada 5 a 7 días durante las primeras 3 a 4 semanas de vida, o con mayor frecuencia si hay cambios en la alimentación o síntomas clínicos. En este escenario, los cambios en la alimentación son una variable critica al interpretar los niveles de fenilalanina. Por eso, cualquier modificación dietética debe ser cuidadosamente documentada y considerada en el análisis clínico y bioquímico, y preferiblemente supervisada por expertos en errores innatos del metabolismo o nutrición clínica pediátrica. Leche materna contiene una cantidad moderada de fenilalanina (aprox. 46 mg por 100 mi). Su digestión puede ser más lenta y el contenido proteico más bajo comparado con algunas fórmulas, por lo que los niveles de fenilalanina pueden subir más lentamente. Algunas fórmulas estándar contienen más proteínas, y por tanto, más fenilalanina. En bebés que reciben fórmula artificial exclusivamente, los niveles de Phe pueden elevarse más rápidamente.
Si la hiperfenilalaninemia persiste, es fundamental considerar la realización de pruebas moleculares que permitan confirmar o descartar variantes patogénicas en el gen PAH o en otros genes asociados con hiperfenilalaninemias no fenilcetonúricas (como PCBD1, GCH1, QDPR, entre otros). La identificación temprana de estas variantes permite diferenciar entre condiciones que requieren tratamiento dietario estricto y aquellas que pueden ser transitorias o no progresivas, evitando tanto el sobretratamiento como la omisión de intervenciones necesarias. La prueba molecular no debe retrasar la toma de decisiones clínicas iniciales, pero debe integrarse en la evaluación diagnóstica de estos casos intermedios.
3. Resultado positivo: valores 6 mg/dL (![]() 360
360 ![]() mol/L). Estos resultados indican alta sospecha de fenilcetonuria clásica. Se debe notificar como caso probable, realizar confirmación diagnóstica urgente e iniciar de manera inmediata el tratamiento con dieta restringida en fenilalanina.
mol/L). Estos resultados indican alta sospecha de fenilcetonuria clásica. Se debe notificar como caso probable, realizar confirmación diagnóstica urgente e iniciar de manera inmediata el tratamiento con dieta restringida en fenilalanina.
Esta clasificación permite una estratificación más precisa del riesgo, reduce la ambigüedad en la toma de decisiones clínicas y garantiza una respuesta proporcional al nivel de sospecha diagnóstica.
Tabla 6. Clasificación de resultados del tamizaje para fenilcetonuria
| Resultado | Valor de fenilalanina | Interpretación | Acciones recomendadas |
| Negativo | < 2 mg/dL (<120 | Resultado normal. No hay evidencia bioquímica de fenilcetonuria ni de hiperfenilalaninemia. | No se requiere seguimiento adicional, salvo factores clínicos o antecedentes familiares relevantes. |
| Zona gris / Indeterminado | 2 mg/dL a 5.9 mg/dL (120-360 | Resultado indeterminado Podría corresponder a formas leves de hiperfenilalaninemia. Reporte como caso probable. | Realizar confirmación diagnóstica (aminoácidos cuantitativos en plasma), seguimiento clínico, sin iniciar tratamiento de forma inmediata, posible estudio de ADN. |
| Positivo | | Alta sospecha de fenilcetonuria clásica. Reporte como caso probable. | Notificar como caso probable, realizar confirmación diagnóstica urgente, inicio temprano del tratamiento. |
(14)
El resultado del tamizaje neonatal para fenilcetonuria puede verse influido por diversas condiciones neonatales, perinatales o maternas que general falsos positivos o negativos, afectando su interpretación. Estas condiciones deben ser registradas en la historia clínica y en la tarjeta para la toma de la muestra. A continuación, se describen los principales escenarios y las recomendaciones asociadas.
Tabla 7. Consideraciones clínicas que requieren análisis individual del resultado del tamizaje de fenilcetonuria (PKU)
| Grupo poblacional | Riesgo a considerar | Recomendación |
| Recién nacido prematuro (menor de 37 semanas) y/o con bajo peso al nacer menor de 2.000 gramos. | Mayor probabilidad de falsos positivos por inmadurez hepática, menor masa corporal y alteración en la homeostasis proteica. | Valorar repetición del tamizaje entre los 7 y 14 días de vida, tras inicio adecuado de alimentación, y confirmar con perfil de aminoácidos en plasma si el resultado es límite. |
| Recién nacido con nutrición parenteral total. | Puede producir falsos positivos por sobrecarga proteica, así como falsos negativos si la nutrición no fenilalanina. | De ser posible, evitar tomar eltamizajedurantelaadministracióndenutriciónparenteral total. Si no, repetir lamuestra dentro de las 48 horasposterioresaliniciodealimentaciónenteralconproteína natural. |
| Recién nacido con alimentación especial (fórmulas hidrolizadas, exentas de fenilalanina, leche deslactosada). | Riesgo de falsos negativos, especialmente si se inicia la fórmula especial ante de tomar la muestra. | Registrar el tipo de alimentación y evaluar si es necesario repetir la muestra tras mínimo 3 tomas de fórmula estándar o leche materna, o al cambiar la alimentación. |
| Reciénnacidoconsepsisneonatal,eventoshipóxicos,ventilaciónmecánicareanimación ometabólicoestrés | Las alteraciones inespecíficas en el metabolismo pueden generar resultados falsamente elevados. | Repetir tamizaje en condiciones estables. Si el resultado es positivo, avanzar de inmediato a confirmación diagnóstica en plasma y pruebas moleculares. |
| Recién nacido con transfusión previa a la toma de la muestra. | Riesgo de falsos negativos por dilución de la sangre del neonato. | Evitar la toma dentro de las 48 a 72 horas post transfusión. Si ya se realizó la toma, repetir el tamizaje a los 7 a 10 días. |
| Gemelos o múltiples. | Las diferencias en la alimentación, metabolismo o peso pueden llevar a resultados discordantes. Considerar el riesgo de dilución cruzada en muestras mal identificadas. | Debe realizarse el etiquetado riguroso de cada muestra, repetir si hay duda, y analizar cada caso por separado. |
| Recién nacido hijo de madre con fenilcetonuria no controlada durante el embarazo. | Niveles altos de fenilalanina materna pueden provocar niveles artificialmente altos en el recién nacidos en las primeras horas de vida, sin que el neonato tenga PKU. | Repetir la muestra tras 48 horas de alimentación, considerar pruebas moleculares si persiste hiperfenilalaninemia. |
| Recién nacido hijo de madre con dieta vegana estricta o con restricción proteica. | Se ha documentado una reducción significativa del aporte fetal de fenilalanina durante la gestación. Se puede producir niveles bajos de fenilalanina en sangre, especialmente si el tamizaje se realiza en las primeras 24 a 48horas, generando un riesgo de falsos negativos. | Se debe asegurar que el recién nacido haya recibido al menos 24 horas de alimentación enteral con leche materna o fórmula estándar antes de la toma del tamizaje. No es recomendable realizar la toma en las primeras 24 horas de vida. |
(15) (10)
Al ser positivo este tamizaje se considera paciente como caso probable de Fenilcetonuria y deberá ser inmediatamente notificado al SIVIGILA de acuerdo con el protocolo y lineamientos nacionales emitidos por el Instituto Nacional de Salud.
A todo recién nacido con prueba de tamizaje alterada se le debe garantizar la confirmación o descarte de la patología EN EL MENOR TIEMPO POSIBLE, lo que garantiza incidir en los resultados en salud y desarrollo que son objetivo central del tamizaje neonatal.
Confirmación diagnóstica de fenilcetonuria
A todo niño o niña con un resultado positivo en el tamizaje para fenilcetonuria, debe tomarse la prueba diagnóstica de cuantificación de aminoácidos en plasma (Descripción CUPS AMINOÁCIDOS CUANTITATIVOS), la cual permite cuantificar los niveles plasmáticos de fenilalanina y tirosina, para calcular la relación fenilalanina/tirosina (Phe/Tyr). Esta relación proporciona mayor especificidad en el diagnóstico, ya que en la fenilcetonuria clásica se presenta un aumento marcado de la fenilalanina con valores bajos o normales de tirosina, resultando en una relación Phe/Tyr generalmente superior a 4-5. Esta información es útil también para diferenciar la PKU de otras causas de hiperfenilalaninemia, como errores secundarios del metabolismo hepático o situaciones transitorias.
Un valor de fenilalanina plasmática mayor de 360 ![]() mol/L (6 mg/dL) se considera un valor de referencia para indicar la necesidad de iniciar tratamiento dietario. Valores mayores de 600
mol/L (6 mg/dL) se considera un valor de referencia para indicar la necesidad de iniciar tratamiento dietario. Valores mayores de 600 ![]() mol/L, especialmente si se acompañan de una relación fenilalanina/tirosina superior a 4, confirman con alta probabilidad el diagnóstico de PKU. En casos con niveles plasmáticos mayores de 1200
mol/L, especialmente si se acompañan de una relación fenilalanina/tirosina superior a 4, confirman con alta probabilidad el diagnóstico de PKU. En casos con niveles plasmáticos mayores de 1200 ![]() mol/L, la posibilidad de falso positivo es prácticamente nula y se debe iniciar tratamiento sin demora. Por otro lado, niveles inferiores a 120
mol/L, la posibilidad de falso positivo es prácticamente nula y se debe iniciar tratamiento sin demora. Por otro lado, niveles inferiores a 120 ![]() mol/L, con una relación Phe/Tyr menor de 2, permiten descartar con seguridad la enfermedad, interpretándose como un falso positivo o una elevación transitoria no clínicamente relevante.
mol/L, con una relación Phe/Tyr menor de 2, permiten descartar con seguridad la enfermedad, interpretándose como un falso positivo o una elevación transitoria no clínicamente relevante.
Tabla 8. Confirmación diagnóstica de fenilcetonuria.
| Resultado de aminoácidos en plasma | Relación fenilalanina / tirosina (Phe/Tyr) | Interpretación clínica | Recomendación |
| < 2 | Resultado normal | Descartar PKU. No requiere tratamiento ni seguimiento especial. | |
 | 2 – 4 | Posible hiperfenilalaninemia leve o transitoria | Repetir prueba; evaluar factores asociados (prematuridad, infección, alimentación); considerar seguimiento. |
| 2 | Compatible con hiperfenilalaninemia sostenida o PKU leve | Confirmar con cuantificación repetida; iniciar orientación dietaria si se mantiene elevado. | |
| 4 | Altamente sugestivo de PKU moderada o clásica | Confirmar diagnóstico. Iniciar tratamiento. | |
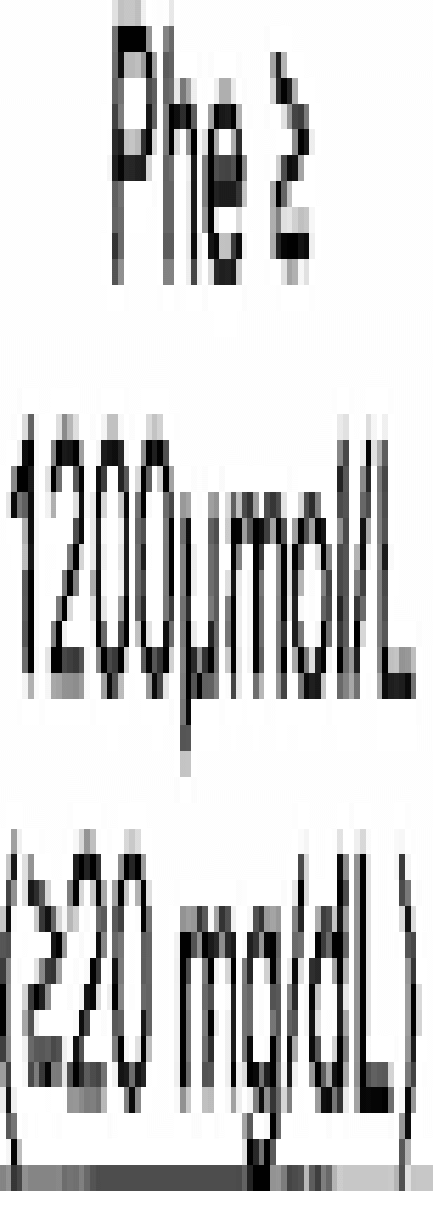 | 5 | PKU clásica prácticamente confirmada | Iniciar tratamiento inmediato sin esperar confirmación adicional. |
(13)
Si este examen diagnóstico es positivo, el paciente se considera como caso confirmado para Fenilcetonuria y deberá iniciarse el tratamiento inmediatamente.
El diagnóstico clínico y bioquímico es suficiente para iniciar tratamiento en fenilcetonuria, se recomienda la incorporación del análisis molecular en el Programa de Tamizaje Neonatal, como estrategia de confirmación diagnóstica definitiva, así como clasificar con mayor precisión la severidad bioquímica, y en algunos casos, predecir la respuesta a terapias específicas. El análisis genético aporta información útil para el asesoramiento genético familiar, evaluación de portadores, planificación reproductiva y registro poblacional de mutaciones en Colombia.
Si bien la integración del análisis molecular contribuye a la calidad, trazabilidad y personalización del tratamiento a largo plazo, en consonancia con estándares internacionales de programas de enfermedades huérfanas y errores innatos del metabolismo; no debe retrasarse el inicio de tratamiento por la toma o resultado de esta prueba.
Una vez diagnosticada la patología, el paciente se considera como caso confirmado por laboratorio y deberá ser inmediatamente ajustada la ficha de notificación de acuerdo con los protocolos y lineamientos emitidos por el Instituto Nacional de Salud.
Igualmente, será de obligatorio cumplimiento el reporte inmediato del resultado positivo y negativo de la prueba confirmatoria al repositorio de tamizaje neonatal, administrado por el INS.
Tratamiento inicial (Plan de cuidado inicial)
El objetivo principal del tratamiento en la fenilcetonuria es prevenir el daño neurológico irreversible causado por la acumulación tóxica de fenilalanina en el sistema nervioso central, garantizando así un desarrollo neurocognitivo y psicosocial adecuado. Se ha estimado que cada 4 semanas de retraso en el inicio del tratamiento puede reducir el coeficiente intelectual en aproximadamente 4 puntos, lo que subraya la urgencia de instaurar el tratamiento en los primeros días de vida.
El tratamiento debe iniciarse tan pronto como se confirme el diagnóstico. Sin embargo, en casos con niveles de fenilalanina ![]() 1200
1200 ![]() mol/L (
mol/L (![]() 20 mg/dL), se recomienda iniciar tratamiento de forma inmediata, de forma paralela con la toma de pruebas diagnósticas y mientras se cuenta con el resultado, ya que estos valores son altamente predictivos de fenilcetonuria clásica. De hecho, la probabilidad de que un nivel igual o superior a 1200
20 mg/dL), se recomienda iniciar tratamiento de forma inmediata, de forma paralela con la toma de pruebas diagnósticas y mientras se cuenta con el resultado, ya que estos valores son altamente predictivos de fenilcetonuria clásica. De hecho, la probabilidad de que un nivel igual o superior a 1200 ![]() mol/L no corresponda a un caso real de PKU clásica es extremadamente baja o virtualmente nula.
mol/L no corresponda a un caso real de PKU clásica es extremadamente baja o virtualmente nula.
Esta estrategia de intervención temprana busca evitar la toxicidad metabólica durante la ventana crítica del neurodesarrollo. El tratamiento debe iniciarse bajo la orientación de personal entrenado, garantizando remisión temprana con especialistas en errores innatos del metabolismo. (10)
Se recomienda el inicio del siguiente plan de cuidado mientras se deriva al paciente al control por parte de profesionales de errores innatos del metabolismo o centros de referencia de enfermedades huérfanas:
Intervenciones iniciales para pacientes neonatos con fenilcetonuria:
- Valoración médica y nutricional inmediata: El paciente deberá contar con una valoración integral que incluya examen físico, medidas antropométricas, evaluación neurológica básica y condiciones de alimentación. Inicialmente la realizará el médico que realiza la interpretación y valoración del niño o la niña con fenilcetonuria confirmada, sin embargo, es importante tener en cuenta que estos pacientes deben tener control con un equipo interdisciplinario que incluya pediatría, neonatología, genética, neurología pediátrica, gastroenterología pediátrica y nutrición con formación en errores innatos del metabolismo. El profesional de nutrición debe participar desde el inicio del plan alimentario, incluyendo la selección del tipo y volumen de fórmula libre de fenilalanina, el diseño del esquema mixto con lactancia materna, y el cálculo del aporte proteico total. La atención por nutrición general o no especializada no es suficiente ni recomendable en esta etapa. (15)
- Inicio de dieta controlada en fenilalanina: Los niños o niñas con niveles de fenilalanina en sangre 360 ![]() mol/L (6 mg/dL) deben iniciar tratamiento con una dieta controlada en fenilalanina, que incluye la combinación cuidadosa entre leche materna o fórmula estándar y una fórmula especial libre de fenilalanina.
mol/L (6 mg/dL) deben iniciar tratamiento con una dieta controlada en fenilalanina, que incluye la combinación cuidadosa entre leche materna o fórmula estándar y una fórmula especial libre de fenilalanina.
Los niños o niñas con niveles de fenilalanina ![]() 1200
1200 ![]() mol/L (
mol/L (![]() 20 mg/dL) deben iniciar inmediatamente la fórmula libre de fenilalanina como principal fuente de nutrición, mientras se confirman los resultados diagnósticos, ya que este valor sugiere fuertemente una fenilcetonuria clásica.
20 mg/dL) deben iniciar inmediatamente la fórmula libre de fenilalanina como principal fuente de nutrición, mientras se confirman los resultados diagnósticos, ya que este valor sugiere fuertemente una fenilcetonuria clásica.
Esta fórmula no debe ser utilizada como única fuente de alimentación, ya que no contiene fenilalanina ni otros aminoácidos esenciales en su forma intacta (como tirosina o triptófano), y su uso exclusivo puede llevar a deficiencias nutricionales graves, detención del crecimiento o descompensaciones metabólicas.
No obstante, en situaciones excepcionales, como niveles iniciales muy elevados de fenilalanina, 1500 ![]() mol/L, se puede emplear de manera transitoria y controlada la fórmula libre de fenilalanina como única fuente de alimentación, con el objetivo de reducir rápidamente la toxicidad. En estos casos, se recomienda realizar controles bioquímicos cada 24 horas y reintroducir una fuente natural de fenilalanina tan pronto como los niveles plasmáticos desciendan por debajo de 600
mol/L, se puede emplear de manera transitoria y controlada la fórmula libre de fenilalanina como única fuente de alimentación, con el objetivo de reducir rápidamente la toxicidad. En estos casos, se recomienda realizar controles bioquímicos cada 24 horas y reintroducir una fuente natural de fenilalanina tan pronto como los niveles plasmáticos desciendan por debajo de 600 ![]() mol/L, para evitar el riesgo de deficiencia de este aminoácido esencial.
mol/L, para evitar el riesgo de deficiencia de este aminoácido esencial.
El volumen y proporción entre fórmula especial y alimentación natural se ajustará progresivamente según niveles plasmáticos y ganancia de peso. En lactantes a término, se espera que los niveles de fenilalanina disminuyan aproximadamente 300-400 ![]() mol/L por día con intervención adecuada.
mol/L por día con intervención adecuada.
El cálculo del aporte proteico total y el ajuste de la fenilalanina deben ser dirigidos por un nutricionista especializado en errores innatos del metabolismo.
La dieta debe ser prescrita y supervisada por un equipo especializado en errores innatos del metabolismo, con cálculo preciso del aporte proteico total, seguimiento clínico estrecho y ajustes permanentes según edad, crecimiento y evolución de niveles plasmáticos de fenilalanina.
La meta bioquímica del tratamiento debe ser mantener los niveles plasmáticos de fenilalanina entre 120 y 360 ![]() mol/L (2 a 6 mg/dL) en niños y niñas menores de 12 años. En adolescentes mayores y adultos, el rango puede extenderse hasta 600
mol/L (2 a 6 mg/dL) en niños y niñas menores de 12 años. En adolescentes mayores y adultos, el rango puede extenderse hasta 600 ![]() mol/L (10 mg/dL) en pacientes estables y bien controlados.
mol/L (10 mg/dL) en pacientes estables y bien controlados.
Es fundamental establecer no solo el rango superior aceptable, sino también un límite inferior de seguridad. Se considera que niveles plasmáticos de fenilalanina por debajo de 30 ![]() mol/L (0,5 mg/dL) son potencialmente peligrosos, especialmente en neonatos y lactantes, ya que pueden interferir con el crecimiento, la mielinización y el desarrollo neurológico. Por lo tanto, el tratamiento debe evitar tanto la hiperfenilalaninemia (360 pmol/L en menores de 12 años) como la hipofenilalaninemia (<30
mol/L (0,5 mg/dL) son potencialmente peligrosos, especialmente en neonatos y lactantes, ya que pueden interferir con el crecimiento, la mielinización y el desarrollo neurológico. Por lo tanto, el tratamiento debe evitar tanto la hiperfenilalaninemia (360 pmol/L en menores de 12 años) como la hipofenilalaninemia (<30 ![]() mol/L), ajustando cuidadosamente la dieta para mantener el equilibrio nutricional.
mol/L), ajustando cuidadosamente la dieta para mantener el equilibrio nutricional.
Niveles por debajo de 120 ![]() mol/L también deben evitarse debido al riesgo de desnutrición proteica y déficit de aminoácidos esenciales. La vigilancia bioquímica regular es esencial para mantener estos rangos y ajustar la dieta de forma personalizada. (14)
mol/L también deben evitarse debido al riesgo de desnutrición proteica y déficit de aminoácidos esenciales. La vigilancia bioquímica regular es esencial para mantener estos rangos y ajustar la dieta de forma personalizada. (14)
- Monitoreo antropométrico: Se indica control semanal de peso durante el primer mes de vida, vigilando ganancia ponderal. Tener en cuenta la pérdida de peso fisiológica que se da los primeros 7 días de vida sin que esta supere el 10% de pérdidas.
- En el contexto del seguimiento nutricional inicial en fenilcetonuria, se recomienda utilizar las curvas lntergrowth-21st para recién nacidos, tanto prematuros como a término, dado que ofrecen una mejor estandarización internacional basada en población saludable y permiten ajustes según edad gestacional. Las curvas Fenton aún son una opción válida para prematuros en unidades neonatales. Las curvas de crecimiento de la OMS 2006 deben utilizarse a partir de los 2 meses de vida para el seguimiento longitudinal en niños nacidos a término. Es importante no emplear exclusivamente las curvas OMS en neonatos prematuros antes de que alcancen las 40 semanas, ya que pueden subestimar o sobrestimar el crecimiento esperado.
- Monitoreo bioquímico de fenilalanina: Se deben medir los niveles de fenilalanina plasmática (Descripción CUPS FENILALANINA CUANTITATIVA) dos (2) veces a la semana hasta lograr niveles estables durante el primer mes de vida. Posteriormente, los controles pueden espaciarse a cada 1-2 semanas en el primer trimestre y luego controlar 1 vez al mes. Debe evitarse que los niveles desciendan por debajo de 120 ![]() mol/L y mantenerse idealmente entre 120-360
mol/L y mantenerse idealmente entre 120-360 ![]() mol/L en menores de 1 año.
mol/L en menores de 1 año.
- Se debe fomentar la lactancia materna, ya que en los niños y niñas que la reciben logran un mejor crecimiento, una adecuada ganancia de peso y un control aceptable de niveles de fenilalanina en sangre, esta práctica debe ir acompañada de la fórmula infantil libre de fenilalanina.
Se recomienda el suministro primero del volumen calculado de fórmula y luego permitir lactancia directa hasta saciedad. Si no es posible lactancia directa, se puede usar leche materna extraída con medidas adecuadas de bioseguridad y conservación. El volumen de fórmula libre de fenilalanina debe calcularse con base en la edad, peso y nivel plasmático de fenilalanina, en coordinación con el equipo especializado. El aporte de fenilalanina en la leche materna es aproximadamente de 46 mg por 100 ml. La madre con diagnóstico de PKU puede amamantar, siempre que su control metabólico sea adecuado. (16)
- Se recomienda que la administración de la formula libre de fenilalanina deberá suministrarse con taza, cuchara o con jeringa, nunca deben ser alimentados con biberones. El uso del biberón es válido si no hay contraindicaciones específicas. Además, forzar otras técnicas puede interferir con el desarrollo neurosensorial, oral y de la succión. Se debe instruir a los padres a que lleven un registro diario del volumen de fórmula metabólica, así como las tomas administradas y eventos clínicos asociados. Este registro debe ser revisado en cada control.
- Indicaciones de hospitalización: Cualquier neonato con signos de descompensación (letargia, vómito persistente, convulsión, rechazo al alimento, hipotermia o hipotonía) debe hospitalizarse para evaluación metabólica, hidratación y manejo multidisciplinario.
El médico tratante podrá indicar estudios adicionales según la condición clínica del paciente.
Seguimiento inicial para pacientes diagnosticados con fenilcetonuria
El seguimiento clínico inicial de los recién nacidos con diagnóstico confirmado de fenilcetonuria debe ser realizado por un equipo interdisciplinario, liderado por un médico pediatra o neonatólogo, con apoyo de telesalud de especialistas en errores innatos del metabolismo. El médico general no debe asumir en solitario el manejo de estos pacientes, salvo que haya recibido entrenamiento específico y cuente con un sistema de apoyo formal (como telemedicina). Esta medida busca evitar errores en el ajuste dietético, seguimiento bioquímico y decisiones terapéuticas que podrían tener consecuencias neurológicas irreversibles.
Desde el inicio, se debe garantizar la participación de:
- Pediatra o neonatólogo.
- Médico genetista.
- Nutrición clínica especializada en errores innatos del metabolismo, para ajustar la dieta, evitar deficiencias y asegurar el cumplimiento de las metas bioquímicas.
- Neurología pediátrica, para evaluación de desarrollo neurológico y detección temprana de signos de daño.
- Psicología y trabajo social, según disponibilidad, para acompañamiento familiar, adherencia al tratamiento y afrontamiento emocional.
El seguimiento debe establecerse con una periodicidad definida (por ejemplo, controles semanales o quincenales durante el primer mes, luego mensuales), y debe incluir:
- Valoración integral.
- Examen neurológico.
- Control bioquímico establecido por el profesional tratante.
- Valoración de adherencia al tratamiento y educación continua a la familia.
Figura 3. Esquema de tamizaje neonatal de fenilcetonuria.
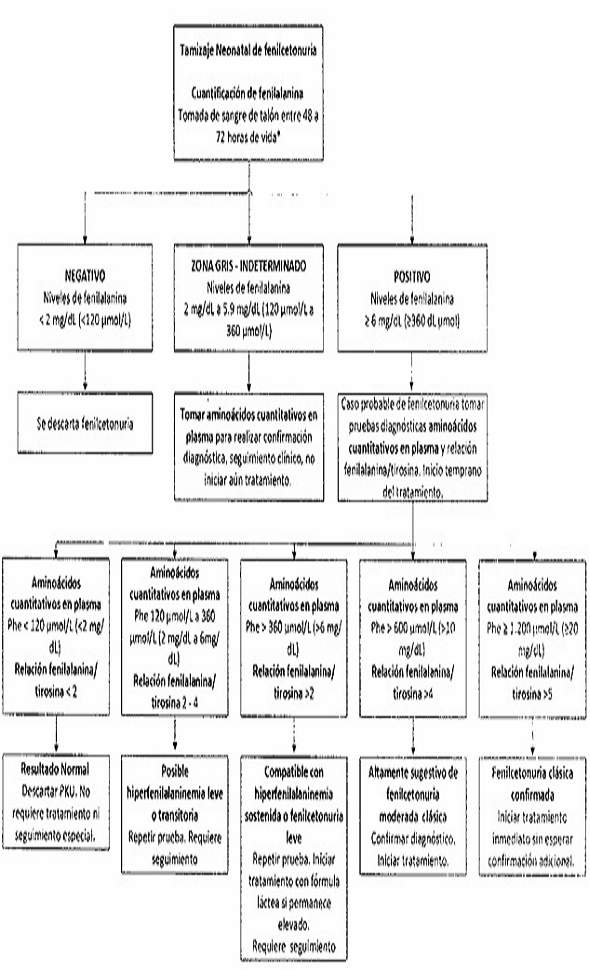
Consideraciones descritas en el apartado 4.1. - componente preanalítico. Fuente: Elaboración propia a partir de literatura referenciada.
Se establecen los puntos de corte de acuerdo con los lineamientos establecidos por el Instituto Nacional de Salud, los cuales están sujetos de actualización. (11)
4.1.3 Tamizaje de Galactosemia
Número de identificación de la enfermedad huérfana: 954
La galactosemia es una enfermedad autosómica recesiva caracterizada por la incapacidad de metabolizar la galactosa en glucosa. La galactosa es un azúcar que se encuentra principalmente en la leche y los productos lácteos humanos y bovinos como parte del disacárido lactosa. La lactosa es hidrolizada a glucosa y galactosa por la enzima intestinal lactasa. La galactosa luego se convierte en glucosa para su uso como fuente de energía.
Tipos de galactosemia
- Deficiencia de galactosa-1 -fosfato uridil transferasa (GALT): la forma más común y grave de galactosemia es causada por la deficiencia de GALT, la enzima que convierte la galactosa- 1-fosfato (galactosa-1-P) en uridina difosfato galactosa (UDPgalactosa). La deficiencia completa de la actividad de GALT se conoce como galactosemia clásica, a menudo denominada con el término aislado "galactosemia". Los pacientes que no reciben tratamiento suelen tener retraso en el crecimiento pondoestatural, ictericia colestásica, hepatomegalia, disfunción hepática y renal, encefalopatía, sepsis principalmente por Escherichia coliy muerte temprana.
Se han descrito múltiples variantes alélicas, con diferentes repercusiones clínicas que van desde la casi normalidad en la variante denominada galactosemia Duarte (a la cual no se le da tratamiento), a graves síntomas en las variantes Indiana o Rennes.
- Deficiencia de galactoquinasa (GALK): Es la primera enzima en la vía del metabolismo de la galactosa, que convierte la galactosa en galactosa-1-P. La principal consecuencia de la deficiencia de GALK es el desarrollo de cataratas, los otros signos de galactosemia están ausentes. Los mecanismos patogénicos subyacentes a este defecto localizado no están claros.
- Deficiencia de uridina difosfato (UDP) galactosa 4-epimerasa (GALE): GALE convierte UDPgalactosa en UDPglucosa. En la mayoría de los pacientes con deficiencia de GALE (o epimerasa), el defecto se localiza en los glóbulos rojos (GR). Los mecanismos patogénicos subyacentes a este defecto limitado no están claros. Estos individuos suelen tener un crecimiento y desarrollo normales, mientras que los pacientes con deficiencia generalizada de GALE tanto en los glóbulos rojos como en todos los demás tejidos presentan síntomas similares a los de la galactosemia clásica. Presentan un cuadro clínico variable que incluye los signos habituales de galactosemia: hipotonía, mala alimentación, vómitos, pérdida de peso, ictericia y complicaciones como retraso del crecimiento, déficit cognitivo y cataratas.
De acuerdo con el portal de información de Orphanet no se conoce la prevalencia general. La incidencia anual de la galactosemia clásica está estimada en 1/40.000-1/60.000 en los países occidentales. La incidencia parece ser variable en otros grupos étnicos con una tasa más alta descrita en la población de nómadas irlandeses, debido probablemente a la consanguinidad. Incidencia anual de galactosemia clásica en Europa y Norte América 1:40.000 - 1:80.000. América Latina 1:80.000- 1:100.000.
De acuerdo con el Registro Nacional de Personas con Enfermedad Huérfana desde el año 2011 se han reportado 36 casos, la mayoría del género masculino con un total de 19 casos en comparación con el género femenino con 14 casos.
| Prevalencia | 1:40.000-60.000 |
| Edad promedio diagnóstico (Meses) | 1 mes |
| Resultado en Salud a incidir con el tamizaje | Discapacidad cognitiva, trastornos del desarrollo, sensoriales y mortalidad |
La mayoría de los bebés afectados nacen con un aspecto saludable, pero experimentan un deterioro rápido y devastador después de la exposición a la leche materna o fórmula láctea, que contiene grandes cantidades de galactosa. Los síntomas agudos pueden progresar en cuestión de días desde ictericia, vómitos, hepatomegalia, alimentación deficiente, retraso en el crecimiento, letargo, diarrea o sepsis.
Si no se retira la lactosa, el metabolito tóxico como el galactitol se acumula a nivel de otros órganos como el cerebro, hígado y riñón puede originar mala absorción tubular renal, cirrosis, insuficiencia hepática o edema cerebral. La mayoría de los neonatos con galactosemia clásica desarrollan sintomatología característica de la enfermedad en las primeras dos semanas de vida y la mayoría de los casos graves y muertes por septicemia se producen en este periodo. (17) (18) (19)
Objetivos de la línea de tamizaje de galactosemia
- Detectar de forma temprana niños y niñas recién nacidos vivos con concentraciones elevadas de galactosa en muestra de talón, sugestivas de galactosemia con el fin de confirmar o descartar el diagnóstico oportunamente.
- Iniciar precozmente el tratamiento dietético en los casos confirmados, minimizando los riesgos asociados y mejorando el pronóstico a largo plazo.
- Establecer lineamientos técnicos claros para el seguimiento de casos sospechosos y confirmados, incluyendo la articulación con genética médica, nutrición especializada y pediatría.
- Identificar condiciones clínicas o factores de riesgo que puedan requerir un abordaje diferenciado o intensificado del seguimiento.
- Articular la línea de tamizaje con los procesos de confirmación diagnóstica, inicio de tratamiento y seguimiento clínico dentro de una ruta de atención integral centrada en el paciente.
Respecto al resultado obtenido, el tamizaje puede definirse como:
- Tamizaje positivo para Galactosemia: recién nacido con niveles de galactosa total por encima del punto de corte establecido ( ![]() 10mg/dL) en muestra de sangre de talón), los cuales son considerados casos probables de galactosemia.
10mg/dL) en muestra de sangre de talón), los cuales son considerados casos probables de galactosemia.
- Tamizaje negativo de Galactosemia: recién nacido con niveles de galactosa por debajo de 10mg/dL o del establecido menor al punto de corte.
El tamizaje de galactosemia será interpretado por un profesional en pediatría, neonatología o profesional en medicina general entrenado en la interpretación de los resultados del tamizaje metabólico básico.
Para efectos de la evaluación y tratamiento del Programa de Tamizaje Neonatal, se emplearán las siguientes definiciones en relación con la confirmación diagnóstica para galactosemia:
- Rellamado: procedimiento de llamado o citación activa de los pacientes y su familia ante un resultado de tamizaje metabólico positivo, con el fin de realizar pruebas confirmatorias y definir la conducta diagnóstica y terapéutica.
- Diagnóstico confirmado de Galactosemia: condición establecida cuando un recién nacido con tamizaje positivo y con reporte de disminución de la actividad de Galactosa 1- fosfato uridil transferasa o prueba molecular compatible con el cuadro.
- Diagnóstico descartado de Galactosemia: condición en la cual, tras el resultado de tamizaje positivo, no hay alteración en pruebas confirmatorias.
Se especifican las siguientes definiciones relacionadas con la atención terapéutica del paciente con diagnóstico confirmado:
- Niño o niña con tratamiento: niño o niña con diagnóstico confirmado de galactosemia que ha iniciado manejo con fórmula láctea especial, según lo indicado por el equipo médico tratante.
- Niño o niña sin tratamiento: niño o niña con diagnóstico confirmado de galactosemia que no ha recibido fórmula especial ni ninguna intervención terapéutica orientada al control de los niveles de galactosa.
- Niño o niña sin información de tratamiento: niño o niña con diagnóstico confirmado de galactosemia en quien no se cuenta con información sobre el inicio y la continuidad del tratamiento.
Respecto a la continuidad del cuidado, se establecen los siguientes conceptos:
- Niño o niña con seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de galactosemia quien tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de especialista con abordaje de su condición de mayor riesgo, según lo señalado en la RPMS.
- Niño o niña sin seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de galactosemia quien no tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de especialista con abordaje de su condición de mayor riesgo, según lo señalado en la RPMS.
Tecnología del tamizaje neonatal de galactosemia
El tamizaje neonatal para galactosemia debe realizarse mediante la punción de talón, recolectando sangre en papel filtro. La prueba para tamizaje que se consideró es la cuantificaclón de galactosa total en sangre (Descripción CUPS: Galactosa Cuantitativa), el punto de corte para tamizaje positivo es ![]() 10mg/dL.
10mg/dL.
Si bien se recomienda que la toma de la muestra se realice entre las 48 y 72 horas de vida, asegurando que el recién nacido haya recibido alimentación previa (mínimo tres tomas), lo cual es indispensable para evitar falsos negativos; en el caso de Colombia está indicada una sola toma de muestra para las 7 patologías, la cual debe desarrollarse entre las 48 y 72 horas con las consideraciones descritas en el apartado 4.1. - componente preanalítico. El tiempo máximo para la toma de la muestra debe ser de 5 días de vida.
Al ser positivo este tamizaje se considera paciente como caso probable de Galactosemia y deberá ser inmediatamente notificado de acuerdo con las indicaciones y orientaciones que emita el Instituto Nacional de Salud.
A todo recién nacido con prueba de tamizaje alterada se le debe garantizar la confirmación o descarte de la patología EN EL MENOR TIEMPO POSIBLE, lo que garantiza incidir en los resultados en salud y desarrollo que son objetivo central del tamizaje neonatal.
Confirmación diagnóstica de galactosemia
A todo niño o niña con un resultado positivo en el tamizaje para galactosemia, debe tomarse la prueba diagnóstica de medición de la actividad enzimática de la Galactosa 1- fosfato Uridil transferasa (Descripción CUPS: GALACTOSA 1 - FOSFATO URIDIL TRANSFERASA ACTIVIDAD), con el fin de confirmar la patología e iniciarse inmediatamente la fórmula de soya o aquella que no tenga lactosa o galactosa o disacáridos que se puedan transformar en estos azúcares, suspendiendo la leche materna.
Si el reporte de disminución de la actividad de Galactosa 1-fosfato uridil transferasa o prueba molecular son compatibles con el cuadro, el paciente se considera como caso confirmado para Galactosemia.
El diagnóstico clínico y bioquímico es suficiente para iniciar tratamiento en galactosemia, se recomienda la incorporación del análisis molecular en el Programa de Tamizaje Neonatal, como estrategia de confirmación diagnóstica, así como clasificar con mayor precisión la severidad bioquímica, y en algunos casos, predecir la respuesta a terapias específicas. El análisis genético aporta información útil para el asesoramiento genético familiar, evaluación de portadores, planificación reproductiva y registro poblacional de mutaciones en Colombia. Si bien la integración del análisis molecular contribuye a la calidad, trazabilidad y personalización del tratamiento a largo plazo, en consonancia con estándares internacionales de programas de enfermedades huérfanas y errores innatos del metabolismo; no debe retrasarse el inicio de tratamiento por la toma o resultado de esta prueba.
El análisis cuantitativo de la actividad GALT de los glóbulos rojos puede verse afectado hasta por tres meses por la transfusión de glóbulos rojos de un donante normal. En tales casos, la prueba molecular es necesaria.
Una vez diagnosticada la patología, el paciente se considera como caso confirmado por laboratorio y deberá ser inmediatamente ajustada la ficha de notificación de acuerdo con las indicaciones y orientaciones que emita el Instituto Nacional de Salud.
Igualmente, será de obligatorio cumplimiento el reporte inmediato del resultado positivo y negativo de la prueba confirmatoria al repositorio de tamizaje neonatal, administrado por el INS.
Tratamiento inicial (Plan de cuidado inicial)
El tratamiento debe iniciarse tan pronto como se confirme el diagnóstico. Una vez identificados por un resultado positivo, los pacientes a quienes se confirma galactosemia, la intervención recomendada es continuar con la restricción dietaría de galactosa de por vida. Incluir suplementación de calcio, fosforo, hierro y Vitamina D. Estos suplementos deben ser adaptados con base en la fórmula de alimentación proporcionada.
Se recomienda el inicio del siguiente plan de cuidado mientras se deriva al paciente al control por parte de profesionales de errores innatos del metabolismo o centros de referencia de enfermedades huérfanas:
- Valoración médica y nutricional inmediata: El paciente deberá contar con una valoración integral que incluya examen físico, medidas antropométricas y condiciones de alimentación. Inicialmente la realizará el médico que realiza la interpretación y valoración del niño o la niña con galactosemia confirmada, sin embargo, es importante tener en cuenta que estos pacientes deben tener control con un equipo interdisciplinario que incluya pediatría, neonatología, genética, gastroenterología pediátrica y nutrición con formación en errores innatos del metabolismo.
El profesional de nutrición debe participar desde el inicio del plan alimentario, incluyendo la selección del tipo y volumen de fórmula láctea.
La atención por nutrición general o no especializada no es suficiente ni recomendable en esta etapa. (20) (21)
Está contraindicada la lactancia materna para estos pacientes
- En el contexto del seguimiento nutricional inicial en galactosemia, se recomienda utilizar las curvas lnterqrowth-21st para recién nacidos, tanto prematuros como a término, dado que ofrecen una mejor estandarización internacional basada en población saludable y permiten ajustes según edad gestacional. Las curvas Fenton aún son una opción válida para prematuros en unidades neonatales. Las curvas de crecimiento de la QMS 2006 deben utilizarse a partir de los 2 meses de vida para el seguimiento longitudinal en niños nacidos a término. Es importante no emplear exclusivamente las curvas OMS en neonatos prematuros antes de que alcancen las 40 semanas, ya que pueden subestimar o sobrestimar el crecimiento esperado.
- Formulas Infantiles de proteína de soya o aquella que no contenga lactosa, galactosa o disacáridos que se puedan transformar en estos carbohidratos. Restricción dietaría de galactosa de por vida. (22) (19)
- Se recomienda que la administración de la formula la formula infantil de soya deberá suministrarse con taza, cuchara o con jeringa, nunca deben ser alimentados con biberones. El uso del biberón es válido si no hay contraindicaciones específicas. Además, forzar otras técnicas puede interferir con el desarrollo neurosensorial, oral y de la succión.
El médico tratante podrá indicar estudios adicionales según la condición clínica del paciente.
Seguimiento inicial para pacientes diagnosticados con galactosemia
El seguimiento clínico inicial de los recién nacidos con diagnóstico confirmado de galactosemia debe ser realizado por un equipo interdisciplinario, liderado por un médico pediatra o neonatólogo, con apoyo de telesalud de especialistas en errores innatos del metabolismo.
El médico general no debe asumir en solitario el manejo de estos pacientes, salvo que haya recibido entrenamiento específico y cuente con un sistema de apoyo formal (como telesalud estructurada). Esta medida busca evitar errores en el ajuste dietético, seguimiento bioquímico y decisiones terapéuticas que podrían tener consecuencias irreversibles.
Desde el inicio, se debe garantizar la participación de:
1. Pediatría o neonatología.
2. Médico genetista.
3. Nutrición clínica especializada en errores innatos del metabolismo, en conjunto con gastroenterología pediátrica para ajustar la dieta, evitar deficiencias y asegurar el cumplimiento de las metas bioquímicas.
4. Psicología y trabajo social, según disponibilidad, para acompañamiento familiar, adherencia al tratamiento y afrontamiento emocional.
5. Neurología.
6. Oftalmología.
El seguimiento clínico y bioquímico debe establecerse con una periodicidad definida (por ejemplo, controles semanales o quincenales durante el primer mes, luego mensuales), y debe incluir:
- Valoración integral.
- Control bioquímico.
- Valoración de adherencia al tratamiento y educación continua a la familia.
Figura 4. Esquema de tamizaje neonatal de galactosemia.
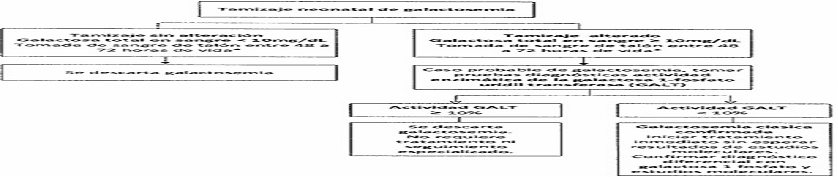
Fuente: Elaboración propia a partir de literatura referenciada. 'Consideraciones descritas en el apartado 4.1. - componente preanalítico.
Se establecen los puntos de corte de acuerdo con los lineamientos establecidos por el Instituto Nacional de Salud, los cuales están sujetos de actualización. (11)
4.1.4 Tamizaie Déficit de Biotinidasa
Número de identificación de la enfermedad huérfana: 522
Es un error congénito autosómico recesivo del metabolismo que conduce a la escasez de biotina. La biotina es una vitamina hidrosoluble del complejo B y es el cofactor esencial de las cuatro carboxilasas humanas: propionil CoA carboxilasa y la metilcrotonil-CoA carboxilasa (catabolismo proteico), acetil-CoA carboxilasa (actúa en el inicio de la síntesis de ácidos grasos) y piruvato carboxilasa (esencial en la gluconeogénesis), su deficiencia da como resultado una deficiencia múltiple de carboxilasa, un trastorno complejo y potencialmente mortal que afecta la gluconeogénesis y el metabolismo de los ácidos orgánicos. Los niveles séricos de biotina dependen de su ingesta en la dieta (donde se encuentra de dos formas, libre y, en mayor cantidad, unida a proteínas) y de su reciclaje endógeno.
La biotina unida a proteína debe ser liberada para ejercer su función. La biotinidasa es un enzima que participa en este proceso. Una de sus funciones principales es reciclar la biotina a partir de la biocitina (biotina unida a proteína) y los biotinil-péptidos procedentes de la degradación de las carboxilasas.
Figura 5. Metabolismo de la biotina
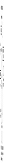
Tomado de: J. Campisto!, M. V. (1996). Déficit de biotinidasa. Forma de presentación y respuesta al tratamiento. ANALES ESPAÑOLES DE PEDIATRIA, 389-392. Obtenido de https://www.aeped.es/sites/default/files/anales/44-4-24.pdf
De acuerdo con el portal de información de Orphanet la prevalencia clínica de la deficiencia de biotinidasa se estima en 1/61.000. La frecuencia de portadores en la población general es, aproximadamente de 1/120.
De acuerdo con el Registro Nacional de Personas con Enfermedad Huérfana desde el año 2018 se han reportado 10 casos, se encuentran con igual distribución para el género femenino y masculino, teniendo 5 casos en cada grupo.
| Prevalencia | 1:61.000 |
| Edad promedio diagnóstico (Meses) | 3 años |
| Resultado en Salud a incidir con el tamizaje | Discapacidad Cognitiva Intelectual |
Aproximadamente el 70% de los niños sintomáticos con déficit total y parcial de biotinidasa presentan convulsiones y a menudo son el síntoma inicial. Habitualmente no responden al tratamiento con fármacos anticonvulsivantes, pero sí al tratamiento con biotina. El déficit profundo de biotinidasa puede provocar los siguientes síntomas:
- Neurológicos: los más frecuentes son hipotonía y convulsiones, ataxia e hipoacusia neurosensorial.
- Dermatológicos: eccema, alopecia.
- Respiratorios: hiperventilación, estridor laríngeo o apnea.
- Oculares: conjuntivitis, alteraciones visuales, como atrofia óptica.
- Infecciones cutáneas virales o fúngicas por afectación del sistema inmune.
- Retraso del desarrollo.
- Alteraciones metabólicas: la mayoría de los niños no tratados presentan alguna de las siguientes alteraciones metabólicas: acidosis láctica, aciduria orgánica o hiperamoniemia leve.
Los síntomas aparecen habitualmente entre la primera semana y los 10 años de vida (media de 3,5 meses), cuando la falta de biotina, por el defecto en su reciclaje y la insuficiente cantidad de biotina libre de la dieta, provoca el déficit de las carboxilasas dependientes de este enzima. Algunos pacientes presentan un único síntoma, mientras que otros presentan múltiples síntomas neurológicos, cutáneos o alteraciones bioquímicas. (23) (24)
Objetivos de la línea de tamizaje de Déficit de Biotinidasa
- Detectar de forma temprana niños y niñas recién nacidos con disminución de la actividad enzimática de la biotinidasa en muestra de sangre de talón, sugestivas de déficit de biotinidasa, con el fin de confirmar o descartar el diagnóstico oportunamente.
- Iniciar precozmente el tratamiento en los casos confirmados, minimizando los riesgos y mejorando el pronóstico a largo plazo.
- Establecer lincamientos técnicos claros para el seguimiento de casos sospechosos y confirmados, incluyendo la articulación interdisciplinaria con el perfil de pediatría.
- Identificar condiciones clínicas o factores de riesgo que puedan requerir un abordaje diferenciado o intensificado del seguimiento.
- Articular la línea de tamizaje con los procesos de confirmación diagnóstica, inicio de tratamiento y seguimiento clínico dentro de una ruta de atención integral centrada en el paciente.
Respecto al resultado obtenido, el tamizaje puede definirse como:
- Tamizaje positivo para Déficit de Biotinidasa: recién nacido con disminución de la actividad enzimática de la biotinidasa por debajo del punto de corte establecido (<58U) en muestra de sangre de talón, los cuales son considerados casos probables.
- Tamizaje negativo para Déficit de Biotinidasa: recién nacido con niveles de actividad enzimática de la biotinidasa por encima del punto de corte establecido. Este resultado no requiere seguimiento adicional, salvo que existan condiciones clínicas especiales o antecedentes familiares relevantes.
El tamizaje para déficit de biotinidasa será interpretado por un profesional en pediatría, neonatología o profesional en medicina general entrenado en la interpretación de los resultados del tamizaje metabólico básico.
Para efectos de la evaluación y tratamiento del Programa de Tamizaje Neonatal, se emplearán las siguientes definiciones en relación con la confirmación diagnóstica para déficit de biotinidasa.
- Rellamado: procedimiento de llamado o citación activa de los pacientes y su familia ante un resultado de tamizaje metabólico positivo, con el fin de realizar pruebas confirmatorias y definir la conducta diagnóstica y terapéutica.
- Diagnóstico confirmado de Déficit de Biotinidasa: condición establecida cuando un recién nacido con tamizaje positivo en muestra de sangre de talón, presenta reporte de la actividad de Biotinidasa sérica positivo.
- Diagnóstico descartado de Déficit de Biotinidasa: condición en la cual, tras el resultado de tamizaje positivo, las pruebas confirmatorias (Actividad enzimática de la biotinidasa sérica) no presentan alteración.
Se especifican las siguientes definiciones relacionadas con la atención terapéutica del paciente con diagnóstico confirmado:
- Niño o niña con tratamiento: niño o niña con diagnóstico confirmado de déficit de biotinidasa que ha iniciado manejo con biotina, según lo indicado por el equipo médico tratante.
- Niño o niña sin tratamiento: niño o niña con diagnóstico confirmado de déficit de biotinidasa que no ha recibido manejo con biotina, ni ninguna intervención terapéutica.
- Niño o niña sin información de tratamiento: niño o niña con diagnóstico confirmado de déficit de biotinidasa del que no se dispone de datos verificables sobre el inicio, tipo o continuidad del tratamiento.
Respecto a la continuidad del cuidado, se establecen los siguientes conceptos:
- Niño o niña con seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de déficit de biotinidasa quien tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de especialista con abordaje de su condición de mayor riesgo, según lo señalado en la RPMS.
- Niño o niña sin seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de déficit de biotinidasa quien no tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de especialista con abordaje de su condición de mayor riesgo según lo señalado en la RPMS.
Tecnología del tamizaje neonatal de Déficit de Biotinidasa
El tamizaje neonatal para déficit de biotinidasa debe realizarse mediante la punción de talón, recolectando sangre en papel filtro La prueba para tamizaje que se consideró es la medición de la actividad enzimática de la biotinidasa (Descripción CUPS: Biotinidasa actividad), el punto de corte para tamizaje positivo es ![]() 58U.
58U.
Si bien se recomienda que la toma de la muestra se realice entre las 24 y 72 horas de vida, asegurando que el recién nacido haya recibido alimentación previa (mínimo tres tomas); en el caso de Colombia está indicada una sola toma de muestra para las 7 patologías, la cual debe desarrollarse entre las 48 y 72 horas con las consideraciones descritas en el apartado 4.1. - componente preanalítico. El tiempo máximo para la toma de la muestra debe ser de 5 días de vida.
Se debe tener en cuenta que las muestras deben estar totalmente secas antes de su envío al laboratorio porque la humedad provoca una pérdida significativa de la actividad enzimática generando un falso positivo. Aproximadamente el 50% de los falsos positivos se producen en prematuros y la mayoría de los restantes se deben a un mal manejo de las muestras, posiblemente por su exposición a unas condiciones excesivas de calor o humedad.
Tabla 9. Consideraciones clínicas que requieren análisis individual del resultado del tamizaje para déficit de biotinidasa.
| Grupo poblacional | Riesgo a considerar |
| Recién nacido prematuro (menor de 37 semanas) y/o con bajo peso al nacer. | Mayor probabilidad de falsos positivos por menor masa corporal. |
| Recién nacido con nutrición parenteral total Puede producir falsos positivos por sobrecarga. | Puede producir falsos positivos por sobrecarga. De ser posible, evitar tomar el tamizaje durante la administración de nutrición parenteral total. Si no, repetir la muestra dentro de las 48 horas posteriores al inicio de alimentación enteral con proteína natural. |
| Recién nacido con ictericia neonatal o hiperbilirrubinemia. | Riesgo de falsos positivos. |
| Recién nacido con disfunción hepática | Riesgo de falsos positivos. |
| Recién nacido en zonas de alta humedad o temperaturas altas. | Riesgo de falsos positivos porque la humedad provoca una pérdida significativa de la actividad enzimática. Almacenar de acuerdo con los lineamientos establecidos por el INS. |
| Recién nacido con transfusiones previas al tamizaje. | Riesgo de falsos negativos. |
(24) (25) (26)
Al ser positivo este tamizaje se considera paciente como caso probable de déficit de biotinidasa y deberá ser inmediatamente notificado al SIVIGILA de acuerdo con el protocolo y lineamientos nacionales emitidos por el Instituto Nacional de Salud.
Igualmente, será de obligatorio cumplimiento el reporte inmediato del resultado positivo y negativo al repositorio de tamizaje neonatal, administrado por el INS.
A todo recién nacido con prueba de tamizaje alterada se le debe garantizar la confirmación o descarte de la patología EN EL MENOR TIEMPO POSIBLE, lo que garantiza incidir en los resultados en salud y desarrollo que son objetivo central del tamizaje neonatal.
Confirmación diagnóstica para déficit de biotinidasa
A todo niño o niña con un resultado positivo en el tamizaje para déficit de biotinidasa, debe tomarse la prueba diagnóstica de medición de la actividad de la biotinidasa sérica (Descripción CUPS: Biotinidasa actividad (sangre)). Se establecen los siguientes puntos de corte para la confirmación diagnóstica < 10% déficit total o grave, entre 10-30% déficit parcial o leve. Si este examen es positivo, el paciente se considera como caso confirmado para defecto de biotinidasa y deberá iniciarse el tratamiento inmediatamente.
El diagnóstico clínico y bioquímico es suficiente para iniciar tratamiento en déficit de biotinidasa. Se recomienda la incorporación del análisis molecular en el Programa de Tamizaje Neonatal, como estrategia de confirmación diagnóstica, así como clasificar con mayor precisión la severidad bioquímica, y en algunos casos, predecir la respuesta a terapias específicas. El análisis genético aporta información útil para el asesoramiento genético familiar, evaluación de portadores, planificación reproductiva y registro poblacional de mutaciones en Colombia.
Si bien la integración del análisis molecular contribuye a la calidad, trazabilidad y personalización del tratamiento a largo plazo, en consonancia con estándares internacionales de programas de enfermedades huérfanas y errores innatos del metabolismo; no debe retrasarse el inicio de tratamiento por la toma o resultado de esta prueba.
Una vez diagnosticada la patología, el paciente se considera un caso confirmado por laboratorio y deberá ajustarse inmediatamente la ficha de notificación de acuerdo con los protocolos y lineamientos emitidos por el Instituto Nacional de Salud.
Igualmente, será de obligatorio cumplimiento el reporte inmediato del resultado positivo y negativo al repositorio de tamizaje neonatal, administrado por el INS.
Tratamiento inicial (Plan de cuidado inicial)
El tratamiento debe iniciarse tan pronto como se confirme el diagnóstico. Para los lactantes a quienes se confirma déficit de Biotinidasa, la intervención recomendada es iniciar suplementos de biotina oral en forma libre, no unida a proteínas. La biotina mejora los síntomas en pacientes sintomáticos y previene los síntomas en pacientes diagnosticados en el tamizaje neonatal o antes de que los síntomas se desarrollen.
La dosis recomendada es de 10 mg de biotina oral por día. Una vez que se han desarrollado algunas características tales como atrofia óptica, pérdida auditiva, o retraso psicomotor, es posible que ya no sean reversibles con el tratamiento con biotina. El tratamiento con biotina debe mantenerse de por vida.
De manera paralela al inicio de la biotina oral, se recomienda que los pacientes diagnosticados restrinjan el consumo de huevo crudo de la dieta. El médico tratante podrá indicar estudios adicionales según la condición clínica del paciente.
Seguimiento inicial para pacientes diagnosticados con déficit de biotinidasa
El seguimiento clínico inicial de los recién nacidos con diagnóstico confirmado de déficit de biotinidasa debe ser realizado por un equipo ¡nterdisciplinario, liderado por un médico pediatra o neonatólogo, con apoyo de telesalud de especialistas en errores innatos del metabolismo. El médico general no debe asumir en solitario el manejo de estos pacientes, salvo que haya recibido entrenamiento específico y cuente con un sistema de apoyo formal (como telesalud estructurada). Esta medida busca evitar errores en el seguimiento bioquímico y decisiones terapéuticas que podrían tener consecuencias irreversibles.
Desde el inicio, se debe garantizar la participación de:
- Pediatría o neonatología.
- Genética.
- Nutrición clínica especializada en errores innatos del metabolismo.
- Neurología pediátrica, para evaluación de desarrollo neurológico y detección temprana de signos de daño.
- Psicología y trabajo social, según disponibilidad, para acompañamiento familiar, adherencia al tratamiento y afrontamiento emocional.
El seguimiento clínico y bioquímico debe establecerse con una periodicidad definida (por ejemplo, controles semanales o quincenales durante el primer mes, luego mensuales), y debe incluir:
- Valoración integral.
- Control bioquímico.
- Valoración de adherencia al tratamiento y educación continua a la familia.
Figura 6. Esquema de tamizaje neonatal déficit de biotinidasa.
Fuente: Elaboración propia a partir de literatura referenciada. Consideraciones descritas en el apartado 4.1. - componente preanalítico.
Se establecen los puntos de corte de acuerdo con los lineamientos establecidos por el Instituto Nacional de Salud, los cuales están sujetos de actualización. (11)
4.1,5 Tamizaje para Fibrosis Quistica
Número de identificación de la enfermedad huérfana: 931
Es una enfermedad genética de herencia autosómica recesiva, caracterizada por disfunción de las glándulas de secreción exocrina, causada por mutaciones en la proteína reguladora de la conductancia transmembrana de la fibrosis quística (CFTR), un canal de cloruro complejo, el cual se encuentra en todos los tejidos exocrinos. La alteración del CFTR ocasiona un transporte alterado de cloruro y/u otros iones afectados como el sodio y el bicarbonato, lo que conduce a secreciones espesas y viscosas en los pulmones, el páncreas, el hígado, el intestino y el tracto reproductivo y a un mayor contenido de sal en las secreciones de las glándulas sudoríparas.
El paciente típico con FQ desarrolla una enfermedad multisistémica que involucra varios o todos estos órganos. En los pulmones, la disminución del líquido periciliar limita el movimiento de las cilias, el moco se modifica en su composición y hay alteración en las defensas locales lo que hace que el moco se espese, sea difícil de expectorar y conlleva a infecciones de inflamación que deterioran en forma progresiva el tejido pulmonar En el páncreas, las secreciones espesas obstruyen los conductos intrapancreáticos, lo que reduce el suministro de enzimas digestivas a los intestinos y dificulta la absorción de nutrientes clave. (27) (28)
El promedio de diagnóstico en Colombia en el 2004 era de 3.6 años (29). Otro estudio más reciente (2018) evidencia que, en una cohorte de pacientes con diagnóstico de fibrosis quística de una Institución de Salud, la edad de diagnóstico se encontraba entre los 2 y 3 años de vida, con una demora de 14 a 16 meses desde la sospecha diagnóstica. (30)
Es importante resaltar que el mejor pronóstico lo tienen las personas cuyo diagnóstico, por síntomas, se hace antes de los 2 años, pero el diagnóstico neonatal, antes del inicio de síntomas, ha demostrado una mejora en diversos indicadores, siendo el más importante el aspecto nutricional.
De acuerdo con el Registro Nacional de Personas con Enfermedad Huérfana desde el año 1968 se han reportado 1154 casos, de acuerdo al género 529 casos para el femenino, 593 para el masculino y 32 casos sin grupo a determinar.
De acuerdo con el portal de información de Orphanet la prevalencia estimada es de 1-5 / 10 000. La incidencia anual oscila entre 1:8000 y 1:10.000.
| Prevalencia | 1-5/10.000 |
| Edad promedio diagnóstico (Meses) | 14 meses |
| Impacto en Salud con el tamizaje | Nutrición, crecimiento, función pulmonar, infecciones, sobrevida, alteraciones hidroelectrolíticas, funcionamiento cognitivo, evita la odisea diagnóstica |
Síntomas respiratorios (tos, sibilancias u obstrucción bronquial o neumonías recurrentes) en el 45% de los casos, íleo meconial en el 20% de los pacientes y retraso en el crecimiento en el 28% de los pacientes. El daño pulmonar inicia desde los primeros meses de vida. Los lactantes con insuficiencia pancreática grave no tratada presentan síndrome de edema con hipoproteinemia, pérdida de electrólitos, anemia y retraso del crecimiento debido a malabsorción. También se pueden presentar síntomas gastrointestinales, a temprana edad el íleo meconial y alteraciones de malabsorción intestinal pueden ser características clínicas de la fibrosis quística. (31) (32)
Objetivos de la línea de tamizaje de Fibrosis Quística
- Detectar de forma temprana niños y niñas recién nacidos vivos con niveles elevados de tripsinógeno inmunorreactivo (TIR) en muestra de talón, sugestivas de fibrosis quística, con el fin de confirmar o descartar el diagnóstico oportunamente.
- Iniciar precozmente el tratamiento en los casos confirmados, minimizando los riesgos y mejorando el pronóstico a largo plazo.
- Disminuir la carga de discapacidad asociada a fibrosis quística mediante una intervención temprana, equitativa y sostenible.
- Establecer lineamientos técnicos claros para el seguimiento de casos sospechosos y confirmados, incluyendo la articulación con genética médica, nutrición especializada y pediatría.
- Identificar condiciones clínicas o factores de riesgo que puedan requerir un abordaje diferenciado o intensificado en el seguimiento.
- Articular la línea de tamizaje con los procesos de confirmación diagnóstica, inicio de tratamiento y seguimiento clínico dentro de una ruta de atención integral centrada en el paciente.
Respecto al resultado obtenido, el tamizaje puede definirse como:
- Tamizaje positivo para Fibrosis Quística: recién nacido con dos (2) niveles de TIR por encima del punto de corte establecido ( ![]() 60ng/mL) en dos (2) muestras de sangre de talón, los cuales son considerados casos probables de FQ (TIR-1 inicial y TIR-2 entre la 3ra y 4ta semanas de vida (antes de los 28 días de vida)).
60ng/mL) en dos (2) muestras de sangre de talón, los cuales son considerados casos probables de FQ (TIR-1 inicial y TIR-2 entre la 3ra y 4ta semanas de vida (antes de los 28 días de vida)).
- Tamizaje negativo de Fibrosis Quística: recién nacido con niveles de TIR-1 por debajo del punto de corte establecido; o altos en la primera muestra, pero descienden por debajo del punto de corte en la segunda muestra (TIR-2).
El tamizaje de FQ será interpretado por un profesional en pediatría, neonatología o profesional en medicina general entrenado en la interpretación de los resultados del tamizaje metabólico básico.
Para efectos de la evaluación y tratamiento del Programa de Tamizaje Neonatal, se emplearán las siguientes definiciones en relación con la confirmación diagnóstica para fibrosis quística:
- Rellamado: procedimiento de llamado o citación activa de los pacientes y su familia ante un resultado de tamizaje metabólico positivo, con el fin de realizar pruebas confirmatorias y definir la conducta diagnóstica y terapéutica.
- Diagnóstico confirmado de fibrosis quística: condición establecida cuando un recién nacido con tamizaje positivo presenta resultados elevados de electrolitos en sudor por clorimetría directa y/o indirecta, complementado por un estudio molecular que soporte el diagnóstico.
- Diagnóstico descartado de FQ: condición en la cual, tras el resultado de tamizaje positivo, las pruebas confirmatorias (clorimetría directa e indirecta) no presentan alteración y (estudio molecular) no hay identificación de mutaciones.
Se especifican las siguientes definiciones relacionadas con la atención terapéutica del paciente con diagnóstico confirmado:
- Niño o niña con tratamiento: niño o niña con diagnóstico confirmado de fibrosis quística que ha iniciado tratamiento para la patología, según lo indicado por el equipo médico tratante.
- Niño o niña sin tratamiento: niño o niña con diagnóstico confirmado de fibrosis quística que no ha recibido ninguna intervención terapéutica.
- Niño o niña sin información de tratamiento: niño o niña con diagnóstico confirmado de fibrosis quística del que no se dispone de datos verificables sobre el inicio, tipo o continuidad del tratamiento.
Respecto a la continuidad del cuidado, se establecen los siguientes conceptos:
- Niño o niña con seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de fibrosis quística quien tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de especialista con abordaje de su condición de mayor riesgo, según lo señalado en la RPMS.
- Niño o niña sin seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de fibrosis quística quien no tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de especialista con abordaje de su condición de mayor riesgo, según lo señalado en la RPMS.
Tecnología del tamizaje neonatal de fibrosis quística
El tamizaje neonatal para fibrosis quística debe realizarse mediante la punción de talón, recolectando sangre en papel filtro. La prueba de tamizaje que se consideró es la medición de tripsinógeno inmunorreactivo (Descripción CUPS: Tripsinogeno inmunoreactivo), el punto de corte para tamizaje positivo es ![]() 60 ng/ml.
60 ng/ml.
Consideraciones del resultado positivo para TIR-1:
La medición del TIR-1 en los primeros días de vida tiene baja especificidad, un nivel elevado de TIR no es específico de fibrosis quística lo que ha sido reportado en grandes series de tamización como el grupo de Winsconsin quienes reportan que los factores de estrés perinatal explicaron aproximadamente el 25% de los resultados falsos positivos en la primera prueba del TIR.
Adicionalmente, se debe estar atento a posibles falsos negativos por posibles errores de laboratorio, por tener los puntos de corte muy elevados en pacientes con íleo meconial o hijos de pacientes con fibrosis quística en tratamiento con moduladores de CFTR. (33)
La TIR-1 puede elevarse por varias causas (falsos positivos):
- Sufrimiento fetal agudo.
- Asfixia.
- Sepsis.
- Distrés respiratorio.
- Malformaciones congénitas.
- Trisomías 13, 18 y 21.
- Otras anomalías cromosómicas.
- Infecciones congénitas.
- Cirugía cardiaca.
- Circulación extracorpórea.
- Atresia intestinal.
- Prematurez y bajo peso al nacer.
Es por esta razón que se hace necesario, en los casos en que la TIR-1 salió positiva, realizar una segunda medición (TIR-2) (Descripción CUPS: Tripsinogeno inmunoreactivo) también en sangre de talón, para verificar si entre la tercera y cuarta semana de vida (tomar antes de los 28 días de vida), han descendido los niveles. Si persisten elevados, se confirmaría un tamizaje positivo. (34) Después de la cuarta semana de vida, la TIR-2 pierde validez y no se debería realizar. (35) (36)
Es indispensable la articulación entre el laboratorio.que procesó la muestra, la IPS que tomó la muestra y la aseguradora, para garantizar el rellamado al paciente ante un resultado positivo de TIR-1.
Si bien se recomienda que la toma de la muestra se realice entre las 48 y 72 horas de vida, asegurando que el recién nacido haya recibido alimentación previa (mínimo tres tomas); en el caso de Colombia está indicada una sola toma de muestra para las 7 patologías, la cual debe desarrollarse entre las 48 y 72 horas con las consideraciones descritas en el apartado 4.1. - componente preanalítico. El tiempo máximo para la toma de la muestra debe ser de 5 días de vida. Si la TIR-1 se toma después de los 15 días, debe interpretarse como si fuera TIR-2.
Al ser positivo este tamizaje se considera paciente como caso probable de fibrosis quística y deberá ser inmediatamente notificado al SIVIGILA de acuerdo con el protocolo y lineamientos nacionales emitidos por el Instituto Nacional de Salud.
Igualmente, será de obligatorio cumplimiento el reporte inmediato del resultado positivo y negativo de las dos mediciones de TIR al repositorio de tamizaje neonatal, administrado por el INS.
A todo recién nacido con prueba de tamizaje alterada se le debe garantizar la confirmación o descarte de la patología EN EL MENOR TIEMPO POSIBLE, lo que garantiza incidir en los resultados en salud y desarrollo que son objetivo central del tamizaje neonatal.
Confirmación diagnóstica de fibrosis quística
A todo niño o niña con dos resultados positivos en TIR para tamizaje de fibrosis quística, debe tomarse las pruebas diagnósticas de iontoforesis por medición directa y/o iontoforesis por medición indirecta. (Descripción CUPS: Electrolitos en sudor [iontoforesis] medición directa, Electrolitos en sudor [iontoforesis] medición indirecta).
El estándar de oro para el diagnóstico es la iontoforesis por medición directa. Sin embargo, reconociendo la poca disponibilidad en el país se considerará la alternativa de la iontoforesis por medición indirecta. Para un mejor rendimiento, la iontoforesis se debe tomar máximo a la siguiente semana posterior al resultado positivo de la TIR-2, así como al recién nacido con un peso mayor a 3 kilogramos.
Los siguientes valores se considerarán puntos de corte para indicar un diagnóstico positivo para fibrosis quística.
Tabla 10. Confirmación diagnóstica de fibrosis quística.
| Tecnología | Resultado | Interpretación clínica | Recomendación |
| Iontoforesis por medición directa | < 30 mmol/L(30 mEq/L) | Normal | Descartar fibrosis quística. No requiere tratamiento ni seguimiento especial. |
| 30-59.9 mmol/L | Intermedio | Probabilidad intermedia de fibrosis quística, remisión a neumología pediátrica. Complementar con estudio molecular. | |
| 60 mmol/L | Elevado | Confirmar diagnóstico. Iniciar tratamiento. Complementar con estudio molecular. | |
| Iontoforesis por medición indirecta | < 50 mmol/L | Normal | Descartar fibrosis quística. No requiere tratamiento ni seguimiento especial. |
| 50 – 79,9 mmol/L | Intermedio | Probabilidad intermedia de fibrosis quística, remisión a neumología pediátrica. Complementar con estudio molecular. | |
| 80 mmol/L | Elevado | Confirmar diagnóstico. Iniciar tratamiento. Complementar con estudio molecular. | |
(37)
Se debe complementar siempre con estudios moleculares que confirmen dos variantes patogénicas o probablemente patogénicas para fibrosis quística. El genotipo que se establece con la prueba molecular direcciona el tratamiento específico del paciente ya que cada variante definirá los medicamentos del tratamiento. Sin embargo, no deben retrasarse las atenciones por la toma o resultado de esta prueba. (38) (39)
El estudio molecular es parte de la evaluación del recién nacido con electrolitos en sudor elevados. Si se detectan dos mutaciones causantes de fibrosis quística y la prueba de sudor es intermedia o positiva, se confirma el diagnóstico de fibrosis quística. Si no se identifican dos mutaciones causantes de fibrosis quística, se debe repetir la prueba en sudor. Si la fibrosis quística no se puede confirmar o excluir definitivamente, se le dará al recién nacido un diagnóstico provisional y se debe iniciar su seguimiento por profesionales expertos para detectar síntomas tempranos y continuar el proceso diagnóstico. Se debe realizar siempre estudio molecular de secuenciación completa del gen CFTR con CNV (40) (41). lina vez diagnosticada la patología, el paciente se considera como caso confirmado por laboratorio y deberá ser inmediatamente ajustada de acuerdo con los protocolos y lineamientos emitidos por el Instituto Nacional de Salud.
Igualmente, será de obligatorio cumplimiento el reporte inmediato del resultado positivo y negativo de las pruebas confirmatorias al repositorio de tamizaje neonatal, administrado por el INS.
Tratamiento inicial (Plan de cuidado inicial)
Es necesario que un caso positivo de fibrosis quística diagnosticado por tamizaje neonatal positivo inicie un manejo multidisciplinario antes de los 2 meses de edad. Se debe precisar si hay o no insuficiencia pancreática para decidir iniciar enzimas pancreáticas y vitaminas liposolubles. Adicionalmente debe iniciarse terapia respiratoria por parte de los cuidadores, de acuerdo con las indicaciones del equipo multidisciplinario tratante, así como el seguimiento nutricional para asegurar una curva de crecimiento normal, previniendo el fallo de medro. Una orientación y acompañamiento psicosocial y asesoría genética es deseable dada la complejidad del diagnóstico y el impacto en la familia. Las demás intervenciones de tratamiento obedecerán a los hallazgos por el equipo durante el seguimiento. (42)
Seguimiento inicial para pacientes diagnosticados con fibrosis quística
Los resultados que respalden el diagnóstico de fibrosis quística deben informarse con prontitud al paciente y/o a sus padres/cuidadores, y se debe programar un seguimiento temprano por especialista en fibrosis quística, idealmente a la semana de la confirmación diagnóstica, así como el asesoramiento genético a la familia. Se debe proporcionar información clara sobre la enfermedad y su manejo y se debe ser conscientes de la angustia emocional que causa el proceso de diagnóstico de la FQ por lo que el apoyo psicológico temprano a las familias es recomendable. Hay evidencia de que el estrés del cuidador puede afectar negativamente muchos aspectos del desarrollo infantil.
El seguimiento clínico inicial de los recién nacidos con diagnóstico confirmado de fibrosis quística debe ser realizado por un equipo interdisciplinario. El médico general no debe asumir en solitario el manejo de estos pacientes. Esta medida busca evitar errores en el seguimiento bioquímico y decisiones terapéuticas que podrían tener consecuencias irreversibles.
Desde el inicio, se debe garantizar la participación de:
- Pediatría y/o neonatología.
- Genética.
- Nutrición clínica especializada en errores innatos del metabolismo.
- Neumología pediátrica.
- Gastroenterología pediátrica.
- Terapia respiratoria.
- Psicología y trabajo social, según disponibilidad, para acompañamiento familiar, adherencia al tratamiento y afrontamiento emocional.
El seguimiento clínico y bioquímico debe establecerse con una periodicidad definida (por ejemplo, controles semanales o quincenales durante el primer mes, luego mensuales), y debe incluir:
- Valoración integral.
- Control bioquímico.
- Valoración de adherencia al tratamiento y educación continua a la familia.
Figura 7. Esquema de tamizaje neonatal de fibrosis quística.
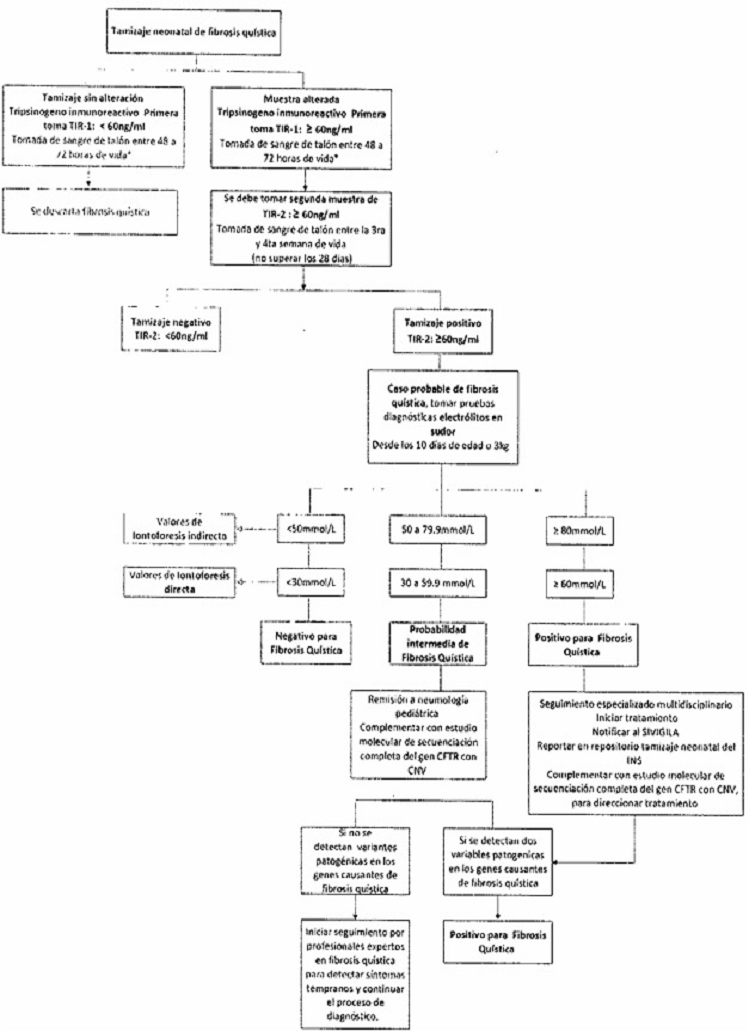
Fuente: Elaboración propia a partir de literatura referenciada.
*Consideraciones descritas en el apartado 4.1. - componente preanalítico.
Se establecen los puntos de corte de acuerdo con los lineamientos establecidos por el Instituto Nacional de Salud, los cuales están sujetos de actualización. (11)
4.1.6 Tamizaje de Hiperplasia Suprarrenal Congénita (HSC)
Número de identificación de la enfermedad huérfana: 1008
La Hiperplasia suprarrenal congénita (HSC), engloba a un grupo de enfermedades autosómicas recesivas, que comportan un trastorno en la esteroidogénesis suprarrenal y que son debidas a deficiencias en cualquiera de las enzimas que intervienen en el paso de colesterol a cortisol y aldosterona. El déficit de cortisol consecuente incrementa la producción de hormona adrenocorticotropa (ACTH) mediante un mecanismo de retroalimentación negativa y, secundariamente, produce una hiperestimulación de la corteza suprarrenal, aumentando el tamaño de las glándulas suprarrenales y provocando la elevación de los esferoides previos al bloqueo enzimático. (43)
De acuerdo con el portal de información de Orphanet la prevalencia estimada es de 1/10.000. La incidencia anual oscila entre 1/5.000 y 1/15.000.
De acuerdo con el Registro Nacional de Personas con Enfermedad Huérfana desde el año 1975 se han reportado en el país 629 personas con hiperplasia suprarrenal congénita, de acuerdo al género 356 son femeninos, 237 masculinos y 35 sin reporte de género. Los años de mayor concentración corresponde al periodo 2016 al 2019.
| Prevalencia | 1:10.000 |
| Edad promedio diagnóstico (Meses) | 2 meses |
| Resultados en Salud a incidir con el tamizaje | Desequilibrio hidroelectrolíticoErrores en la asignación de sexoCrecimientoDesarrolloCrisis adrenal llevaría a morbimortalidad |
El espectro clínico de la enfermedad varía desde las formas más graves a las leves, según el grado de deficiencia de la enzima. La hiperplasia suprarrenal congénita se divide en formas clásicas y no clásicas, a su vez las formas clásicas de subdividen en: perdedoras de sal y virilizantes simples. (44) (45)
- Forma perdedora de sal: Representa la forma más grave y la más frecuente (75% de los afectados). Debida a variantes enzimáticas la más frecuente es la ocasionada por la alteración de la enzima 21 hidroxilasa que metaboliza el paso hacia la formación de cortisol, generando una disminución a ausencia del mismo, llevando a la expresión clínica de hipocortisolismo con hiponatremia, hiperpotasemia, acidosis metabólica, natriuresis elevada y niveles séricos disminuidos de aldosterona, con una elevada actividad de renina plasmática (ARP) y cociente ARP/aldosterona elevada. Clínicamente se caracteriza por un cuadro de deterioro progresivo en el recién nacido, con anorexia, falta de ganancia ponderal, decaimiento, diarrea, llantos, poliuria y vómitos. Estas manifestaciones podrían no ser evidentes hasta que las concentraciones de sodio sérico bajan de 125 mEq/L. Si no se reconoce el cuadro y no se instaura el tratamiento oportuno, evoluciona en poco tiempo a un cuadro grave de deshidratación hipotónica, shock y muerte en el contexto de una verdadera crisis adrenal La mayoría debutan sobre los 15 días de vida como media de alarma. En las niñas normalmente se detecta al nacer por la clínica de genitales ambiguos o alterados, pero en los varones puede pasar desapercibida por no presentar alteraciones genitales marcadas, pudiendo tener consecuencias letales.
- Forma virilizante: Es la forma moderada-grave de la enfermedad. La actividad enzimática se sitúa por debajo del 10%, permitiendo que la actividad enzimática residual de la 21 hidroxilasa permita la producción de cantidades mínimas pero suficientes de cortisol y aldosterona para no desarrollar un síndrome pierde sal. Por tanto, el diagnóstico clínico depende del exceso de andrógenos por encima del bloqueo enzimático. Las niñas afectadas presentan trastorno de la diferenciación sexual en el momento del nacimiento, mientras que los niños pueden presentar signos de virilización (hiperpigmentación, pene elongado) o pasar desapercibidos inicialmente y presentar manifestaciones clínicas con posterioridad: aparición precoz de vello púbico, vello axilar, pene alargado, así como aceleración de la velocidad de crecimiento.
- Forma no clásica o de comienzo tardío: Se presenta con más frecuencia por la deficiencia de 21-OH, es la forma más leve de la enfermedad en la que pueden existir pacientes completamente asintomáticos. Las formas no clásicas por definición se presentan sin virilización, la presentación más común en la edad pediátrica sería la de una pubarquia precoz. La actividad enzimática se sitúa entre el 20-50% y los síntomas clínicos son variables y se pueden presentar a cualquier edad, incluso tan temprano como a los seis meses de vida. Generalmente los síntomas de hiperandrogenismo son pocos marcados, aunque variables desde únicamente acné (generalmente quístico) a oligomenorrea, alopecia de distribución masculina e infertilidad.
Objetivos de la línea de tamizaje de Hiperplasia Suprarrenal Congénita
- Detectar de forma temprana niños y niñas recién nacidos vivos con concentraciones elevadas de 17 alfa hidroxiprogesterona en muestra de talón, sugestivas de hiperplasia suprarrenal congénita, con el fin de confirmar o descartar el diagnóstico oportunamente.
- Iniciar precozmente el tratamiento en los casos confirmados, minimizando el riesgo de daños irreversibles y mejorando el pronóstico a largo plazo.
- Establecer lineamientos técnicos claros para el seguimiento de casos sospechosos y confirmados, incluyendo la articulación con genética médica, endocrinología y pediatría.
- Identificar condiciones clínicas o factores de riesgo que puedan requerir un abordaje diferenciado o intensificado del seguimiento.
- Articular la línea de tamizaje con los procesos de confirmación diagnóstica, inicio de tratamiento y seguimiento clínico dentro de una ruta de atención integral centrada en el paciente.
Respecto al resultado obtenido, el tamizaje puede definirse como:
- Tamizaje positivo para HSC: recién nacido con niveles de 17-OHP por encima del punto de corte establecido según peso en muestra de sangre de talón, los cuales son considerados casos probables de HSC.
- Tamizaje negativo de HSC: recién nacido con niveles de 17-OHP inferiores al punto de corte establecido. Este resultado no requiere seguimiento adicional, salvo que existan condiciones clínicas especiales o antecedentes familiares relevantes.
El tamizaje de HSC será interpretado por un profesional en pediatría, neonatología o profesional en medicina general entrenado en la interpretación de los resultados del tamizaje metabólico básico.
Para efectos de la evaluación y tratamiento del Programa de Tamizaje Neonatal, se emplearán las siguientes definiciones en relación con la confirmación diagnóstica para hiperplasia suprarrenal congénita:
- Rellamado: procedimiento de llamado o citación activa de los pacientes y su familia ante un resultado de tamizaje metabólico positivo, con el fin de realizar pruebas confirmatorias y definir la conducta diagnóstica y terapéutica.
- Diagnóstico confirmado de HSC: condición establecida cuando un recién nacido con tamizaje positivo presenta elevación en el reporte de 17-OHP en suero.
- Diagnóstico descartado de HSC: condición en la cual, tras el resultado de tamizaje positivo, las pruebas confirmatorias (17-OHP en suero) no presentan alteración.
Se especifican las siguientes definiciones relacionadas con la atención terapéutica del paciente con diagnóstico confirmado:
- Niño o niña con tratamiento: niño o niña con diagnóstico confirmado de HSC que ha iniciado tratamiento para HSC, según lo indicado por el equipo médico tratante.
- Niño o niña sin tratamiento: niño o niña con diagnóstico confirmado de HSC que no ha recibido ninguna intervención terapéutica para HSC.
- Niño o niña sin información de tratamiento: niño o niña con diagnóstico confirmado de HSC del que no se dispone de datos verificables sobre el inicio, tipo o continuidad del tratamiento.
Respecto a la continuidad del cuidado, se establecen los siguientes conceptos:
- Niño o niña con seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de HSC quien tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de especialista con abordaje de su condición de mayor riesgo, según lo señalado en la RPMS.
- Niño o niña sin seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de HSC quien no tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de especialista con abordaje de su condición de mayor riesgo, según lo señalado en la RPMS
Tecnología del tamizaje neonatal de hiperplasia suprarrenal congénita
El tamizaje neonatal para hiperplasia suprarrenal congénita debe realizarse mediante la punción de talón, recolectando sangre en papel filtro. La prueba para tamizaje que se consideró es la determinación de 17 - Alfa hidroxiprogesterona (17-OHP), (Descripción CUPS: Hidroxiprogesterona 17 alfa). Los puntos de corte para tamizaje positivo de acuerdo con el peso son:
- RN <1500 gramos de peso: ![]() 250 nmol/L
250 nmol/L
- RN entre 1500 g y 2499 gramos de peso: ![]() 180 nmol/L
180 nmol/L
- RN con peso mayor a 2500 gramos de peso: ![]() 80 nmol/L
80 nmol/L
Si bien se recomienda que la toma de la muestra se realice entre las 48 y 72 horas de vida, asegurando que el recién nacido haya recibido alimentación previa (mínimo tres tomas), lo cual es indispensable para evitar falsos negativos); en el caso de Colombia está indicada una sola toma de muestra para las 7 patologías, la cual debe desarrollarse entre las 48 y 72 horas con las consideraciones descritas en el apartado 4.1. - componente preanalítico.
El tiempo máximo para la toma de la muestra debe ser de 5 días de vida, ya que se pretende con el tamizaje anticiparse a la aparición de una crisis de pérdida salina grave y potencialmente letal y evitar la morbimortalidad derivada de la pérdida salina, evitar una incorrecta asignación de sexo en una niña con genitales externos virilizados, diagnosticar precozmente las formas virilizantes simples para evitar la hiperandrogenización durante la infancia que determinará una talla final baja.
Los prematuros y los neonatos con enfermedades concomitantes, por estar sometidos a un estrés adicional, tienden a presentar niveles más altos de 17-OHP que los recién nacidos a término y pueden generar resultados falsos positivos. Además, se pueden generar falsos positivos cuando la muestra de sangre total se obtiene en las primeras 24 horas de vida.
Al ser positivo este tamizaje se considera paciente como caso probable de hiperplasia suprarrenal congénita y deberá ser inmediatamente notificado al SIVIGILA de acuerdo con el protocolo y lineamientos nacionales emitidos por el Instituto Nacional de Salud. Igualmente, será de obligatorio cumplimiento el reporte inmediato del resultado positivo y negativo al repositorio de tamizaje neonatal, administrado por el INS. Todo niño o niña con tamizaje positivo para HSC debe garantizarse la prueba confirmatoria de manera inmediata.
A todo recién nacido con prueba de tamizaje alterada se le debe garantizar la confirmación o descarte de la patología EN EL MENOR TIEMPO POSIBLE, lo que garantiza incidir en los resultados en salud y desarrollo que son objetivo central del tamizaje neonatal.
Confirmación diagnóstica de hiperplasia suprarrenal congénita
A todo niño o niña con un resultado positivo en el tamizaje para hiperplasia suprarrenal congénita, debe tomarse la prueba diagnóstica de determinación sérica de 17 alfa hidroxiprogesterona (Descripción CUPS: Hidroxiprogesterona 17 alfa), de manera inmediata.
Tabla 11. Confirmación diagnóstica de hiperplasia suprarrenal congénita.
| Resultado de 17-OH en suero | Interpretación clínica | Recomendación |
| < 2 ng/ml | Resultado normal | Descartar HSP. No requiere tratamiento ni seguimiento especial. |
| 2 ng/ml a 9,9 ng/ml | No conclusiva | Remitir a endocrinología pediátrica para valoración y estudios adicionales (requiere realizar prueba de estímulo con ACTH) |
| | Hiperplasia suprarrenal confirmada | Iniciar tratamiento inmediato sin esperar confirmación adicional. Remitir a unidad de cuidado intensivo neonatal. |
(46) (47)
Si este examen es positivo, el paciente se considera un caso confirmado para Hiperplasia Suprarrenal Congénita y deberá hospitalizarse en la unidad de recién nacidos para el inicio o establecimiento del tratamiento.
El diagnóstico clínico y bioquímico es suficiente para iniciar tratamiento en hiperplasia suprarrenal congénita, se recomienda la incorporación del análisis molecular en el Programa de Tamizaje Neonatal, como estrategia de confirmación diagnóstica definitiva, así como clasificar con mayor precisión la severidad bioquímica, y en algunos casos, predecir la respuesta a terapias específicas. El análisis genético aporta información útil para el asesoramiento genético familiar, evaluación de portadores, planificación reproductiva y registro poblacional de mutaciones en Colombia.
Si bien la integración del análisis molecular contribuye a la calidad, trazabilidad y personalización del tratamiento a largo plazo, en consonancia con estándares internacionales de programas de enfermedades huérfanas y errores innatos del metabolismo; no debe retrasarse el inicio de tratamiento por la toma o resultado de esta prueba.
Una vez diagnosticada la patología, el paciente se considera como caso confirmado por laboratorio y deberá ser inmediatamente ajustada la ficha de notificación de acuerdo con los protocolos y lineamientos emitidos por el Instituto Nacional de Salud.
Igualmente, será de obligatorio cumplimiento el reporte inmediato del resultado positivo y negativo de la prueba confirmatoria al repositorio de tamizaje neonatal, administrado por el INS.
Tratamiento inicial (Plan de cuidado inicial)
Uno de los objetivos del tratamiento inmediato en la hiperplasia suprarrenal congénita es frenar la hipersecreción de ACTH y el hiperandrogenismo concomitante, razón por la cual el paciente debe ser hospitalizado inmediatamente
Se recomienda el inicio del siguiente plan de cuidado mientras se deriva al paciente a unidad de cuidado intensivo y endocrinología pediátrica.
- Monitoreo bioquímico: Se debe monitorizar de los niveles de 17- OHP, androstenediona, medición de electrolitos, niveles de renina, testosterona total. Deben tomarse antes de empezar tratamiento. Durante los dos primeros años de vida la 17- OHP debe ser medida con método de extracción (17-OHP pediátrica).
- Inicio de tratamiento: Iniciar el tratamiento con hidrocortisona (20 a 25 mg/m2/día repartidos en dos o tres dosis). Su administración puede ser vía oral, intravenosa o intramuscular, de forma continuada y durante toda la vida del paciente. Esto corrige la fisiopatología subyacente del trastorno del déficit de cortisol. Se recomienda aumentar la dosis en los períodos de estrés o cuando disminuya la ingesta de sal.
No se debe retrasar el inicio del tratamiento esperando los resultados de los laboratorios. Pero si deben tomarse de forma previa al inicio del tratamiento.
- Hiperplasia clásica - forma perdedora de sal: El manejo de los niños y niñas durante el periodo neonatal es un reto, ya que dos tercios presentan pérdida salina. Los recién nacidos son particularmente vulnerables a la hipovolemia, hipoglucemia y a las alteraciones electrolíticas, en niños con HSC se observa un incremento de la mortalidad. A pesar del tratamiento hormonal, y de las indicaciones a los padres, aproximadamente el 8% de los afectados presentan hipoglucemia en los primeros años de vida.
Para la forma perdedora de sal, el profesional de endocrinología pediátrica, de acuerdo con los resultados de los laboratorios anteriormente mencionados, deberá definir manejo adicional con fludrocortisona y suplementación con sal.
No se debe retrasar el inicio del tratamiento esperando los resultados de los laboratorios. Pero si deben tomarse de forma previa al inicio del tratamiento.
- Monitoreo bioquímico: Se debe dejar la orden médica de monitorizar los niveles de 17- OHP, androstenediona, medición de electrolitos, niveles de renina, testosterona total en tres meses posterior al inicio del tratamiento, pues constituyen los mejores parámetros para controlar la eficacia del tratamiento. Durante los dos primeros años de vida la 17-OHP debe ser medida con método de extracción (17-OHP pediátrica).
- Es indispensable el apoyo psicológico para los pacientes afectados y su familia. Se debe realizar una evaluación rutinaria de los desórdenes psiquiátricos y del comportamiento. El asesoramiento a los padres podría ayudar a reconocer los síntomas y prevenir complicaciones futuras, por lo tanto, el manejo interdisciplinario es fundamental.
Seguimiento inicial para pacientes diagnosticados con hiperplasia suprarrenal congénita
El seguimiento clínico inicial de los recién nacidos con diagnóstico confirmado de hiperplasia suprarrenal congénita debe ser realizado por un equipo interdisciplinario, liderado por un médico endocrinólogo pediatra o pediatra con apoyo de telesalud de especialistas en errores innatos del metabolismo. Esta medida busca evitar errores en el ajuste terapéutico, seguimiento bioquímico y decisiones terapéuticas que podrían tener consecuencias irreversibles.
Desde el inicio, se debe garantizar la participación de:
- Pediatría o neonatología.
- Endocrinología pediátrica.
- Genética.
- Urología.
- Psiquiatría, psicología y trabajo social, según disponibilidad, para acompañamiento familiar, adherencia al tratamiento y afrontamiento emocional.
El seguimiento clínico y bioquímico debe establecerse con una periodicidad definida (por ejemplo, controles semanales o quincenales durante el primer mes, luego mensuales), y debe incluir:
- Valoración integral.
- Control bioquímico.
- Valoración de adherencia al tratamiento y educación continua a la familia.
Figura 8. Esquema de tamizaje neonatal de hiperplasia suprarrenal congénita.
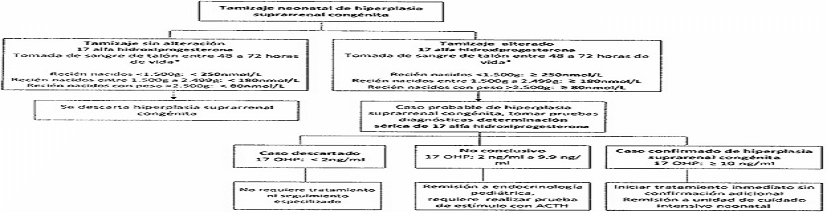
Fuente: Elaboración propia a partir de literatura referenciada.
*Consideraciones descritas en el apartado 4.1. - componente preanalitico.
Se establecen los puntos de corte de acuerdo con los lineamientos establecidos por el Instituto Nacional de Salud, los cuales están sujetos de actualización. (11)
4.1.7 Tamizaje Defectos de la Hemoglobina
Número de identificación de la enfermedad huérfana rara:
Drepanocitosis: 751
Alfa talasemia: 78
Beta talasemia: 227
Las hemoglobinopatías son un conjunto de enfermedades de origen genético con alteración cualitativa o cuantitativa de las cadenas de globina de la hemoglobina.
Las alteraciones pueden ser estructurales, con cambios en la secuencia de aminoácidos de la globina. Por ejemplo, tal como ocurre en la HbS, HbC, HbD y HbE. Por otro lado, se puede observar alteración en la síntesis de una globina estructuralmente normal, tal como ocurre en las talasemias. Por último, se pueden encontrar individuos en los que coexisten alteraciones estructurales y talasémicas.
La enfermedad de células falciformes, drepanocitosis o hemoglobina S es una hemoglobinopatía estructural en la cual se da la sustitución del ácido glutámico por valina en el 6o aminoácido de la cadena de P globina. La condición puede manifestarse de varias maneras:
- Individuo heterocigoto (HbAS): portador del rasgo falciforme o rasgo drepanocítico.
- Individuo homocigoto (HbSS): la forma más frecuente (aproximadamente 75% de los individuos) y denominada anemia de células falciformes.
- Individuo doble heterocigoto: portador del rasgo falciforme y coocurrencia de variante patogénica para otra hemoglobinopatia: HbSC; HbSD, HbS0+ talasemia; HbS0O talasemia; entre otras.
Los individuos con HbSS y HbSpO talasemia tienen un compromiso más temprano y severo, generalmente; por ello, son de interés principal para el tamízaje neonatal. (48)
El cambio p.Glu6Val (HbS) produce menor solubilidad de la hemoglobina, que se puede agregar y polimerizar en estado desoxigenado. Esta HbS polimerizada daña a los glóbulos rojos, ya que los ciclos repetidos de polimerización-despolimerización dañan al citoesqueleto y la membrana celular, como consecuencia de la polimerización los glóbulos rojos toman entonces forma de hoz, se adhieren al endotelio vascular y entre si, ocluyen la luz de pequeños vasos y ocasionan infarto de los tejidos, conduciendo a la disminución de la vida útil de los eritrocitos con hemolisis y las secuelas relacionadas. Estos eritrocitos son rígidos, con menor capacidad de deformación para pasar por vasos sanguíneos pequeños y tienen menor resistencia al traumatismo mecánico al que se ven sometidos durante la circulación y podrían romperse, generando hemolisis. El flujo defectuoso de los glóbulos rojos en la microcirculación ocasiona la oclusión de los capilares y las vénulas poscapilares. Finalmente, los fenómenos hemolíticos y vaso oclusivos causan daño progresivo.
Otros cambios moleculares patogénicos en la secuencia son: p.GluSLys (HbC), p.Glu121Gln (HbD), p.Glu26Lys (HbE), y p.Glu121Lys (HbO), que pueden producir anemia, pero no producen la forma de hoz de los eritrocitos que causa la HbS.
Adicionalmente, se puede encontrar la ausencia en producción de la cadena 0 de la globina que ocasiona la 0-talasemía mayor (00), o disminución en la producción (0+). Lo que implica ausencia o disminución de la HbA (adulta), respectivamente. Así, como producción incrementada de HbA2 en diferente medida con persistencia de HbF. (49)
Los defectos hereditarios de la hemoglobina constituyen los trastornos hereditarios más comunes, afectan a más de 5% de la población mundial. Se han descrito en la literatura cerca de 2.000 variantes de la hemoglobina (Hb), aunque no todas tienen significancia clínica. Anualmente, se estima que hay más de 330.000 nacimientos afectados. De estas, la enfermedad de células falciformes es la más frecuente y ha sido reconocida como un problema de salud mundial. (50)
A nivel mundial, el porcentaje de portadores de talasemia es mayor que el de portadores de anemia de células falciformes (SCA, por sus siglas en inglés) pero debido a la mayor frecuencia del gen de la anemia de células falciformes en ciertas regiones, el número de nacimientos afectados es mayor que el de los que presentan talasemia. En 2008, la Organización Mundial de la Salud (OMS) reveló que alrededor del 5,2% de la población mundial presenta una variante genómica significativa que provoca hemoglobinopatía y que el 24% es portador de todas las variantes conocidas, tanto patógenas como no patógenas. Estos trastornos podrían provocar SCA, disminución de la esperanza de vida de los glóbulos rojos (GR)/hemólisis y otras patologías sistémicas, dependiendo de la(s) mutación(es) específica(s).
Los trastornos de la hemoglobina constituyen los problemas más frecuentes en el mundo, se ha descrito mayor ocurrencia en poblaciones históricamente más expuestas a malaria, con una presión de selección positiva, al conferir protección para la enfermedad en los portadores del rasgo falciforme.
Se estima que la incidencia mundial de anemia de células falciformes es de aproximadamente 2,28/1000 nacimientos, con una distribución muy variable en las diferentes poblaciones humanas, desde 0,07/1000 nacimientos en Europa hasta 10,68/1000 nacimientos en África. La distribución de portadores de variantes de hemoglobina de interés clínico (incluyendo HbS, HbC, HbD, HbE, o-Talasemia) también es amplia, 18,2% en África y 1,1% en Europa. (51)
Por otro lado, los trastornos de la hemoglobina de interés clínico representan aproximadamente el 3,4% de las muertes en niños menores de 5 años y la mediana de la mortalidad de los hombres con anemia de células falciformes es de 53 años y de 58,5 años para las mujeres. La OMS estimó que la anemia de células falciformes era responsable de 10- 20% de la mortalidad infantil en países en vía de desarrollo, y que fallecían 10% de los niños afectados sin diagnóstico neonatal en países desarrollados. En 2008, Van der Pías et al, estimaron en Holanda que la mortalidad era de 2,7/1000 pacientes/año para enfermedad de células falciformes, con 97,3% de supervivencia a los 18 años, antes de la introducción del tamizaje neonatal.
En Colombia, Rosero y Bermúdez reportaron frecuencia de 0,12% para anemia de células falciformes en una muestra de individuos de regiones afrocolombianas. El Instituto Nacional de Salud indicó que durante los dos primeros años (2016-2017) de vigilancia de drepanocitosis fueron reportados 195 casos de todo el territorio nacional, pero principalmente de la región pacífica.
De acuerdo con el Registro Nacional de Personas con Enfermedad Huérfana desde el año 1963 se han reportado en el país 1900 personas con defecto de hemoglobina, de acuerdo al género 983 son femeninos, 886 masculinos y 31 no cuentan con reporte de género. Los años de mayor concentración corresponde al periodo 2016 al 2022.
Estos casos se han reportado en 26 departamentos, la mayor cantidad se concentran en el departamento de Valle del Cauca con un total de 898 casos que corresponden al 47.2%, seguido de Bolívar con el 18.6%, Cauca con el 12.2%, Córdoba 4.1% y Nariño con el 4%.
| Edad promedio diagnóstico (Meses) | 12 meses |
| Resultados en Salud a incidir con el tamizaje | *Mortalidad en < 5 años *Carga de la enfermedad *Discapacidad cognitiva intelectual *Tasas de complicaciones agudas: (Crisis vaso oclusivas, Evento Cerebro Vascular, síndrome torácico agudo, infecciones, hipertensión pulmonar, falla renal) |
Las manifestaciones clínicas de las hemoglobinopatías son muy variables, y dependen del genotipo (ocurrencia de variantes de hemoglobina) y la edad del individuo afectado. Se considera que las formas HbSS y ![]() talasemia tienen mayor severidad, los portadores heterocigotos (HbAS) de rasgo falciforme generalmente son sanos o con compromiso menor.
talasemia tienen mayor severidad, los portadores heterocigotos (HbAS) de rasgo falciforme generalmente son sanos o con compromiso menor.
En población pediátrica menor de 5 años con anemia de células falciformes se observa un riesgo elevado de cuadros infecciosos, siendo la septicemia por neumococo reportada como la causa más frecuente de muerte y en segundo lugar los eventos cerebrovasculares pediátricos. En mayores de 5 años el riesgo de infecciones disminuye. Algunas manifestaciones graves como las infecciones y el secuestro esplénico pueden manifestarse tan temprano como a los 2-3 meses de edad. Anemia y hemolisis se pueden observar a 6 -12 meses de edad. Antes de los 2 años pueden presentarse crisis aplásicas y síndrome torácico agudo, y los eventos cerebrovasculares luego de los 2 años. En niños mayores de 5 años la mortalidad se asocia con síndrome torácico agudo.
La anemia de células falciformes produce una afectación sistémica por oclusión vascular, hemolisis y desarrollo de cuadros infecciosos. Este compromiso se traduce en anemia hemolitica, episodios de dolor y complicaciones en órganos y sistemas importantes como sistema nervioso central, respiratorio, musculoesquelético, genitourinarias, oftalmológicas, esplénicas, y en crecimiento y desarrollo del individuo afectado. La afectación es crónica con manifestaciones agudas como episodios de dolor, secuestro esplénico, síndrome torácico agudo, eventos cerebrovasculares principalmente isquémicos en la infancia y hemorrágicos en adultos jóvenes, exacerbaciones agudas de la anemia y cuadros infecciosos. Todo este compromiso afecta la calidad de vida y genera discapacidad. (52) (53)
Objetivos de la línea de tamizaje de Defectos de la Hemoglobina
- Detectar de forma temprana niños y niñas recién nacidos vivos con probables defectos de la hemoglobina por medio de la medición de los niveles de hemoglobina S, coexistencia de hemoglobina S y variante para ![]() - talasemia, con el fin de confirmar o descartar el diagnóstico oportunamente.
- talasemia, con el fin de confirmar o descartar el diagnóstico oportunamente.
- Iniciar precozmente el tratamiento en los casos confirmados, minimizando el riesgo de daños irreversibles y mejorando el pronóstico a largo plazo.
- Establecer lineamientos técnicos claros para el seguimiento de casos sospechosos y confirmados, incluyendo la articulación con genética médica y pediatría.
- Identificar condiciones clínicas o factores de riesgo que puedan requerir un abordaje diferenciado o intensificado del seguimiento.
- Articular la línea de tamizaje con los procesos de confirmación diagnóstica, inicio de tratamiento y seguimiento clínico dentro de una ruta de atención integral centrada en el paciente.
Respecto al resultado obtenido, el tamizaje puede definirse como:
- Tamizaje positivo para DH: recién nacido con HPLC con presencia de Hemoglobina S, existencia variante para a - talasemia o ![]() - talasemia en muestra de sangre de talón, los cuales son considerados casos probables de DH.
- talasemia en muestra de sangre de talón, los cuales son considerados casos probables de DH.
- Tamizaje negativo de DH: recién nacido con HPLC sin presencia de Hemoglobina S, con niveles de HbA, HbF dentro de los puntos de corte. Este resultado no requiere seguimiento adicional, salvo que existan condiciones clínicas especiales o antecedentes familiares relevantes.
El tamizaje para defectos de la hemoglobina será interpretado por un profesional en pediatría, neonatología o profesional en medicina general entrenado en la interpretación de los resultados del tamizaje metabólico básico.
Para efectos de la evaluación y tratamiento del Programa de Tamizaje Neonatal, se emplearán las siguientes definiciones en relación con la confirmación diagnóstica para defectos de la hemoglobina:
- Rellamado: procedimiento de llamado o citación activa de los pacientes y su familia con resultado de tamizaje metabólico positivo, con el fin de realizar pruebas confirmatorias y definir conducta diagnóstica y terapéutica.
- Diagnóstico confirmado de DH: condición establecida cuando un recién nacido con tamizaje positivo presenta una prueba confirmatoria con reporte de Hemoglobina S, coexistencia de hemoglobina S y variante para a - talasemia o ![]() - talasemia en sangre total alterado, con una tecnología diferente a la de tamizaje.
- talasemia en sangre total alterado, con una tecnología diferente a la de tamizaje.
- Diagnóstico descartado de DH: condición en la cual, tras el resultado de tamizaje positivo, las pruebas confirmatorias no presentan alteración.
Se especifican las siguientes definiciones relacionadas con la atención terapéutica del paciente con diagnóstico confirmado:
- Niño o niña con tratamiento: niño o niña con diagnóstico confirmado de DH que ha iniciado manejo para DH, según lo indicado por el equipo médico tratante.
- Niño o niña sin tratamiento: niño o niña con diagnóstico confirmado de DH que no ha iniciado ninguna intervención terapéutica para DH.
- Niño o niña sin información de tratamiento: niño o niña con diagnóstico confirmado de DH del que no se dispone de datos verificables sobre el inicio, tipo o continuidad del tratamiento.
Respecto a la continuidad del cuidado, se establecen los siguientes conceptos:
- Niño o niña con seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de DH quien tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de especialista con abordaje de su condición de mayor riesgo, según lo señalado en la RPMS.
- Niño o niña sin seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de DH quien no tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de especialista con abordaje de su condición de mayor riesgo, según lo señalado en la RPMS.
Tecnología del tamizaje neonatal para defectos de la hemoglobina
El tamizaje neonatal para defectos de la hemoglobina debe realizarse mediante la punción de talón, recolectando sangre en papel filtro. La prueba para tamizaje que se consideró es la cromatografía líquida de alto desempeño HPLC (Descripción CUPS: Hemoglobinas (específico) cualitativa o cuantitativa), el punto de corte para drepanocitosis es la presencia de Hemoglobina S, coexistencia de hemoglobina S y variantes estructurales de la cadena p. de las cuales, las más frecuentes son: HbC, HbE, HbD y HbO-Arab que son las involucradas en los síndromes falciformes y variantes para a - talasemia o ![]() - talasemia.
- talasemia.
Si bien se recomienda que la toma de la muestra se realice hacia las 72 horas de vida, asegurando que el recién nacido haya recibido alimentación previa (mínimo tres tomas), lo cual es indispensable para evitar falsos negativos); en el caso de Colombia está indicada una sola toma de muestra para las 7 patologías, la cual debe desarrollarse entre las 48 y 72 horas con las consideraciones descritas en el apartado 4.1. - componente preanalítico. El tiempo máximo para la toma de la muestra debe ser de 5 días de vida. (54)
Las diferentes pruebas de tamizaje y de diagnóstico basadas en proteínas que separan diferentes facciones de hemoglobina, son sensibles, pero no específicas para la SCA, teniendo en cuenta que es el diagnóstico principal y de talasemias como secundario; tienen la ventaja de ser económicas, sólidas y relativamente fáciles de interpretar. Sin embargo, un resultado de tamizaje con patrón FS puede indicar diferentes formas de enfermedad drepanocítica- Homocigoto SS o Spo -talasemia, que predice un genotipo severo, o drepanocitosis con persistencia de hemoglobina fetal (S-HPFH) una condición benigna. También se puede confundir FSA (sugestiva de HbS p+ talasemia) diagnosticada como rasgo falciforme al que no se le realiza seguimiento. Además, estas pruebas pueden verse alteradas por la prematuridad o transfusiones sanguíneas. De ahí la importancia de realizar una prueba confirmatoria con un método se separación de hemoglobinas distinto al tamizaje y en ocasiones se requieren pruebas moleculares para aclarar el diagnóstico.
Al ser positivo este tamizaje se considera paciente como caso probable para defectos de la hemoglobina y deberá ser inmediatamente notificado al SIVIGILA de acuerdo con el protocolo y lineamientos nacionales emitidos por el Instituto Nacional de Salud.
Igualmente, será de obligatorio cumplimiento el reporte inmediato del resultado positivo y negativo al repositorio de tamizaje neonatal, administrado por el INS.
A todo recién nacido con prueba de tamizaje alterada se le debe garantizar la confirmación o descarte de la patología EN EL MENOR TIEMPO POSIBLE, lo que garantiza incidir en los resultados en salud y desarrollo que son objetivo central del tamizaje neonatal.
Confirmación diagnóstica para Defectos de la hemoglobina
A todo niño o niña con un resultado positivo en el tamizaje para defectos de la hemoglobina, debe tomarse la prueba diagnóstica con una técnica diferente a la del tamizaje, electroforesis capilar o isoelectroenfoque en sangre total (Descripción CUPS: Hemoglobinas (especifico) cualitativa o cuantitativa) para determinación de las hemoglobinas presentes.
Se debe considerar que la presencia de hemoglobina fetal (hasta 6-12 meses de edad) puede dificultar el diagnóstico temprano.
Los errores de diagnóstico que pueden ocurrir durante las pruebas neonatales incluyen los siguientes:
Las pruebas de solubilidad pueden no ser válidas debido a la gran cantidad de Hb F presente en la sangre fetal.
La prueba de electroforesis de Hb después de la transfusión de glóbulos rojos puede dar como resultado un diagnóstico incorrecto. En tales casos, el diagnóstico de SCD debe utilizar pruebas de ADN o posponerse durante al menos cuatro meses después de la transfusión.
En bebés muy prematuros, es posible que no se detecte la Hb A, lo que resulta en un diagnóstico erróneo. Los bebés muy prematuros con rasgo drepanocítico pueden tener niveles de Hb S superiores a los de Hb A, lo que da como resultado un diagnóstico incorrecto de hemoglobina S/beta + talasemia (55)
Si este examen diagnóstico es positivo, el paciente se considera como caso confirmado para defectos de la hemoglobina y deberá iniciarse el tratamiento inmediatamente.
El diagnóstico clínico y bioquímico es suficiente para iniciar tratamiento para defectos de la hemoglobina, se recomienda la incorporación del análisis molecular en el Programa de Tamizaje Neonatal, como estrategia de confirmación diagnóstica definitiva, así como clasificar con mayor precisión la severidad bioquímica, y en algunos casos, predecir la respuesta a terapias específicas. El análisis genético aporta información útil para el asesoramiento genético familiar, evaluación de portadores, planificación reproductiva y registro poblacional de mutaciones en Colombia.
Si bien la integración del análisis molecular contribuye a la calidad, trazabilidad y personalización del tratamiento a largo plazo, en consonancia con estándares internacionales de programas de enfermedades huérfanas y errores innatos del metabolismo; no debe retrasarse el inicio de tratamiento por la toma o resultado de esta prueba.
Una vez diagnosticada la patología, el paciente se considera como caso confirmado por laboratorio y deberá ser inmediatamente ajustada la ficha de notificación de acuerdo con los protocolos y lineamientos emitidos por el Instituto Nacional de Salud.
Igualmente, será de obligatorio cumplimiento el reporte inmediato del resultado positivo y negativo de la prueba confirmatoria al repositorio de tamizaje neonatal, administrado por el INS.
Tratamiento inicial (Plan de cuidado inicial)
El objetivo de una intervención temprana es evitar la aparición de las complicaciones agudas y crónicas. Esta intervención se basa en la educación a los cuidadores/padres para identificación rápida de los eventos de compromiso agudo, hidratación, evitar climas extremos y detectar complicaciones crónicas; y la prevención primaria de las infecciones, especialmente por neumococo. La prevención primaria de las infecciones incluye el inicio de profilaxis antibiótica y esquema de vacunación.
Seguimiento inicial para pacientes diagnosticados con defectos de la hemoglobina
El seguimiento clínico inicial de los recién nacidos con diagnóstico confirmado para defectos de la hemoglobina debe ser realizado por un equipo interdisciplinario, liderado por un médico pediatra o neonatólogo, con apoyo de telesalud de especialistas en errores innatos del metabolismo.
El médico general no debe asumir en solitario el manejo de estos pacientes, salvo que haya recibido entrenamiento específico y cuente con un sistema de apoyo formal (como telesalud estructurada). Esta medida busca evitar errores en el ajuste dietético, seguimiento bioquímico y decisiones terapéuticas que podrían tener consecuencias neurológicas irreversibles.
Desde el inicio, se debe garantizar la participación de:
1. Pediatra o neonatólogo.
2 Genetista.
3. Hematología pediátrica.
4. Psicología y trabajo social, según disponibilidad, para acompañamiento familiar, adherencia al tratamiento y afrontamiento emocional.
El seguimiento clínico y bioquímico debe establecerse con una periodicidad definida (por ejemplo, controles semanales o quincenales durante el primer mes, luego mensuales), y debe incluir:
- Valoración integral.
- Control bioquímico.
- Valoración de adherencia al tratamiento y educación continua a la familia.
Figura 9: Esquema de tamizaje neonatal para defectos de la hemoglobina.

Fuente: Elaboración propia a partir de literatura referenciada. 'Consideraciones descritas en el apartado 4.1. - componente preanalítico.
Se establecen los puntos de corte de acuerdo con los lineamientos establecidos por el Instituto Nacional de Salud, los cuales están sujetos de actualización.
4.2. Tamizaje neonatal auditivo
Corresponde a la detección de recién nacidos con alteraciones auditivas que pueden llevar a hipoacusia, afectar su capacidad auditiva y de esta forma, amenazar el desarrollo integral del niño o la niña en el curso de la vida.
La Resolución 3280 del 2018, menciona la obligatoriedad para la realización de este tamizaje a toda la población neonatal y que de acuerdo con los factores de riesgo auditivos evaluados en el paciente se utilizarían en combinación ambas tecnologías propuestas: Emisiones Otoacústicas (EOA) o Respuesta Auditiva de Tallo Encefálico Automatizada (RATEA)[12] o solamente RATEA de rutina en todos los niños sin factor de riesgo. En este acto resolutivo adicional a la información expuesta en la referida resolución se consideró adicionar los tiempos máximos de toma de tamizaje auditivo, la tecnología que permita confirmar el diagnóstico y asi mismo la remisión con el especialista de fonoaudiología o audiologia para continuar de acuerdo con la ruta de riesgo el tratamiento y seguimiento.
Objetivos
- Identificar niños y niñas recién nacidos con posibles alteraciones auditivas temporales o permanentes.
- Definir las condiciones de retamizaje de los recién nacidos con resultado positivo para alguna de las pruebas definidas.
- Identificar niños y niñas recién nacidos con condiciones de riesgo que requieren un seguimiento particular ante la posibilidad de padecer de hipoacusia, por la naturaleza de sus características de riesgo.
- Establecer los aspectos mínimos de oportunidad y características del diagnóstico de alteraciones auditivas, del inicio del tratamiento en el marco del plan de cuidado.
Definiciones
- Caso probable: recién nacido que no pasa la prueba con alguno de los métodos de tamización definidos Emisiones Otoacústicas (EOA) o con Respuesta Auditiva de Tallo Encefálico Automatizada (RATEA).
- Caso con tamizaje negativo sin antecedente de riesgo: recién nacido el cual pasa la prueba realizada en el tamizaje auditivo sin antecedentes de riesgo.
- Caso con tamizaje negativo, pero con antecedente de riesgo[13]: recién nacido el cual pasa la prueba realizada en el tamizaje auditivo pero que tiene antecedente de riesgo.
- Caso confirmado: caso probable en el cual se confirma por tecnología dura alteración auditiva.
- Niño o niña con seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de alteración auditiva congénita quien tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de pediatría con abordaje de su condición de mayor riesgo según lo señalado en la RPMS.
- Niño o niña sin seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de alteración auditiva congénita quien no tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de pediatría con abordaje de su condición de mayor riesgo según lo señalado en la RPMS
Tecnologías de tamizaje
- Emisiones Otacústicas (EOA):
Las Emisiones Otacústicas son sonidos producidos por la actividad de las células ciliadas externas en la cóclea que se registran en el Canal Auditivo Externo - CAE; proporcionan una medida de la audición y su registro e interpretación no requiere mucho tiempo ni un equipo muy costoso, son de fácil implementación lo que la hace útil en el programa de tamizaje universal.
Las células ciliadas externas del oído interno tienen la característica de contraerse por la presencia de actina generando energía mecánica que se transmite en forma de sonido hacia el conducto auditivo externo donde es registrado por un micrófono. También tiene como característica transformar el sonido que reciben del exterior en impulsos eléctricos, los cuales serán trasmitidos al cerebro a través del nervio Auditivo.
Las EOA reflejan el buen funcionamiento periférico de la vía auditiva ya que son el resultado de la actividad fisiológica de las células ciliadas externas, por lo que su presencia se relaciona con un buen funcionamiento de los mecanismos cocleares activos. Las EOA no determinan el umbral auditivo ni el grado de hipoacusia que presente la persona examinada. Están presentes en el 96-100% de las personas con audición normal, y desaparecen en pérdidas auditivas mayores a 35db; pero pueden estar ausentes cuando hay tapón de cerumen, líquido en el conducto auditivo externo o líquido en oído medio. Tienen una sensibilidad de 50% y una especificidad del 84%. (56)
Las EOA son rápidas de realizar y entregan una medición especifica, pero se ven alteradas por la presencia de ruido ambiental, por patologías a nivel del oído medio y no evalúan la fisiología de la vía auditiva retrococlear. (57)
- Respuesta Auditiva de Talio Encefálico Automatizada (RATEA).
También conocida como B.E.R.A. (Brainstem Evoked Responses Audiometry), es la prueba objetiva más utilizada en la actualidad; se puede aplicar a niños o niñas de edades muy tempranas. Son una poderosa herramienta para valoración objetiva de la audición. Permite determinar presencia o ausencia de hipoacusia evaluando la actividad periférica de la vía auditiva, ubicando el sitio de la lesión para realizar diagnóstico diferencial. Se obtiene a partir de electrodos de superficie que registran la actividad neuronal generada en la cóclea, nervio auditivo, y tronco cerebral en respuesta a los estímulos acústicos tipo click entregados a través de un auricular por conducción aérea, que produce información en las frecuencias de 2000- 4000Hz. Aparecen a los 10 milisegundos una serie de ondas (cinco), como respuesta neurológica a la señal auditiva, que coinciden con el paso por los diferentes núcleos nerviosos, donde se encuentran las sinapsis.
Los parámetros más importantes para valorar son las latencias de las ondas I, III y V, especialmente la V, dado que su desaparición nos permite reconocer el umbral de audición del sujeto explorado. Los BERA tienen una sensibilidad del 100% y una especificidad del 98%. (56)
Por ser una versión automatizada puede realizarse en ambientes ruidosos, tiene una muy alta especificidad, no se afecta por la presencia de líquido en el oído medio y permite identificar patología retrococlear (p ej: neuropatía auditiva). (57)
El tamizaje auditivo según el Comité Conjunto de Audición Infantil (JCIH), podrá ser realizado por equipos multidisciplinarios de profesionales, incluidos profesionales en fonoaudiologia, profesionales de medicina y profesionales en enfermería y en las instituciones donde se tenga disponibilidad de profesionales en audiología.
Procedimientos a seguir según los resultados del tamizaje
Según el Comité Conjunto de Audición Infantil (JCIH), la audición de todos los neonatos se debe evaluar a más tardar al mes de edad, en caso de alguna alteración en las pruebas iniciales realizar el retamizaje máximo al mes de edad y aquellos que no pasan la evaluación deben tener una evaluación audiológica integral a más tardar a los 3 meses de edad. Los bebés con pérdida auditiva confirmada deben recibir la intervención adecuada a más tardar a los 6 meses de edad por parte de profesionales de la salud y con experiencia en pérdida auditiva y sordera en la educación en primera infancia. (58)
Por lo anterior, para Colombia a partir de la Ruta Integral de Atención Materno Perinatal (RIAMP), se definió en los neonatos que: "dadas las limitaciones del uso exclusivo de EOA en la evaluación de la vía auditiva a nivel retrococlear, se debe preferir el uso de RATEA de rutina en todos los niños. En el caso de los recién nacidos y niños con alto riesgo de pérdida auditiva deben utilizarse de forma combinada las EOA y la RATEA. Estas pruebas deben realizarse idealmente antes del mes de vida. En caso en que no se logre garantizar su realización integral en el primer mes de vida, debe garantizarse en el marco de las atenciones de la Ruta para la Promoción y el Mantenimiento de la Salud para la primera infancia. Debe registrarse siempre en la historia clínica neonatal su realización y su resultado. Su implementación atenderá los criterios de progresividad y adaptabilidad que se requieran a nivel territorial para garantizar su realización". (59)
El Comité Conjunto de Audición Infantil (JCIH); definió que el tamizaje puede ser realizado por equipos multidisciplinarios de profesionales, incluidos profesionales en medicina, profesionales en enfermería y en las instituciones donde se tenga disponibilidad de profesionales en fonoaudiologia. Todos los miembros del equipo trabajan juntos para garantizar que el programa de tamizaje sea exitoso (58). En la figura 10, se muestra el esquema de atenciones en el marco del tamizaje auditivo.
Figura 10. Esquema de atenciones para tamizaje auditivo
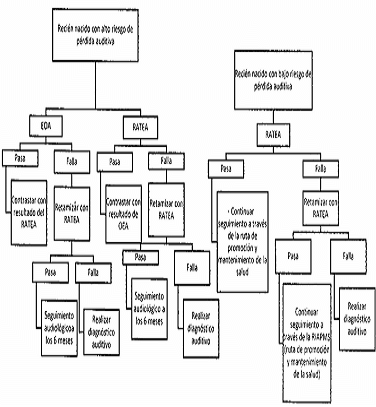
Fuente: Elaboración propia a partir de literatura referenciada.
Para el caso de los recién nacidos en los que se requiere realizar diagnóstico auditivo se realizará valoración audiológica, pruebas diagnósticas que permitan brindar resultados cuantitativos que lleven a! diagnóstico audiológico, en niños de 0 a 6 meses se usará la audiometría por observación del comportamiento y en niños entre los 5 meses a 2 años, audiometría con refuerzo visual. Es importante resaltar que, para establecer el diagnóstico definitivo, se requiere del análisis de un conjunto de pruebas audiológicas objetivas especializadas orientadas a determinar el estado o lesiones de oído, la disfunción vestibular, las alteraciones de la audición y los trastornos de la comunicación. Estos resultados permiten definir la conducta a seguir en el tratamiento otológico o audiológico y tomar decisiones de intervención con ayudas técnicas auditivas implantables, las cuales se deben garantizar de manera continua en la atención para reducir el riesgo de discapacidad.
4.3. Tamizaje neonatal visual
Corresponde a la detección de recién nacidos con alteraciones oculares o visuales al examen físico, con compromiso de la capacidad visual en diferentes espectros, que van desde afectaciones leves hasta severas ocasionando ceguera total, lo cual amenaza el desarrollo integral del niño o la niña en el curso de la vida o incluso causar la muerte (como en el caso del retinoblastoma).
En la Resolución 3280 de 2018 se mencionaba de forma muy general las técnicas que se debían realizar como parte de la atención del recién nacido en las primeras 24 a 48 horas de vida frente al tamizaje visual; adicional a lo anterior y de acuerdo a la Guía de Práctica Clínica para la detección temprana, el diagnóstico, el tratamiento y el seguimiento de los defectos refractivos en menores de 18 años, se describen cada una de estas técnicas con las respuestas normales y anormales para tener en cuenta por medio del examen físico y además se menciona que al encontrar alguna alteración, el médico, pediatra o neonatólogo deberá remitir de manera inmediata al especialista por oftalmología u oftalmología pediátrica.
Objetivos
- Identificar niños y niñas recién nacidos con alteraciones oculares por medio del examen físico.
- Definir las condiciones en las que se requiere remitir de manera inmediata a la valoración por oftalmología.
- Identificar niños y niñas recién nacidos con condiciones de riesgo que requieren un seguimiento particular ante la posibilidad de padecer de alteraciones visuales/oculares, por la naturaleza de sus características de riesgo.
- Establecer los aspectos mínimos de oportunidad y características del diagnóstico de alteraciones visuales, del inicio del tratamiento en el marco del plan de cuidado
Definiciones
- Caso probable: recién nacido con alteración visual/ocular identificada con los métodos de tamización (prueba del reflejo rojo, inspección externa y examen pupilar) a través de los hallazgos clínicos del examen físico.
- Caso con tamizaje negativo sin antecedente de riesgo: recién nacido en el cual no se evidencian alteraciones oculares en el tamizaje sin antecedentes de riesgo.
- Caso con tamizaje negativo, pero con antecedente de riesgo: recién nacido en el cual no se evidencian alteraciones oculares en el tamizaje pero que por antecedentes de riesgo requiere de seguimiento especial.
- Caso confirmado: caso sospechoso en el cual se confirma por oftalmología la alteración visual/ocular.
- Caso con valoración negativa: recién nacido en el cual se descarta por oftalmología la alteración visual/ocular.
- Niño o niña con seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de alteración visual congénita quien tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de pediatría con abordaje de su condición de mayor riesgo según lo señalado en la RPMS.
- Niño o niña sin seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de alteración visual congénita quien no tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de pediatría con abordaje de su condición de mayor riesgo según lo señalado en la RPMS
Tecnologías de tamizaje
La Guía de Práctica Clínica para la detección temprana, el diagnóstico, el tratamiento y el seguimiento de los defectos refractivos en menores de 18 años, indica que la búsqueda activa de alteraciones visuales en la población pediátrica sana se debe iniciar con una evaluación en el periodo neonatal y continuar durante cada visita de crecimiento y desarrollo. Teniendo en cuenta, que existen una serie de pruebas que se utilizan para identificar los defectos visuales en niños y niñas y su elección dependerá principalmente de la edad del niño o niña. (60)
De acuerdo con la misma guía, el tamizaje visual al momento del nacimiento debe ser realizado e interpretado por un profesional en neonatología, pediatría o en medicina general entrenado en las estrategias de detección de alteración visual. Para el tamizaje en neonatos, se establecen los siguientes aspectos que deben ser valorados:
1. Prueba del reflejo rojo
Para realizar la prueba del reflejo rojo adecuadamente, el examinador sostiene un oftalmoscopio directo cerca de su ojo con la potencia de la lente del oftalmoscopio en "0". En una habitación oscura, la luz del oftalmoscopio debe dirigirse hacia ambos ojos del niño simultáneamente desde una distancia de aproximadamente 18 a 30 pulgadas (45 a 75 centímetros). La potencia del lente del oftalmoscopio debe ser ajustado para garantizar la precisión del enfoque del examinador.
Se debe observar un reflejo rojo simétrico de ambos ojos para que pueda ser considerado normal. El reflejo rojo varía según la pigmentación de la retina y, por lo tanto, varía según raza/etnia. Opacidades en el reflejo rojo, un reflejo notablemente disminuido, la presencia de un reflejo blanco o amarillo, o asimetría de los reflejos (reflejo de Brückner) son todas indicaciones para derivación a un oftalmólogo con experiencia en el examen de niños. La excepción a esta regla es una opacidad transitoria de una película opaca en la película lagrimal que es móvil y desaparece por completo con el parpadeo (61).
Normal: El niño o la niña mira la luz. En ambos ojos el reflejo es igual.
Posibles diferencias en defectos refractivos: un reflejo rojo es más brillante que el otro.

Cuerpo extraño I abrasión (cornea izquierda): el reflejo rojo de la pupila retroiluminará defectos corneales o cuerpos extraños. El movimiento de la cabeza del examinador en una dirección parecerá mover la opacidad corneal en la dirección opuesta.
Estrabismo: el reflejo de luz corneal se desplaza temporalmente en el ojo derecho desviado, lo que indica endotropia.
2. Inspección externa
La inspección externa involucra la evaluación de los párpados, pestañas, el sistema lagrimal y la órbita. Debe ser evaluada en la anatomía de la cara (incluidos los párpados, la distancia interocular y la presencia o ausencia de pliegues de epicanto[14]), los bordes de la órbita y la presencia de anomalías oculofaciales deben ser evaluados.
También debe tenerse en cuenta la posición de la cabeza y la cara (incluyendo la inclinación, posiciones compensatorias, o la postura de la cabeza hacia arriba o hacia abajo). Características distintivas inusuales de la familia pueden sugerir la presencia de una anomalía congénita y merecen una evaluación de otras anormalidades físicas en el niño (p. Ej., Orejas, manos).
Niños o niñas que tienen pliegues epicantales prominentes y/o un puente nasal plano y ancho y una alineación binocular normal a menudo tienen la ilusión de una endotropia[15] (pseudoendotropía). (61)
3. Examen pupilar
Se debe evaluar el tamaño, la forma, la simetría y la respuesta a la luz de las pupilas. Para establecer diferencias en el tamaño de la pupila estas deben observarse con poca luz. Una diferencia de más de un milímetro puede ser clínicamente significativa. La reactividad pupilar se observa al ¡luminar con la luz directamente cada ojo. La prueba de luz con intercambios entre luz y penumbra se utiliza para evaluar la presencia de un defecto pupilar aferente.
En una habitación oscura se ubica la luz de la linterna en el ojo derecho durante menos de 5 segundos, con el niño o niña fijando en un lugar distante, la pupila, debe contraerse. A continuación, la luz se lleva rápidamente por el puente nasal hacia el ojo izquierdo y la respuesta pupilar se observa sobre el ojo derecho. La linterna se balancea hacia atrás y adelante varias veces.
Una respuesta normal es la constricción pupilar. La respuesta anormal es la dilatación pupilar cuando la luz brilla en el ojo lo que es indicativo de un defecto pupilar aferente. Un defecto pupilar aferente suele ser un signo de un problema unilateral con el nervio óptico o de otras áreas en la vía visual anterior. La evaluación pupilar en neonatos puede ser un desafío debido a los frecuentes cambios en el paciente, fijación y enfoque. (61)
4. Reflejo luminoso corneal
Esta prueba compara la posición del reflejo de la luz sobre la córnea en los dos ojos. El examinador debe alinearse al niño o niña y fijar la luz de la linterna desde una distancia de 12 pulgadas (30 centímetros). Se deben observar las posiciones de los dos reflejos corneales. Con la reflexión normal de la luz corneal, los reflejos simétricos son centrados o ligeramente desplazados nasalmente.
Si los ojos están desalineados, los reflejos serán simétricos. Si hay endotropia, un reflejo se desplazará temporalmente. Si la exotropia está presente, un reflejo será desplazado nasal. Si hay una desalineación vertical, un reflejo se desplazará hacia arriba o hacia abajo. (61).
Procedimientos a seguir según los resultados del tamizaje
Los métodos incluidos en la tabla 12, son los que se consideraron en la guía de práctica clínica en Colombia, pueden ser practicados en neonatos por los profesionales de la salud.
Tabla 12. Métodos de tamización en neonatos
| Método | Signos indicadores de remisión |
| Prueba del reflejo rojo | Ausente, blanco, opaco o asimétrico |
| Inspección externa | Anormalidad estructural, por ejemplo: ptosis. |
| Examen pupilar | Forma irregular, tamaño desigual, pobre o inadecuada reacción a la luz |
| Reflejo luminoso corneal | Asimétrico o desplazado |
Adoptada de la Guía AAO Pediatric Ophthalmology/Strabismus Panel. PPP. Pediatric eye evaluations. San Francisco CA. AAO. 2012 y ajustada al contexto local por el Grupo Desarrollador de la Guia de Práctica Clínica para la detección temprana, el diagnóstico, el tratamiento y el seguimiento de los defectos refractivos en menores de 18 años.
- Ante cualquiera de los signos indicadores de remisión se considera como un hallazgo positivo al examen físico y debe ser remitido de manera inmediata a valoración por oftalmología o por oftalmología pediátrica según la disponibilidad.
- Los recién nacidos prematuros por el riesgo de ROP serán diagnosticados y tratados de acuerdo con los lineamientos vigentes del programa canguro.
- Para el caso de diagnóstico de lesiones obstructivas del eje visual, el inicio del tratamiento no deberá superar los 45 días.
- Se debe realizar la búsqueda directa de antecedentes familiares de retinoblastoma, considerando el alto porcentaje asociado a componente hereditario.
- Para las patologías infecciosas, ROP y retinoblastoma el inicio del tratamiento debe ser inmediato.
- En ningún caso el inicio del tratamiento superará los 3 meses del nacimiento del niño o niña
En la figura 11 se condensan las atenciones y conductas en el marco del tamizaje visual. Además de esto, se han documentado factores de riesgo que ameritan un seguimiento especial por pediatría (todos ellos considerados niños o niñas con mayor riesgo[16]) con remisión durante el primer mes a oftalmología, aun cuando el resultado del tamizaje sea negativo[17].
- Síndrome dismórfico / genético o sospecha - Anomalía craneofacial
Las alteraciones funcionales y estructurales de la vía visual aparecen desde el desarrollo embrionario y fetal, evidenciándose así desde el nacimiento, por lo que para el clínico esto representa un reto para realizar el diagnóstico preciso y así otorgar un asesoramiento adecuado, situación que se complica cuando se presentan anomalías múltiples o también los llamados síndromes polimalformativos.
Los defectos de la visión que suelen originar estas anomalías pueden producir ceguera total o parcial. Según su patogenia, las anomalías oculares pueden ser resultado de una anomalía anatómica o de un defecto bioquímico. Las alteraciones de la visión pueden ser de origen prenatal y presentarse en el periodo neonatal, además de producirse mediante una pérdida progresiva de la visión o ser tardías (62).
- Hijo o hija de madre con infección gestacional o perínatal con alto riesgo de malformaciones, problemas del desarrollo o necesidad de atención especial en salud en el niño (Por ejemplo, exposición a Sífilis, Toxoplasmosis, Rubéola, Citomegalovirus, Herpes virus, VIH, Zika virus):
En el recién nacido existen características clínicas que sugieren TORCH o infección congénita tales como retardo del crecimiento intrauterino, rash, petequias, púrpura, ictericia, hepatomegalia, esplenomegalia, linfadenopatía, hidrocefalia, calcificaciones intracraneales, sordera, anormalidades cardíacas, neumonía y anormalidades esqueléticas. Oculares como coriorretimtis (Toxoplasma, rubéola, citomegalovirus, herpes simple, sífilis); cataratas (rubéola, citomegalovirus); glaucoma (rubéola); microftalmia (toxoplasma, rubéola, citomegalovirus); conjuntivitis (herpes simple) y miopía (rubéola congénita). (63)
En 2015, el mundo se vio afectado por un brote de infección por virus del Zika (ZIKV, por sus siglas en inglés), que comenzó en las islas del Pacífico Sur y se propagó a Brasil y otros países de las zonas tropicales de América Latina. Aunque el comportamiento clínico de la enfermedad es el de un síndrome febril agudo, la mayor preocupación fue la confirmación de su efecto neurotrópico y la relación causal directa con microcefalia en RN de las zonas con una mayor incidencia por el brote en Brasil. (64)
En Colombia, según la información reportada al Sistema de Vigilancia en Salud Pública (SIVIGILA), se evidencia la relación positiva entre infección por ZIKV en gestantes y aparición de microcefalia durante el brote hasta cuarenta semanas posteriores al pico de notificación por ZIKV. (65). Por el riesgo de la detección de patologías infecciosas de manera tardía, a todo recién nacido sin control prenatal o con menos de 4 controles prenatales se le debe garantizar el tamizaje por oftalmología y la realización de las pruebas de detección de acuerdo con los protocolos establecidos para cada patología.
- Síndrome de Down:
Según el estudio de Zarante et all, en la evaluación y pronóstico de 52.744 nacimientos en tres ciudades colombianas, el síndrome de Down ocupó el cuarto lugar en frecuencia con una tasa de 17,8 por 10.000 nacimientos en las ciudades estudiadas. (66) Las alteraciones visuales y oculares en los pacientes con síndrome de Down son las mismas que aquejan a la población infantil en general, pero en estos pacientes ocurren con mayor frecuencia y en un grado más marcado. (67)
Las anomalías oculares y visuales más frecuentes en pacientes con síndrome de Down son: defectos refractivos, de los cuales la hipermetropía es el más frecuente, seguido de la miopía y el astigmatismo; trastornos de acomodación, ambliopía, estrabismo; nistagmos, cataratas, obstrucción del conducto naso-lagrimal, blefaritis, conjuntivitis, queratocono, entre otros. (67)
- Antecedente familiar hasta tercer grado de consanguineidad de enfermedades visuales/oculares genéticas o congénitas: retinoblastoma, glaucoma congénito, catarata o ceguera congénitas.
El retinoblastoma es la primera enfermedad para la cual se ha descrito una etiología genética. En aproximadamente el 55% de los casos se ha determinado su origen hereditario en su mayoría generando la formal bilateral de retinoblastoma, así como el 15% de las formas unilaterales. (68).
En glaucoma congénito la mayoría de los casos son esporádicos, es decir sin agregación familiar; cuando se hereda se transmite como un rasgo autosómico recesivo, el cual es más común en ciertas poblaciones consanguíneas. (69) Sin embargo, el antecedente es relevante para la valoración oftalmológica antes del primer mes. Aunque tradicionalmente se ha descrito que aproximadamente un tercio de las cataratas infantiles se heredan, un tercio está asociado con otras enfermedades o síndromes, y el tercio restante es idiopático. La clasificación etiológica de la catarata infantil no es tan simple y directa. Diferentes estudios dan resultados variables. Las causas importantes de catarata infantil en niños más pequeños incluyen aberraciones genéticas, trastornos metabólicos, prematuridad, e infecciones intrauterinas. (70)
En todas las regiones del mundo la catarata, algunas enfermedades de la retina (principalmente distrofias retinianas hereditarias) y las anomalías congénitas que afectan el ojo son causas importantes de ceguera, siendo la etiología genética una causa importante en todo el mundo. (71). Por eso, se debe indagar siempre por antecedentes familiares de ceguera congénita y deben ser valorados por oftalmología durante el primer mes de vida.
Figura 11. Resultados del tamizaje visual en el neonato.
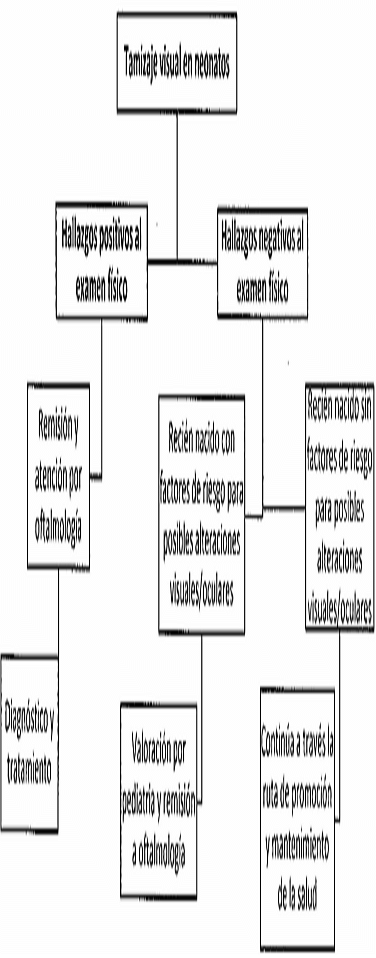
Fuente: Elaboración propia a partir de literatura referenciada.
Los recién nacidos con alguna alteración evidente detectada en el tamizaje visual neonatal, deberán ser valorados en una consulta de primera vez por oftalmología o por interconsulta por especialista en oftalmología pediátrica, garantizando así su diagnóstico y remisión según la condición; lo anterior, con la finalidad de reducir el riesgo de discapacidad.
4.4. Tamizaje de cardiopatía congénita
Corresponde a la detección de cardiopatía congénita compleja por medio de la saturación de oxígeno (pulsooximetría) pre y postductal. Las cardiopatías congénitas son las malformaciones (anomalías o defectos) congénitas más frecuentes y las que causan mayor mortalidad por este motivo, en niños menores de cinco años en Colombia. Se estima que 8 de cada 1000 recién nacidos nace con una cardiopatía congénita y que aproximadamente 2-3 de cada 1000 nacidos vivos tiene una cardiopatía congénita compleja. Sin embargo, se considera que la verdadera incidencia puede llegar a ser más alta teniendo en cuenta que muchos óbitos fetales se pueden producir asociados a cardiopatías incompatibles con la vida (72).
Se define como cardiopatía congénita toda anomalía estructural del corazón, o de los grandes vasos intratorácicos, que real o potencialmente tiene significado funcional y que se origina durante el desarrollo embrionario cardiovascular, está presente al nacimiento y puede ser incluso diagnosticada en el período prenatal. Sin embargo, al hablar de cardiopatías congénitas complejas, el tamizaje neonatal se ha orientado a la identificación de las siguientes patologías: Síndrome de corazón izquierdo hipoplásico, Atresia pulmonar, Tetralogía de Fallot, Drenaje venoso pulmonar anómalo total, Transposición de grandes arterias, Atresia tricúspidea y Tronco arterioso (Circulation, 2018).
Frente a los defectos congénitos, uno de los mayores adelantos científicos ha sido el diagnóstico antenatal, lo que permite anticipar el plan de atención del recién nacido y organizar el lugar del parto con un nivel adecuado de atención y equipos multidisciplinarios, así como brindar información y acompañar a las familias. En el caso de las cardiópatas congénitas, la situación no es diferente.
En general, el 80% de las cardiopatías congénitas se detectan por ultrasonido prenatal, o son evidentes clínicamente al nacimiento. Del 20% que habitualmente no se detectan, la oximetría de pulso puede identificar un 15%, quedando tan solo un 5% aproximado sin pauta de detección temprana. (73)
El tamizaje de cardiópata congénita compleja fue uno de los procedimientos incluidos en la atención para el cuidado del recién nacido de los Lineamientos Técnicos y Operativos de la RIAMP de la Resolución 3280 de 2018, por lo que, si bien no fue descrita de forma explícita en la Ley 1980 de 2019, por el antecedente normativo, pero sobre todo por la carga de morbimortalidad que representa se incluye dentro del Programa de Tamizaje Neonatal.
En la Resolución 3280 de 2018 se menciona de forma muy general la realización de este examen, sin embargo como patología parte del Programa de Tamizaje Neonatal fue necesario ajustar la información para dar cuenta de la técnica correcta a utilizar, el perfil del profesional que se encargará de hacer el tamizaje y el perfil encargado de la interpretación del mismo, al igual que se incluyen los flujogramas que permiten seguir el paso a paso del tamizaje de acuerdo a la altura geográfica en que se encuentre el paciente y así mismo se menciona la tecnología confirmatoria requerida y la valoración por el especialista para definir tratamiento.
Es fundamental tener en cuenta que el tamizaje neonatal de cardiopatía congénita compleja debe ser evaluado de forma articulada con la información que pueda obtenerse de la atención para el cuidado prenatal de la madre gestante, especialmente en relación con la identificación de aneuploidías y la realización de las ecografías prenatales, teniendo en cuenta que la evaluación antenatal no es suficiente para la identificación temprana de cardiopatías congénitas.
En el contexto del Programa de Tamizaje Neonatal, todo niño o niña con un tamizaje positivo debe ser atendido integralmente con un criterio de URGENCIA VITAL, puesto que la cardiopatía congénita compleja tiene una alta probabilidad de mortalidad en el período neonatal.
Objetivos de la línea de tamizaje de cardiopatía congénita compleja
- Identificar niños y niñas recién nacidos vivos con sospecha de cardiopatía congénita compleja por medio de la evaluación de la pulsooximetría pre y postductal, que no hayan tenido diagnóstico prenatal.
- Describir el procedimiento del tamizaje de cardiopatía congénita compleja y definir las pautas de actuación ante el tamizaje positivo.
- Establecer los elementos mínimos de oportunidad e interrelación del tamizaje de cardiopatía congénita compleja, con su evaluación diagnóstica e inicio de tratamiento en el marco del plan de cuidado.
Definiciones de la línea de tamizaje de cardiopatía congénita compleja
En el contexto del Programa de Tamizaje Neonatal, frente a la cardiopatía congénita compleja se precisan las siguientes definiciones:
- Pulsooximetría: es una técnica no invasiva, que mide la saturación de oxígeno en la hemoglobina de los eritrocitos.
- Pulsooximetría preductal: registro de la pulsooximetría realizada en la mano derecha del recién nacido con el transductor adecuado (para población neonatal).
- Pulsooximetría postductal: registro de la pulsooximetría realizada en el pie derecho o el pie izquierdo del recién nacido con el transductor adecuado (para población neonatal).
- Niño o niña perdido del Programa de Tamizaje Neonatal: recién nacido vivo en quien no se realiza el tamizaje neonatal o en quien no se realizan las pruebas de confirmación diagnóstica a pesar de haber tenido un tamizaje positivo. Debe tenerse en cuenta en qué punto se pierden los niños o las niñas con el objeto de tomar las medidas necesarias para evitar esta situación.
- Niño o niña excluido del Programa de Tamizaje Neonatal: recién nacido vivo a quien se realizó el tamizaje pero que fallece antes del diagnóstico habiendo tenido un tamizaje positivo. Se incluyen también los niños y las niñas con diagnóstico prenatal de cardiopatía.
Respecto al resultado obtenido, el tamizaje puede definirse como:
- Tamizaje positivo: recién nacido con pulsooximetría a las 24 horas del nacimiento por debajo del punto de corte o con una diferencia mayor a 3% entre la pulsooximetría pre y post ductal, según el procedimiento de tamizaje.
- Tamizaje negativo: recién nacido con pulsooximetría a las 24 horas del nacimiento por encima del punto de corte y con una diferencia menor a 3% entre la pulsooximetría pre y post ductal según el procedimiento de tamizaje.
Respecto al diagnóstico de cardiopatía congénita compleja dentro del Programa de Tamizaje Neonatal, se tendrán en cuenta las siguientes definiciones:
- Diagnóstico confirmado de cardiopatía congénita: recién nacido con tamizaje de cardiopatía congénita positivo a quien se le realiza diagnóstico de cualquier cardiopatía congénita.
- Diagnóstico descartado de cardiopatía congénita: recién nacido con tamizaje positivo para cardiopatía congénita en quien no se identifican alteraciones cardiovasculares estructurales durante la evaluación diagnóstica.
En relación con el tratamiento dentro del Programa de Tamizaje Neonatal, se especifican las siguientes definiciones:
- Niño o niña con tratamiento: niño o niña con diagnóstico confirmado de cardiopatía congénita quien se encuentra en tratamiento médico o ha recibido tratamiento quirúrgico o intervencionista, se encuentra en programación de cirugía u otra intervención, o está en manejo expectante por indicación médica.
- Niño o niña sin tratamiento: Niño o niña con diagnóstico confirmado de cardiopatía congénita quien se encuentra sin tratamiento ni seguimiento por cardiología pediátrica a pesar de estar indicado por causa de su diagnóstico.
- Niño o niña sin información de tratamiento: Niño o niña con diagnóstico confirmado de cardiopatía congénita en quien no se cuenta con información sobre tratamiento médico, quirúrgico o intervencionista por causa de su patología
- Niño o niña con seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de cardiopatía congénita compleja quien tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de pediatría con abordaje de su condición de mayor riesgo según lo señalado en la RPMS.
- Niño o niña sin seguimiento en el marco de la RPMS: niño o niña con diagnóstico confirmado de cardiopatía congénita compleja quien no tiene seguimiento en la consulta de valoración integral en salud por profesional de pediatría o medicina con apoyo de pediatría con abordaje de su condición de mayor riesgo según lo señalado en la RPMS
Estas definiciones serán empleadas en la formulación, la evaluación y el seguimiento del Programa de Tamizaje Neonatal, en la línea específica de cardiopatía congénita, pero que no generan conflicto frente a las definiciones que puedan tenerse en el SIVIGILA, puesto que este es solo un elemento del funcionamiento del Programa de Tamizaje Neonatal y no lo abarca completa ni integralmente.
NOTA: debe considerarse que un niño o una niña puede tener cardiopatía congénita y manifestarla posterior a haber tenido un tamizaje negativo, lo que debe comunicarse también a las familias. De otro lado, todos los casos de cardiopatía congénita deben reportarse al SIVIGILA, incluso aquellos que tienen diagnóstico prenatal y que por este motivo fueron excluidos del Programa de Tamizaje Neonatal.
Procedimiento de tamizaje de cardiopatía congénita compleja.
El tamizaje de cardiopatía congénita compleja se realiza a través de la medición de la saturación de oxígeno en la hemoglobina de los eritrocitos por medio de la pulsooximetría. Esta pulsooximetría debe hacerse en la palma de la mano derecha (preductal) y en la región distal de cualquiera de los pies, (postductal) a todo recién nacido a término, aparentemente sano. Puede hacerse en serie (uno seguido del otro, es decir, de forma secuencial) o en paralelo (pre y postductal simultáneamente), hasta obtener una lectura confiable (se alcanza cuando hay regularidad y/o estabilidad de la onda registrada en el pulsooxímetro o si existe alguna indicación de que el dispositivo está monitoreando adecuadamente la frecuencia cardiaca del recién nacido) (AAP, 2025).
Este tamizaje podrá ser realizado por profesionales en enfermería, profesionales en medicina general, especialistas en pediatría o en neonatología y debe hacerse entre las 24 y las 48 horas del nacimiento o lo más cercano a esta ventana de tiempo antes del egreso hospitalario del recién nacido, en el caso en el que sea dado de alta antes del tiempo establecido en la Resolución 3280 de 2018 o la norma que la sustituya o la modifique. A este respecto, la IPS que atiende al recién nacido debe garantizar la estancia hospitalaria de mínimo 24 horas para todos los recién nacidos a término, sin riesgos ni complicaciones. Igualmente, la IPS debe garantizar el desarrollo de capacidades de los profesionales encargados de realizar el tamizaje neonatal de cardiopatía congénita. El líder o referente de tamizaje neonatal de la IPS debe verificar regularmente la forma como los profesionales practican el tamizaje de cardiopatía congénita compleja y debe adoptar las medidas a las que haya lugar para garantizar su adecuada realización. Debe quedar por escrito esta verificación, la formulación del plan de mejora necesario y su implementación.
El tamizaje se hace mediante un proceso que puede ser de un solo paso, o repetido en hasta dos pasos, según los hallazgos que se vayan presentando. Se recomienda realizar el tamizaje durante el estado de alerta del niño o niña para reducir la posibilidad de que se presente una hipoxemia relacionada con hipoventilación durante el sueño profundo. Sin embargo, no existe un criterio de incondicionalidad respecto al estado de sueño-vigilia del recién nacido para realizar el tamizaje. De otro lado, el recién nacido debe estar respirando el aire ambiente (no tener oxígeno suplementario), estar tranquilo y en un ambiente térmicamente adecuado.
Existen estudios que demuestran que pueden presentarse diferencias significativas de forma normal en la pulsooximetría según la altitud en la que viven los recién nacidos, pero también dependiendo de la edad de los niños en el momento del registro de la oximetría y del tipo de pulsooxímetro que se utilice para la medición. Esto quiere decir que la práctica (y también el programa) de tamizaje neonatal de cardiopatía congénita compleja de un país debe considerar variables y características propias de la población, de la altitud en la que nacen los niños y de las prácticas de atención de los recién nacidos, lo que podrá verse reflejado en tasas de falsos positivos en mayor o menor grado, que pueden tener como consecuencias la ansiedad parental ante la posibilidad de que sus hijos tengan una cardiopatía congénita (con la posible afectación secundaria del vínculo, el relacionamiento de los padres con sus hijos y las prácticas de cuidado de los niños) y el mayor costo del Programa de Tamizaje Neonatal (Diferencias de pulsooximetría por altitud, 2008; 2013).
Adicionalmente, debe tenerse en cuenta que el Programa de Tamizaje Neonatal de Colombia frente a la línea de cardiopatía congénita compleja, incluye elementos adicionales de valoración del recién nacido complementarios a la toma de la pulsooximetría, lo que representa una medida complementaria para detectar niños con posible cardiopatía congénita que hayan sido posibles falsos negativos en el tamizaje. De esta forma, a partir del protocolo implementado por la Academia Americana de Pediatría, el Colegio Americano del Corazón y la Asociación Americana del Corazón para el tamizaje de cardiopatía congénita compleja, en el contexto del Programa de Tamizaje Neonatal de Colombia, se considera ajustar los puntos de corte y adaptar el protocolo de tamizaje según la altitud y previendo también los distintos resultados que pueden presentarse como consecuencia de la progresiva adherencia a la indicación de estancia hospitalaria de mínimo 24 horas para los recién nacidos sanos, a término. (74)
Sin embargo, se aclara que esta adaptación del protocolo y de los puntos de corte del Programa de Tamizaje Neonatal de cardiopatía congénita compleja de Colombia podrá ser revisada y ajustada posteriormente a partir del análisis que se haga del funcionamiento del programa y considerando las generalidades y las particularidades de la prestación de los servicios de salud en el país. Teniendo en cuenta lo anteriormente mencionado, el tamizaje neonatal de cardiopatía congénita para recién nacidos de lugares con una altitud menor a 1.500 m.s.n.m, se debe realizar según lo descrito en la figura 12. Así mismo, el tamizaje neonatal de cardiopatía congénita para recién nacidos de lugares con una altitud mayor o igual a 1.500 m.s.n.m., se deberá hacer según lo definido en la figura 13.
Figura 12. Esquema tamizaje neonatal de cardiopatía congénita en recién nacidos en lugares con altitud menor a 1.500 m.s.n.m, (MSPS. Adaptado de AAP, 2025)
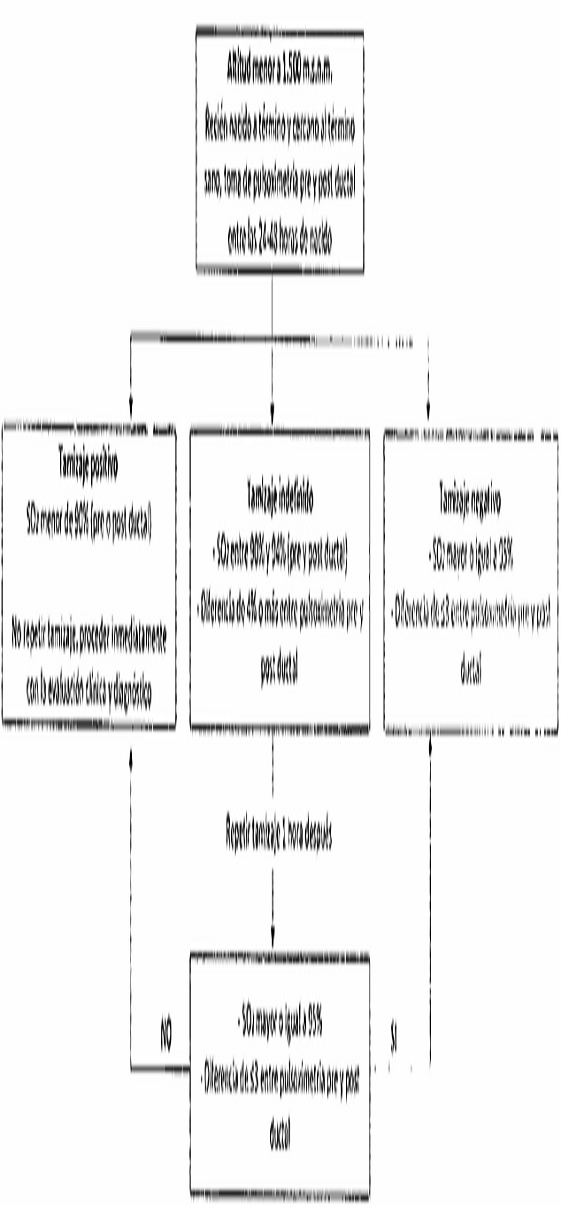
Fuente: Elaboración propia a partir de literatura referenciada.
Figura 13. Flujograma de tamizaje neonatal de cardiopatía congénita en recién nacidos en lugares con altitud mayor o igual a 1.500 m.s.n.m. (MSPS, Adaptado de AAP, 2025)
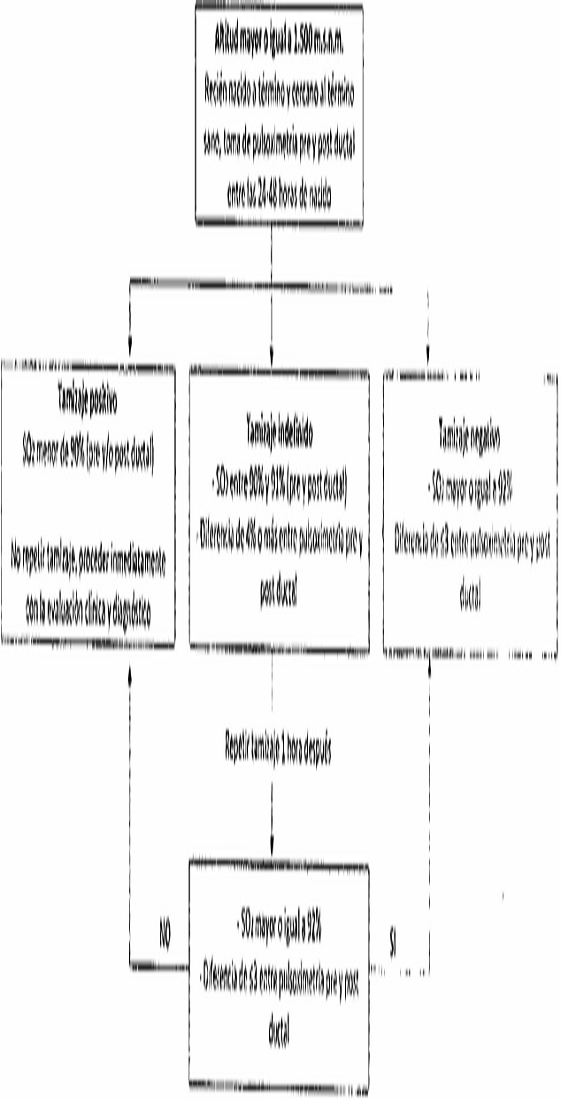
Fuente: Elaboración propia a partir de literatura referenciada.
Interpretación del tamizaje de cardiopatía congénita
El tamizaje neonatal de cardiopatía congénita (como práctica de tamizaje dirigida a identificar grupos de niños con riesgo de presentar una cardiopatía congénita) se realizará al universo de recién nacidos a término y cercanos al término (con prematuridad leve de 35 semanas o más), y que se encuentren aparentemente sanos. Se excluyen del tamizaje los recién nacidos prematuros puesto que ellos ya se consideran población de riesgo y requieren una atención integral que implica monitorización invasiva o no invasiva (según el estado clínico del paciente) ya que pueden presentar hipoxemia por inmadurez orgánica relacionada con la prematuridad, lo cual va a producir inmediatamente un resultado positivo del tamizaje.
El tamizaje de cardiopatía congénita será interpretado por un profesional en neonatología, profesional en pediatría o profesional en medicina general entrenado en la interpretación de los resultados del tamizaje de cardiopatía del o la recién nacido (a).
Así mismo, se excluyen los recién nacidos enfermos, puesto que la hipoxemia es un indicador frecuente de enfermedad en los neonatos, que inmediatamente va a resultar en un tamizaje positivo, pero que además por causa de su enfermedad en particular, van a recibir distintas medidas de atención integral en salud en la fase aguda y en su seguimiento. No obstante, debe tenerse en cuenta que la cardiopatía congénita compleja puede llevar a deterioro clínico del neonato en las primeras 24 horas de vida, antes de la realización del tamizaje neonatal, por lo que la historia clínica y el examen físico son indispensables en la posible detección de una patología de este tipo como responsable del deterioro. En todo caso, el resultado final del procedimiento de tamizaje neonatal de cardiopatía congénita compleja podrá ser solamente positivo o negativo.
El resultado del tamizaje será positivo cuando: 1) El niño o la niña presente una saturación menor a 90% en cualquier momento del tamizaje y a cualquier altitud, y 2) Cuando presente una diferencia de 4% o más entre la pulsooximetría pre y postductal (independiente de cuál sea la mayor) en la medición repetida y a cualquier altitud.
El resultado del tamizaje será negativo cuando: 1) El niño o la niña presente una saturación mayor o igual al punto de corte según la altitud en la primera o en la segunda medición (95% por debajo de los 1.500 m.s.n.m. y 92% por encima de los 1.500 m.s.n.m.) y no tenga una diferencia de 4% o más entre la pulsooximetría pre y postductal en ninguna de las mediciones; y 2) Cuando tenga una saturación mayor o igual a 90% en la tercera medición de pulsooximetría, en el caso en el que haya estado indicada la repetición, y no tenga una diferencia significativa entre las saturación pre y postductal (mayor al 3%).
La pulsooximetría preductal puede ser mayor que la post ductal en casos de corto circuito de derecha a izquierda con ductus abierto, como en la hipertensión pulmonar suprasistémica. A su vez, la pulsooximetría post ductal puede ser mayor que la preductal en casos de corto circuito de izquierda a derecha con ductus abierto, como en la Transposición de grandes arterias. Por este motivo, se valora la diferencia entre pulsooximetrías pre y postductales y no la predominancia de una de ellas sobre la otra.
NOTA debe tenerse en cuenta que un resultado de tamizaje negativo NO descarta del todo, una cardiopatía congénita (ni siquiera una cardiopatía congénita compleja), especialmente aquellas que no son dependientes del ductus, por lo que deben analizarse siempre los demás datos que puedan ser recuperados en la anamnesis y en el examen físico general y en el examen cardiovascular, incluyendo la toma de tensión arterial en las cuatro extremidades, ya establecida en la Resolución 3280 de 2018 o la norma que la modifique o sustituya.
Claves para un correcto tamizaje
Debe garantizarse que todos los equipos, dispositivos e insumos para la realización, tanto del tamizaje como de la evaluación diagnóstica, sean adecuados para la evaluación de recién nacidos, lo que incluye el pulsooxímetro, el electrocardiógrafo y el ecocardiógrafo.
A nivel del tamizaje, el oxímetro de pulso consta de tres partes: 1) El monitor (donde se encuentra la pantalla con los valores y la onda pletismográfica de la saturación de oxígeno o un equivalente), 2) el cable, y 3) el sensor (con la fuente de luz y el detector). Se recomienda emplear el pulsooxímetro con sensor de cinta adhesiva y no uno de pinza, puesto que este último plantea mayores riesgos de alteraciones en el registro.
En la figura 14, se presenta como modelo un procedimiento de tamizaje neonatal con un sensor de cinta adhesiva.
Figura 14. Modelo de realización de tamizaje neonatal de cardiopatía congénita con pulsooxímetro con sensor de cinta adhesiva.

(Imagen generada con inteligencia artificial. OpenAl, 2025)
Para el correcto tamizaje, se debe emplear solamente un sensor neonatal, y asegurarse que el sensor esté en contacto con la piel, sin lesionarla.
- No debe haber espacios entre el sensor y la piel.
- El sensor debe quedar fijo por sí solo, no se recomienda usar la mano u otro adhesivo para sostenerlo.
- Si el recién nacido está llorando, temblando, con frió o en sueño profundo, la lectura puede estar equivocada.
Asimismo, la fuente de luz y el detector del sensor deben estar alineados. Debe cubrirse el sensor para evitar la interferencia con la luz, y durante la medición, se debe evaluar la correlación adecuada entre la onda de pulso y la frecuencia cardíaca del niño.
Actuación frente a un tamizaje positivo para cardiopatía congénita
Todo recién nacido con tamizaje positivo para cardiopatía congénita debe ser hospitalizado y atendido con criterio de URGENCIA, puesto que las cardiopatías congénitas susceptibles de tamizaje tienen una alta probabilidad de generar mortalidad neonatal a corto plazo. En este sentido, ante un tamizaje positivo para cardiopatía congénita se debe garantizar la valoración completa del estado físico del niño inmediata (para considerar causas adicionales de hipoxemia e incluyendo la toma de tensión arterial), la estabilización que el niño pueda requerir según su estado clínico, la valoración por cardiología pediátrica y la toma de Ecocardiograma transtorácico con Doppler a color (realizado por cardiólogo pediatra). Teniendo en cuenta lo anterior, los niños y las niñas con tamizaje positivo deben ser hospitalizados en una Unidad de Cuidados Intensivos Neonatales y deben permanecer monitoreados.
En caso de no contar con cardiólogo pediatra ni con ecocardiograma en la institución en la que nació el niño, la EAPB debe garantizar el traslado URGENTE a,institución en la que se pueda realizar la confirmación diagnóstica e iniciar el tratamiento que el niño requiera según su patología y su estado clínico. En todo caso, la valoración por cardiología pediátrica y la realización del ecocardiograma debe ser garantizado dentro de las 24 horas siguientes a obtener el resultado positivo del tamizaje neonatal.
Se recomienda que antes de la valoración por cardiología pediátrica y la realización del ecocardiograma, al recién nacido con tamizaje positivo para cardiopatía congénita se le realice un electrocardiograma (EKG) completo (que incluya las derivaciones derechas V3R y V4R) y una radiografía de tórax (en proyecciones anteroposterior y lateral). Sin embargo, la realización del EKG y de la radiografía de tórax no debe considerarse un requisito (y, por lo tanto, una potencial barrera) para acceder a la valoración por cardiología pediátrica ni para la realización del ecocardiograma con Doppler.
Identificación y valoración de niños con riesgo y/o sospecha de cardiopatía congénita susceptibles de no ser detectados por el tamizaje neonatal
La elaboración de la historia clínica con enfoque antenatal de riesgo, valorando adecuadamente los antecedentes familiares y obstétricos, y la realización del examen físico completo, y también el específico cardiovascular, son fundamentales para identificar grupos de niños con riesgo y/o sospecha de cardiopatía congénita, que, en algunos casos, pueden tener tamizaje negativo.
A continuación, se describen los elementos más importantes para tener en cuenta tanto en la anamnesis como en el examen físico para la detección de riesgo o de una posible cardiopatía congénita en un recién nacido (independiente del resultado del tamizaje neonatal):
Datos de anamnesis:
- Datos de evaluación antenatal de cromosomopatías o de defectos congénitos por ecografía prenatal de detalle anatómico.
- Prematuridad.
- Recién nacidos macrosómicos.
- Sospecha de síndromes genéticos como el Síndrome de Down (se asocia con Canal AV, CIA, CIV, Tetralogía de Fallot, Ductus Arteriosus Persistente-DAP), Trisomía 13 y 18 (CIV, Coartación de Aorta, Displasias polivalvulares y Cardiopatías complejas), Síndrome de Noonan (Estenosis pulmonar, CIA y Miocardiopatía), Síndrome de Williams, (Estenosis aórtica supravalvular), Síndrome de DiGeorge (Interrupción del arco aórtico, Tronco arterioso).
- Defectos congénitos como los asociados a rubéola congénita (se asocian con DAP y estenosis pulmonar periférica), Asociación CHARGE (CIA, CIV, DAP), Asociación VACTERL (CIV, Tetralogía de Fallot).
- Hijo o hija de madre con enfermedades maternas como la Diabetes (se asocia con hipertrofia septal asimétrica y con transposición de grandes arterias) o el Lupus Eritematoso Sistémico (se asocia con Bloqueo Aurículo Ventricular Completo, requiere EKG y ecocardiograma).
- Hijos o hijas de madres con exposición a agentes físicos o químicos como el alcohol (Comunicación Interauricular-CIA o Comunicación Interventricular-CIV), Litio (Anomalía de Ebstein), fármacos o drogas como el ácido retinoico (Cardiopatías troncoconales), Ácido Valproico (CIA, CIV, Estenosis aórtica, Coartación aórtica, Atresia pulmonar sin CIV), la talidomida, anfetaminas y AINES (alteran los procesos de maduración de la musculatura lisa a nivel arteriolar pulmonar y ductal en el tercer trimestre del embarazo con posible Hipertensión Pulmonar).
Adicional a los demás elementos fundamentales del examen físico general completo que puedan sugerir una patología aguda o una comorbilidad, en el contexto de la atención neonatal y del Programa de Tamizaje Neonatal, siempre deben tenerse en cuenta los siguientes aspectos en relación con el examen cardiovascular:
- Frecuencia cardiaca: taquicardia o bradicardia.
- Cianosis: aunque debe tenerse en cuenta que no todas las cardiopatías congénitas producen cianosis.
- Hiperdinamia precordial: siempre es considerada anormal y sugestiva de cardiopatía congénita. Indica sobreesfuerzo cardiaco.
- Punto de Máximo Impulso: permite valorar la posibilidad de sobrecarga de trabajo de segmentos anatómicos específicos del corazón y puede sugerir crecimiento de cavidades cardíacas.
- Presencia de hepatomegalia: es un indicador de congestión venosa central asociada a falla cardiaca retrógrada.
- Palpación de pulsos braquiales y femorales: se valora su intensidad y simetría, permite valorar diferencias que pueden presentarse en patologías como la Coartación de Aorta.
- Soplos cardiacos: siempre son considerados patológicos en los recién nacidos.
- Tensión arterial en las 4 extremidades: debe presentar mediciones similares entre las 4 extremidades, con diferencias entre miembros inferiores y superiores que no sean mayores a 10 mm Hg. Deben registrarse estas mediciones en la historia clínica y hace parte del examen físico neonatal completo exigido en la Resolución 3280 de 2018 o la norma que la modifique o sustituya.
Relación con los demás componentes de la Atención Integral en Salud y las Rutas Integrales de Atención en Salud.
Reconociendo que la cardiopatía congénita compleja es una agrupación de patologías distintas que pueden llegar a requerir un manejo diferente, el objetivo principal de esta línea de tamizaje dentro del Programa de Tamizaje Neonatal consiste en la identificación de los niños con sospecha de cardiopatía congénita compleja y la garantía de su evaluación diagnóstica urgente. La evaluación diagnóstica, el tratamiento y el seguimiento debe hacerse en el marco de la atención resolutiva que se necesite, sin barreras de ningún tipo.
Todo niño o niña, independiente del resultado del tamizaje neonatal con pulsooximetría o de la presencia de factores o antecedentes de riesgo o de alteraciones al examen físico, tiene derecho a la atención resolutiva particular a su condición, pero también al resto de los procedimientos y atenciones enunciados en los Lincamientos Técnicos y Operativos de la RIAMP y la RIAPMS de la Resolución 3280 de 2018 o la norma que la modifique o sustituya. En el caso de tener un tamizaje positivo o de cumplir algunos de los criterios de mayor riesgo para la salud, la supervivencia y del desarrollo de la mencionada Resolución, deben ser considerados como niños de mayor riesgo y recibir la valoración integral en salud acorde a su condición de riesgo.
Bibliografía
1. Kyriakíe S and cois. Capitulo 1. Newborn screening, emergency treatment and molecular testing. In: Pediatric Endocrinology and Inborn Errors of Metabolism Second Edition. McGraw Hill; 2017.
2. Uribe AG, Gómez FR, Muños NJM, Bernal GB. Guía de práctica clínica del recién nacido sano [Internet], MinSalud Colombia. 2013. 50 p. Available from: https://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/INEC/IETS/GPC_Pro f_Sal_RNSano.pdf
3. Guía de práctica clínica Detección de anomalías congénitas en el recién nacido. 2013.
4. Instituto Nacional de Salud (INS). Informe de evento 2024 Parotiditis. 2025; 1-41. Available from: https://www.ins.gov co/buscador- eventos/Informesdeevento/PAROTIDITIS INFORME DE EVENTO 2024.pdf
5. Andermann A, Blancquaert I, Beauchamp S, Déry V. Revisiting Wilson and Jungner in the genomic age: A review of screening criteria overthe past 40 years. Bull World Health Organ. 2008;86(4):317-9.
6. Salud IN de. Informe técnico repositorio de tamizaje neonatal 2024. 2024.
7. Hidalgo AM, Fuya OP, Martínez DP. Repositorio de tamizaje neonatal, una herramienta para la toma de decisiones en salud pública. Biomedica. 2025;45(4):599-611.
8. Unido R. Handbook Public Health. 2021. Newborn blood spot screening: programme handbook. Available from: https://www.gov.uk/government/publications/health- professional-handbook-newborn-blood-spot-screeníng
9. Australia. New South Wales. 2025. Newborn Screening Program de Australia. Available from: https://www.schn.health.nsw.gov.au/nsw-newborn-screening-program
10. Smith WE, Berry SA, Bloom K, Brown C, Burton BK, Demarest OM, et al. Phenylalanine hydroxylase deficiency diagnosis and management: A 2023 evidence-based clinical guideline of the American College of Medical Genetics and Genomics (ACMG). Genet Med. 2025;27(1).
11. Francia Patricia Correa, Reggie García Robles, Dora Beatriz Robayo G AJB Actualización de las recomendaciones técnicas y operativas para laboratorios de Tamizaje Neonatal. Inst Nac Salud. 2022;1:1-45.
12. van Wegberg AMJ, MacDonald A, Ahring K, Bélanger-Quintana A, Bebió S, Blau N, et al. European guidelines on diagnosis and treatment of phenylketonuria: First revisión. Mol Genet Metab. 2025;145(2).
13. Bodamer, O., Hahn S. OverView of phenylketonuria. Up to date [Internet], 2025; Available from: https://www.uptodate.com/contents/phenylketonuria-overview
14. Andoni M. Tratamiento dietético nutricional del paciente pediátrico y adolescente con FENILCETONURIA en 1o, 2° y 3er nivel de atención [Internet]. GPC. Guía de Práctica Clínica. Catálogo maestro de guías de práctica clínica. 2016. 1-52 p. Available from: http://www.imss.gob.mx/sites/all/statics/guiasclinicas/554GER.pdf
15. Urrego MV. Recomendaciones para la creación del programa de detección y manejo inicial de errores innatos del metabolismo en la población infantil menor de un año para Colombia. Repos Univ Nac Colomb [Internet]. 2014;2014. Available from: https://repositorio.unal.edu.co/bitstream/handle/unal/51846/05599287.2014.pdf7seque nce=1&isAllowed=y
16. Jameson E, Remmington T, Dietary interventions for phenylketonuria. Cochrane Database Syst Rev. 2020;2020(7).
17. Sutton, R, Rand, E., & Hahn S. UpToDate. 2022. Galactosemia: Clinical features and diagnosis. Available from: https://www.uptodate.com/contents/galactosemia-clinical- features-and-diagnosis
18. Welling L, Bernstein LE, Berry GT, Burlina AB, Eyskens F, Gautschi M, et al. International clinical guideline for the management of classical galactosemia: diagnosis, treatment, and follow-up. J Inherit Metab Dis. 2017;40(2):171-6.
19. Brook M. Pyhtila KAS et al. Newborn Screening for Galactosemia in the United States: Looking Back, Looking Around, and Looking Ahead. JIMD Rep. 2014;4:113-6.
20. CENETEC. GALACTOSEMIA. Tamizaje, diagnóstico, tratamiento médico de las complicaciones e intervención nutricional. GPC Guía Práctica Clínica Catálogo Maest guías práctica clínica [Internet]. 2017,54. Available from: https://cenetec- difusion.com/gpc- sns/?p=726%0Ahttp://www.imss.gob.mx/s¡tes/all/statics/guiasclinicas/536GER.pdf
21. López Mejía L, Vergara Vázquez M, Guillén López S, López Olivan F. Actualidades en el tratamiento nutricional de pacientes con galactosemia clásica. Acta Pediátrica México. 2018;39(6);75
22. CENETEC. GPC Evidencias y Recomendaciones. Cenetec [Internet], 2012,59. Available from: http://www.cenetec.salud.gob.mx/descargas/gpc/CatalogoMaestro/141_GPC_HEMOFI LIA_PEDIATRICA/lmss_ER.pdf
23. España M de SG de. PROTOCOLO DE CRIBADO NEONATAL. 2020;
24. Porta F, Pagliardini V, Celestino I, Pavanello E, Pagliardini S, Guardamagna O, et al. Neonatal screening for biotinidase deficiency: A 30-year single center experience. Mol Genet Metab Reports [Internet]. 2017;13(September):80-2. Available from: http://dx.doi.Org/10.1016/j.ymgmr.2017.08.005
25. Wolf B. Biotinidase deficiency. Gene Rev. 2023;
26. Seoane Mato D. Cribado neonatal del déficit de biotinidasa Neonatal screening for biotinidase deficiency Red española de agencias de evaluación de Tecnologías y pResTaciones del sisTema nacional de salud. 2014; 1-88. Available from: https://www.sergas.es/docs/Avalia-t/avalia_t201307Cribadodeficitbiotinidasa.pdf
27. Castellani C, Duff AJA, Bell SC, Heijerman HGM, Munck A, Ratjen F, et al. ECFS best practice guidelines: the 2018 revisión. J Cyst Fibros [Internet], 2018; 17(2): 153-78. Available from: https://doi.org/10.1016/j_jcf.2018.02.006
28. Ministerio de Salud. Guia de fibrosis quística. 2014.
29. Vásquez C, Aristizábal R, Daza W. Fibrosis quística en Colombia. Registro Colombiano de Fibrosis Quística. Primer informe. Rev Neumol Pediatr [Internet], 2010;5(1):44-50. Available from: http://www.neumologia-pediatrica.cl
30. Saza, L„ Soler J. DIFICULTADES EN EL PROCESO DIAGNÓSTICO DE UNA COHORTE CON FIBROSIS QUISTICA EN COLOMBIA. Repos Univ del Rosario. 2018¡302-8.
31. Comités Nacionales de neumologia, Nutrición G y G de T de K. Guia De Diagnóstico Y Tratamiento De Pacientes on Fibrosis Quística. Actualización. Com Nac Neumonol Nutr Gastroenterol y Grup Trab Kinesiol [Internet]. 2015;65. Available from: https://www.sap.org.ar/uploads/consensos/gu-iacutea-de-diagn-oacutestico-y- tratamiento-de-pacientescon-fibrosis-qu-iacutestica-actualizaci-oacuten.pdf
32. Munck A, Southern KW, Castellani C, de Winter-de Groot KM, Gartner S, Kashirskaya N, et al. Defining key outcomes to evalúate performance of newborn screening programmes for cystic fibrosis. J Cyst Fibros [Internet], 2021;20(5):820-3. Available from: https://doi.Org/10.1016/j.jcf.2021.02.006
33. Arrudi-Moreno M, García-Romero R, Samper-Villagrasa P, Sánchez-Malo MJ, Martin- de-Vicente C. Cribado neonatal de fibrosis quística: análisis y diferencias de los niveles de tripsina inmunorreactiva en recién nacidos con cribado positivo. An Pediatría. 2021;95(1):11-7.
34. Castellani C, Massie J, Sontag M, Southern KW. Newborn screening for cystic fibrosis. Lancet Respir Med [Internet], 2016;4(8):653-61. Available from: http://dx.d0i.0rg/10.1016/S2213-2600(16)00053-9
35. Dayasiri K, Hull J, Rao S. NICE guidance on diagnosis and management of cystic fibrosis. Arch Dis Child Educ Pract Ed. 2021;106(1):31-4.
36. Godoy C, Brito PP, Amorim T, Souza EL, Boa-Sorte N. IRT/IRT as a newborn cystic fibrosis screening method: optimal cutoff points for a mixed population. Cad Saude Publica. 2025;40(7).
37. Castellani C, Linnane B, Pranke I, Cresta F, Sermet-Gaudelus I, Peckham D. Cystic Fibrosis Diagnosis in Newborns, Children, and Adults. Semin Respir Crit Care Med. 2019;40(6):701-14.
38. Castellani C, Simmonds NJ, Barben J, Addy C, Bevan A, Burgel PR, et al. Standards for the care of people with cystic fibrosis (CF): A timely and accurate diagnosis. J Cyst Fibros. 2023;22(6):963-8.
39. Katkin J. UpToDate. 2022. Cystic fibrosis: Clinical manifestations and diagnosis. UptoDate. Available from: https://www.uptodate.com/contents/cystic-fibrosis-clinical- manifestations-and-diagnosis
40. Castells EM, Sánchez A, Frómeta A, Moksde Y, Silva E, Ozunas N, et al. Newborn Screening Program for Cystic Fibrosis in Cuba: Three Years' Experience. J Inborn Errors Metab Screen. 2023; 11.
41. Farrell PM, White TB, Ren CL, Hempstead SE, Accurso F, Derichs N, et al. Diagnosis of Cystic Fibrosis: Consensus Guidelines from the Cystic Fibrosis Foundation. J Pediatr [Internet]. 2017;181:S4-S15.e1. Available from: http://dx.doi.org/10.1016/jjpeds.2016.09.064
42. Schmidt M, Werbrouck A, Verhaeghe N, De Wachter E, Simoens S, Annemans L, et al. Strategies for newborn screening for cystic fibrosis: A systematic review of health economic evaluations. J Cyst Fibros [Internet], 2018; 17(3):306–15. Available from: https://d0i.0rg/l 0.1016/j.jcf.2018.03.002
43. Latorre S, Garzón C, Manosalva G, Merchán S, Jacomussi L, Maldonado S. Hiperplasia adrenal congénita por déficit de 21 hidroxilasa: un reto diagnóstico y terapéutico. Repert Med y Cirugía [Internet], 2016;25(2):79–88. Available from: http://dx.d0i.0rg/l 0.1016/j.reper.2O16.05.001
44 Dulín Iñiguez E EZB. Cribado neonatal de hiperplasia suprarrenal congénita Newborn screening of congenital adrenal hyperplasia. Endocrino! Diabetes Nutr. 2018,65(1): 1-4.
45. Valiñas L, Lema L, Atienza G. Cribado neonatal de la hiperplasia suprarrenal congénita. Revisión sistemática. 2014;
46. Sharma L, Momodu II SG. Congenital Adrenal Hyperplasia. StatPearls Treasure Isl [Internet]. 2025; Available from: https://www.ncbi.nlm.nih.gov/books/NBK448098/
47. Sarafoglou K, Merke DP, Reisch N, Claahsen-Van Der Grinten H, Falhammar H, Auchus RJ. Interpretaron of Steroid Biomarkers in 21-Hydroxylase Deficiency and Their Use in Disease Management. J Clin Endocrinol Metab [Internet], 2023; 108(9):2154-75. Available from: https://doi.org/10.1210/clinem/dgad134
48. P. MCS. Drepanocitosis en Colombia: análisis de la notificación como enfermedad huérfana o rara al sistema de vigilancia en salud pública, 2016 y 2017. Inf epidemiológico Nac [Internet], 2018;1 - 14. Available from: https://www.mendeley.com/catalogue/a0de1a44-71ac-3d4c-912e-49e9077ab659/
49. Quarmyne MO, Bock F, Lakshmanan S, Attell BK, Snyder A, Boudreaux J, et al. Newborn Screening for Sickle Cell Disease and Thalassemia. JAMA Heal Forum. 2025;6(3):1-10.
50. New York. United Nations. Recognition of sickle-cell anaemia as a public health problem. United Nations Gen Assem. 2008;A/RES/63/2:1-2.
51. Queiro T. Cribado neonatal de la anemia falciforme Cribado neonatal de la anemia falciforme Neonatal screening for sickle cell disease. Cons Sanidade [internet], 2013; Available from: http://www.sergas.es/Docs/Avalia-t/avalia-t201202anemia-falciformeDef.pdf
52. Frómmel C. Newborn screening for sickle cell disease and other hemoglobinopathies: A short review on classical laboratory methods – Isoelectric focusing, HPLC, and capillary electrophoresis. Int J Neonatal Screen. 2018;4(4).
53. Bain BJ, Daniel Y, Henthorn J, de la Salle B, Hogan A, Roy NBA, et al. Significant haemoglobinopathies: A guideline for screening and diagnosis: A British Society for Haematology Guideline. Br J Haematol. 2023;201(6):1047-65.
54. Mosca A, Paleari R, Palazzi G, Pancaldi A, lughetti L, Venturelli D, et al. Screening for sickle cell disease: Focus on newborn investigations. Clin Chem Lab Med [Internet], 2024;62(9):1804-13. Available from: https://doi.org/10.1515/cclm-2024-0478
55. Jilek R, Marcy J, Johnson C, YoungerG, Calhoun A, Tung ML. lowa Newborn Screening Program Experience with Hemoglobinopathy Screening overthe LastTwo Decades and Its Increasing Global Relevance. Int J Neonatal Screen. 2024; 10(1).
56. Ordóñez L, Diaz D, González-Marín N, Rueda R, Silva R, Ramírez C, et al. Tamizaje auditivo neonatal en pacientes de alto riesgo con otoemisiones acústicas: evaluación de resultados. ACTA Otorrinolaringol CIRUGÍA CABEZA Y CUELLO. 2018;45(2):112-20.
57. Nazar G, Goycoolea M, Godoy JM, Ried E, Sierra M. Universal newborn hearing screening: Review of 10,000 evaluations. Rev Otorrinolaringol y cirugía cabeza y cuello. 2009;
58. Busa J, Harrison J, Chappell J, Yoshinaga-ltano C, Grimes A, Brookhouser PE, et al. Year 2007 position statement: Principies and guidelines for early hearing detection and intervention programs. Pediatrics. 2007.
59. Ministerio de Salud y la Protección Social. Resolución 3280 de 2018. "Por medio de la cual se adoptan los lineamientos técnicos y operativos de la Ruta de Atención para la Promoción y Mantenimiento de la salud y la Ruta Integral de Atención en Salud para la Población Materno Perinatal." Resolución 3280 [Internet], 2018;1-348. Available from: https://www.minsalud.gov.co/Normatividad_Nuevo/Resolucion No. 3280 de 20183280. pdf%OAhttps://www.m¡nsalud.gov.co/s¡tes/rid/Lists/Bibl¡otecaD¡g¡tal/RIDE/D E/DIJ/resolucion-3280-de-2018.pdf
60. Sánchez Vanegas, G., Buitrago García, D. C., Moreno, C., Segura, M. M., Fernández Jaramillo J, Solano Franco, A. Angulo S. Guía de práctica clínica para la detección temprana, el diagnóstico, el tratamiento y el seguimiento de los defectos refractivos en menores de 18 años. Pediatría. 2017;
61. Wallace DK, Morse CL, Melia M, Sprunger DT, Repka MX, Lee KA, et al. Pediatric Eye Evaluations Preferred Practice Pattern®. Ophthalmology. 2018;
62. Reyes-Morales D, Salgado-Valladares MB. Diagnóstico de alteraciones oculares anatómicas y funcionales en neonatos TT - Anatomic and functional diagnosis of ocular abnormalities in neonates. Perinatol Reprod Hum. 2013;
63. Ambou Frutos I, Liana Lastra Pérez I, Deysi Vilches Lescaille I, Lisis Osorio Illas I, Meysi Ramos López I, Nasibis Rodríguez Ahuar I Instituto Cubano de Oftalmología II, et al. Manifestaciones clínicas asociadas al síndrome de TORCH Clinical manifestations associated to the TORCH syndrome. Revista Cubana de Oftalmología. 2018.
64. Duarte FOM, García AR, Bedoya MR, Rángel GS. Reporting of birth defects from the Zika outbreak in Colombia, 2015-2017. Rev Panam Salud Publica/Pan Am J Public Heal. 2019;43:2015-7.
65. Mendivelso Duarte FO, Robayo García A, Rodríguez Bedoya M, Suárez Rángel G. Notificación de defectos congénitos por brote del virus del Zika en Colombia, 2015-2017. Rev Panam Salud Pública. 2019;
66. Zarante I, Franco L, López C, Fernández N. Frecuencia de malformaciones congénitas: evaluación y pronóstico de 52.744 nacimientos en tres ciudades colombianas. Biomédica. 2010;
67. Molina M. N, Paez P, Cordovez Wandurraga C. Alteraciones visuales y oculares en pacientes con síndrome de Down. Cieñe y Tecnol para la Salud Vis y Ocul. 2008;
68. Gamm DM, Kulkarni AD, Albert DM. Retinoblastoma. In: Garner and Klintworth's Pathobiology of Ocular Disease Part B, Third Edition. 2007.
69. Cortés-González V, Villanueva-Mendoza C. Epidemiología del glaucoma congénito en la Asociación para Evitar la Ceguera en México, revisión de 5 años. Rev Mex Oftalmol. 2015;
70. Khokhar S, Pillay G, Dhull C, Agarwal E, Mahabir M, Aggarwal P. Pediatric cataract. Indian Journal of Ophthalmology. 2017.
71. Gilbert C, Foster A. Childhood blindness in the context of VISION 2020 - The right to sight. Bull World Health Organ. 2001;
72. García RU, Peddy SB. Heart Disease in Children. Prim Care - Clin Off Pract [Internet], 2018;45(1):143-54. Available from: https://doi.Org/10.1016/j.pop.2017.10.005
73. Cullen Benítez PJ, Guzmán Cisneros B. Tamiz de cardiopatías congénitas críticas. Recomendaciones actuales. Acta Médica Grup Ángeles [Internet], 2014;12(1 ):24-9. Available from: https://www.medigraphic.com/pdfs/actmed/am-2014/am141d.pdf
74. Oster ME, Pinto NM, Pramanik AK, Markowsky A, Schwartz BN, Kemper AR, et al. Newborn Screening for Critical Congenital Heart Disease: A New Algorithm and Other Updated Recommendations: Clinical Report. Pediatrics. 2025; 155(1): 1-9.
1. Los EINI propuestos a tamizar son: Hípotiroidismo congénito, hiperplasia suprarrenal congénita, deficiencia de biotinidasa, fenilcetonuria. galactosemia, deficiencia de acil CoA deshidrogenasa de cadena media (MCAD) o acidarías orgánicas (acidemia propriónica y acidemia metiimalónica).
2. Seguido por los defectos del sistema osteomuscular con 68,1 casos por cada 10.000 nacidos vivos y los defectos del sistema nervioso central con 25,7 casos por cada 10.000 nacidos vivos.
3. La condición buscada debe ser un problema de salud importante, debe existir un tratamiento aceptado para los pacientes con enfermedad reconocida, el diagnóstico y tratamiento deben estar disponibles, debe existir una etapa de latencia asintomática temprana reconocible, debe haber una prueba de tamizaje reconocida, la prueba debe ser aceptada por la población, la historia de la enfermedad conocida y tratamiento reconocido.
4. Esta definición de las patologías a incluir en el tamizaje debe ser validada con el IETS (Instituto de Evaluación Tecnológica en Salud) en lo que corresponde a la valoración de costos, de tal manera que la decisión del sistema de salud sea sustentable en el tiempo. La consideración debe sopesar el impacto en los individuos afectados contra la carga para los individuos no afectados
5. Un análisis de Programas de Tamizaje Neonatal en Europa en 2010 mostró la gran variabilidad en términos de condiciones incluidas (de 2 hasta 30); educación a las familias, consentimiento informado; edad de recolección de la muestra, metodología de screening. almacenamiento de muestra así como confirmación diagnóstica, tratamiento y seguimiento.
6. Debe explicarse la naturaleza del examen de tamizaje, para evitar riesgos psicosociales asociados a falsos positivos en los cuales es descartada posteriormente la patología. Otros riesgos asociados a: i) la toma de muestra de sangre: hematoma o infección y, ii) toma de saturación: equimosis.
7. Las directrices, conceptos o disposiciones relacionados con la toma, manejo, almacenamiento y transporte de la muestra; su procesamiento analítico; así como todos los aspectos que considere necesarios para avanzar en la calidad del tamizaje neonatal, serán definidos por el INS.
8. El retardo mental asociado al tiempo de hipotiroidismo congénito sin tratamiento muestra que el recién nacido antes del mes, puede tener secuelas neurológicas: de 1 a 3 meses, las secuelas dependen del caso y la severidad (se estima que por cada día que pasa pierden un punto de coeficiente intelectual) y aquellos niños y niñas con más de 3 meses que no reciben tratamiento, tendrán secuelas neurológicas.
9. Para el 2025, se establecen los siguientes puntos de corte, de acuerdo con los lineamientos establecidos por el Instituto Nacional de Salud los cuales son sujetos de actualización continua.
10. Para el 2025, se establecen los siguientes puntos de corte, de acuerdo con los lineamientos establecidos por el Instituto Nacional de Salud los cuales son sujetos de actualización continua
11. En articulación con los demás actores que tienen responsabilidad en este proceso de gestión (EAPB y DTS)
12. En la Resolución 3280 se menciona Respuesta Auditiva de Tallo Encefálico Automatizada (RATEA), sin embargo, la denominación en CUPS actualmente de la tecnología es 954632: Potenciales Evocados Auditivos de Corta Latencia Automatizados Medición de Maduración (PEAA)
13. Se determinaron como factores de riesgo para hipoacusia: antecedente familiares de sordera. Recién nacidos con Bajo peso al nacer (BPN): <2500 gr, Recién nacido prematuro: <37 semanas; estigmas asociados a un síndrome (Espectro Oculo-Aurículo-Vertebral o Síndrome de Goldenhar, Labio y/o paladar Hendido, Malformación anatómica auricular y/o CAE, Síndrome de Down, Malformaciones congénitas de cabeza y cuello y Síndromes relacionados con desordenes auditivo-vestibulares): meningitis o neuroinfección (Infecciones del oído. Secuelas de meningitis), hiperbilirrubinemia (aún sin incompatibilidad de RH) que requiere manejo con fototerapia o exanguinotransfusión, antecedentes maternos de exposición a ototóxicos; examen necrológico anormal (Reflejos auditivos alterados. Retraso del desarrollo motor); traumas prenatales que puedan afectar al feto; Trastorno respiratorio; Traumas perinatales; Infecciones maternas de Rubéola, Citomegalovirus, sífilis, herpes, toxoplasma. VIH. o sospecha de Zika o Chikungunya (mientas se disponga de prueba serológica) u otras infecciones intrauterinas que pueden generar riesgo de hipoacusia; Hipoxia permatal - criterios por clínica o gases arteriales, incluye estado fetal insatisfactorio, hipoxia prenatal y RN que requiere maniobras; RN en UCI neonatal con requerimiento de oxígeno; Hipotiroidismo o errores congénitos del metabolismo.
14. El pliegue del epicanto es un pliegue del párpado superior que cubre la esquina interna del ojo Por lo general, los niños muy pequeños lo tienen, lo cual es normal, y también es común en las personas de descendencia asiática. El pliegue del epicanto puede ser un rasgo diagnóstico importante en algunas condiciones tales como el síndrome de Down.
15. Estrabismo convergente.
16. A excepción de los casos de antecedente de enfermedades visuales / oculares genéticas o congénitas.
17. También Se consideran factores de riesgo para alteraciones oculares: Hipoxía perinatal, Riesgo o sospecha de lesión neurológica aguda (hipoglicemia severa, convulsiones, ictericia severa no tratada, sepsis con afectación de SNC o candidemia)


